Autophagy:徐州医科大学王午阳团队发现,靶向溶酶体离子通道可治疗胰腺癌
2021-04-26 haibei MedSci原创
在最近的研究中,研究人员表明,通过增加MCOLN1通道的表达或使用MCOLN1激动剂ML-SA5或MK6-83来激活MCOLN1,可以扰乱自噬体和溶酶体之间的融合,以阻止细胞自噬流的进行。
自噬是一种进化上保守的降解过程,有助于清除不需要的蛋白质和受损的细胞器,并为细胞的生存提供必要的营养,特别是在各种压力条件下。已有的研究显示,为了保证癌细胞生长对营养物质的高需求,细胞自噬有所提升。

最近,研究人员发现,MCOLN1/TRPML1是胰腺癌、乳腺癌、胃癌、恶性黑色素瘤和胶质瘤等癌症中致癌性自噬的药物目标。MCOLN1/TRPML1是一种特异性定位于溶酶体的非选择性阳离子通道,在调节包括内吞、外吞、溶酶体适应和自噬等多种细胞过程中起着关键作用。迄今为止,MCOLN1的既定功能归因于它能够调节钙离子从溶酶体的释放,钙离子是一种重要的第二信使,有利于囊泡融合/分裂。
在最近的研究中,研究人员表明,通过增加MCOLN1通道的表达或使用MCOLN1激动剂ML-SA5或MK6-83来激活MCOLN1,可以扰乱自噬体和溶酶体之间的融合,以阻止细胞自噬流的进行。此外,研究人员还证明了MCOLN1通过介导锌从溶酶体的释放来调节自噬。最后,研究人员发现来自MCOLN1的锌流入阻断了自噬小体中STX17(syntaxin 17)和溶酶体中VAMP8的相互作用,从而破坏了由这两个SNARE蛋白决定的融合过程。
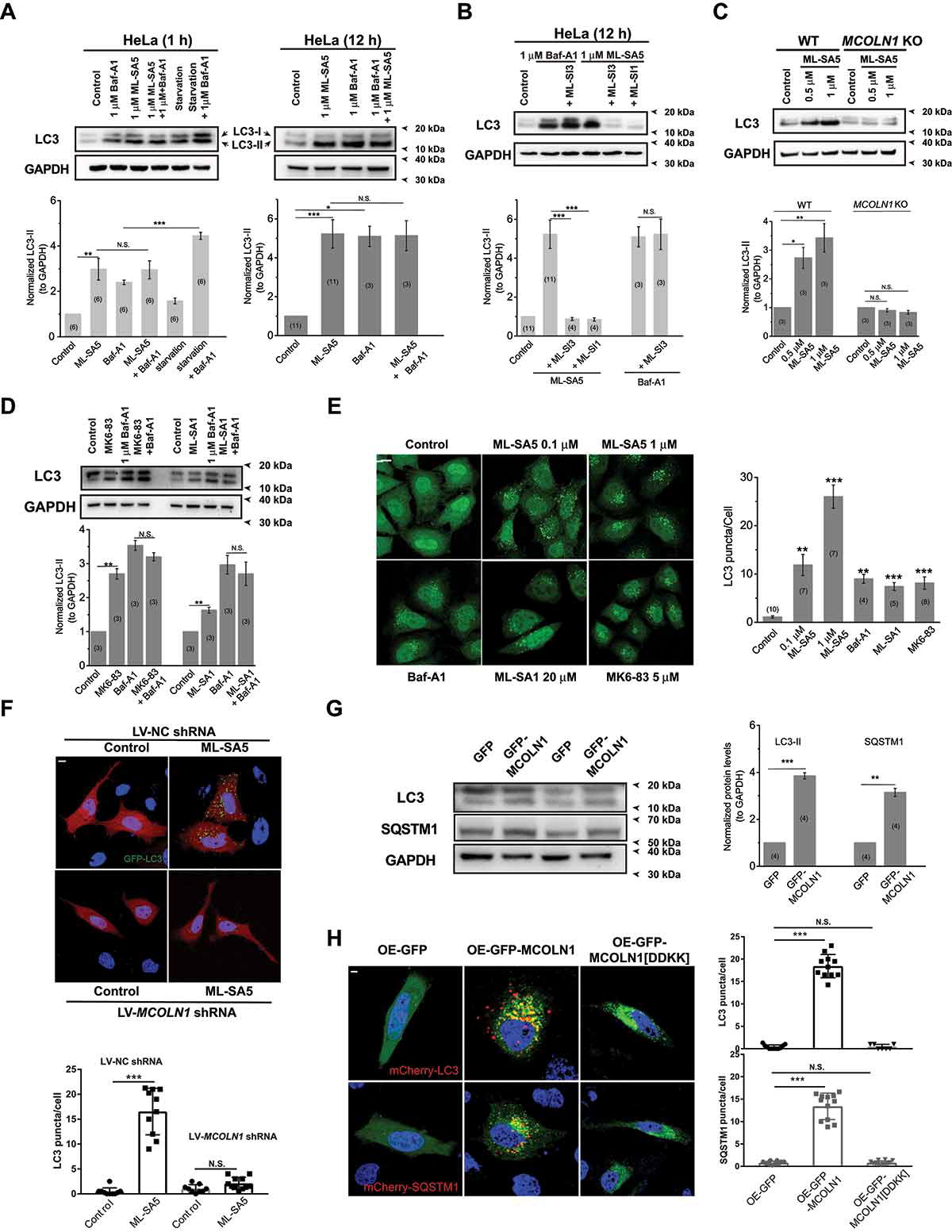
MCOLN1的激活能特异性地调节自噬
在此基础上,研究人员证明了源自细胞外液的锌流入可以通过与溶酶体锌相同的机制阻止自噬,证实了锌作为膜贩运参与者的基本功能。并且,用激动剂ML-SA5或MK6-83激活MCOLN1,可以通过唤起自噬停滞和随后的凋亡反应及细胞周期停滞,引发一些癌细胞的死亡,而对正常细胞几乎没有影响。
与体外结果一致的是,在Patu 8988 t异种移植小鼠中施用ML-SA5能有效抑制肿瘤的生长并提高生存率。
总之,这些结果表明,溶酶体阳离子通道MCOLN1通过介导锌流入细胞质,来精细地控制癌症中的致癌自噬。
原始出处:
Jiansong Qi et al. MCOLN1/TRPML1 finely controls oncogenic autophagy in cancer by mediating zinc influx. Autophagy (2021).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#医科大学#
45
#离子通道#
59
学习了
67
学习了
68
这些结果表明,溶酶体阳离子通道MCOLN1通过介导锌流入细胞质,来精细地控制癌症中的致癌自噬。
66