美国FDA批准Omadacycline抗生素上市
2018-08-12 MedSci MedSci原创
今天Paratek宣布其改良四环素omadacycline获得FDA专家组支持上市用于急性细菌皮肤感染(17票支持、1票反对)和社区获得性肺炎(14票支持、四票反对)。Omadacycline有静脉滴注和口服两个剂型,前者用于住院治疗、后者用于出院后继续治疗。该产品已经在三个三期临床达到与莫西沙星比非劣效的试验终点,PDUFA日期是今年十月。如果FDA批准该药上市Paratek准备明年开始销售
今天Paratek宣布其改良四环素omadacycline获得FDA专家组支持上市用于急性细菌皮肤感染(17票支持、1票反对)和社区获得性肺炎(14票支持、四票反对)。Omadacycline有静脉滴注和口服两个剂型,前者用于住院治疗、后者用于出院后继续治疗。该产品已经在三个三期临床达到与莫西沙星比非劣效的试验终点,PDUFA日期是今年十月。如果FDA批准该药上市Paratek准备明年开始销售,专家预计峰值销售为5亿美元(ECCMID 2016:Omadacycline是安全有效的皮肤感染治疗药物)。
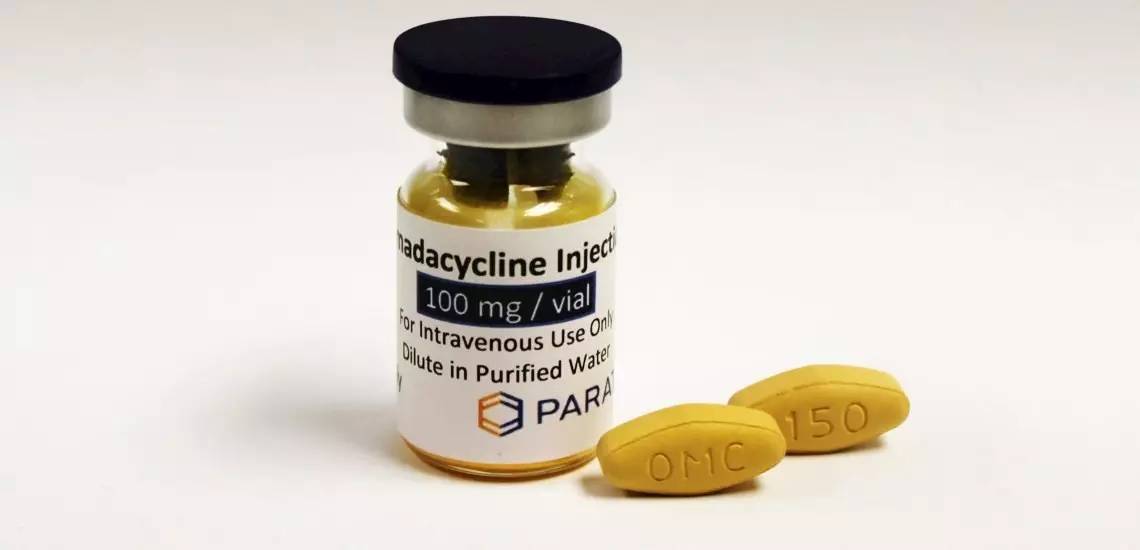
Omadacycline 是一种新型口服施用或静脉注射的一天一次抗生素,对 Gram 阳性、Gram 阴性和非典型细菌具有广谱活性。它正在被开发作为社区获得性细菌感染的经验性治疗,包括急性细菌性皮肤及皮肤结构感染、社区获得性肺炎(CABP)、尿路感染及其他社区获得性感染。Omadacycline 在美国已经获得合格传染病产品(QIDP)认证和快速通道资格。
与每日两次只口服(twice-daily, oral-only)利奈唑胺相比较,研究人员在名为 OASIS-2、涉及 735 例 ABSSSI 成人患者的关键性 3 期临床研究评估了每日一次只口服(once-daily, oral-only)omadacycline 方案的疗效和安全性。接受第一剂药物 48〜72 小时后,在早期临床反应(ECR)指标中,与利奈唑胺相比,omadacycline 达到了 FDA 在修订意向治疗(mITT)人群(10%NI 保守度,95%置信区间)中指定的统计学非劣性(NI)主要终点。Omadacycline 的 ECR 率为 87.5%,而利奈唑胺为 82.5%。针对最常见的 ABSSSI 病原体(包括耐甲氧西林金黄色葡萄球菌,MRSA)引起的感染,omadacycline 具有高的临床成功率。 Paratek 公司首席运营官兼首席医疗总裁 Evan Loh 博士说道:“我们对只口服给药皮肤感染适应症研究中观察到的卓越疗效感到兴奋,这与 OASIS- 1 和 OPTIC 研究中观察到的疗效一致。本研究的完成率和有效率非常高,证实了 omadacycline 只需口服方案的效益,以及我们对 omadacycline 获得 ABSSSI 和 CABP 批准的信心。”
耐药菌感染是个已经发生的健康威胁,而且这个威胁会越来越严重。据CDC估计每年美国发生200万例耐药菌感染,死亡23,000人。更严重的超级耐药菌出现也只是早晚的事情,前几天业界大佬还警告现在社会对超级耐药菌的威胁有点漫不经心。2016年美国发现首例mcr-1多粘菌素耐药感染、2017年发生过一起对所有13类抗生素都耐药死亡案例,而现在的抗生素研发投入力度确实有轻敌嫌疑。大公司纷纷退出这个领域,最近一个是诺华、上个月宣布退出抗生素研发。

Omadacycline是一种改良的新型四环素(图片来源:Paratek官网)
现在只有一些小公司还奋战在抗生素领域,但多数在中晚期临床研究的抗生素都是对已有药物的微小改进。Omadacycline化学结构与10年前上市的tigecycline只差一个羰基,所有四环素的关键药效团都没有变化。去年奥地利生物技术公司Nabriva的lefamulin在一个CABP三期临床试验中与莫西沙星比显示非劣效,结构与葛兰素老药Retapamulin也只是侧链有点区别。但即使这样微小变化也不能保证就能和标准疗法比达到非劣效、更不用说击败标准疗法了。如Tetraphase的主打产品eravacycline先后在两个复杂尿路感染的非劣效三期临床失败,现在市值与巅峰时比已经损失90%以上。Cempra的大环内酯抗生素solithromycin虽然疗效达到非劣效,但安全性受到一些质疑、FDA要求再做一个9000人的安全性试验。Cempra去年几乎以手上现金储备价格卖给Merlinta、投资者损失惨重。抗生素一般合成复杂、构效关系研究难度较大,找到Omadacycline这样显示非劣效的新类似物已经不容易,但是这种创新不大可能有效应对超级耐药菌的入侵。Omadacycline只是微量创新,之于超级耐药菌如同创可贴之于枪伤、实在勉为其难。
中国初创公司再鼎医药与美国专注于四环素衍生物开发及商业化的创新公司Paratek制药达成合作,前者获得了Omadacycline在中国的开发及商业化许可。根据协议,再鼎医药获得了Omadacycline在大中华地区(包括中国大陆、香港、澳门及台湾)的独家开发和商业推广许可。同时,双方需要建立联合指导委员会以审评和监督所有的开发细节。Paratek 制药将会获得750万美元的首付金并会得到后期开发、注册及上市的里程碑款项,再鼎同时还要支付Omadacycline在大中华地区销售收入的分成。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#FDA批准#
36
#ADA#
26
#Omadacycline#
0
#美国FDA#
43
新型的抗生素
69
学习了,谢谢分享
77
不错的文章值得拥有
81