Cell Res:复旦大学周俭/杨欣荣/樊嘉等发现肝癌侵袭区促进肝细胞-肿瘤细胞串扰、局部免疫抑制和肿瘤进展
2023-06-26 iNature iNature 发表于上海
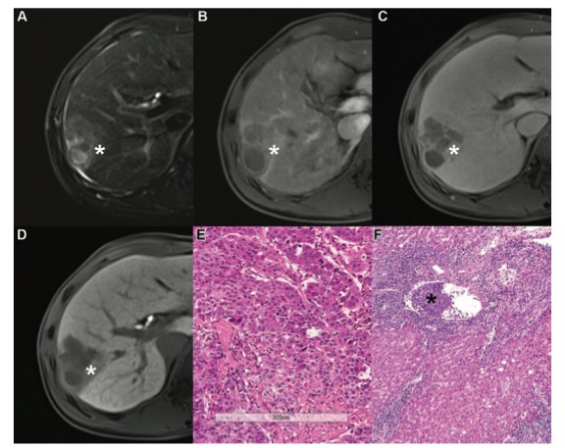
该研究利用纳米级分辨率的新型肿瘤边界扫描和数字化模型-空间增强分辨率组学测序,在肝癌患者的肿瘤边界周围发现了一个500 μ m宽的区域,称为“侵袭区”。
剖析和理解肿瘤生态系统,特别是肿瘤边缘的生态系统对肿瘤细胞的浸润和侵袭具有重要意义,对于探索肿瘤转移机制和开发有效的新治疗方法至关重要。
2023年6月19日,复旦大学周俭、杨欣荣、樊嘉和华大生命科学研究院陈奥、刘石平等团队合作在Cell Research在线发表了题为“An invasive zone in human liver cancer identified by Stereo-seq promotes hepatocyte–tumor cell crosstalk, local immunosuppression and tumor progression”的研究论文,该研究利用纳米级分辨率的新型肿瘤边界扫描和数字化模型-空间增强分辨率组学测序(Stereo-seq),在肝癌患者的肿瘤边界周围发现了一个500 μ m宽的区域,称为“侵袭区”。在该区域检测到强烈的免疫抑制、代谢重编程和严重受损的肝细胞。该研究还发现了位于肿瘤旁附近的受损肝细胞亚群,其血清淀粉样蛋白A1和A2(统称为SAAs)的表达增加。
相邻恶性细胞中CXCL6的过表达可诱导附近肝细胞中JAK-STAT3通路的激活,从而导致这些肝细胞中SAAs的过表达。此外,侵袭区肝细胞过度表达和分泌SAAs可导致巨噬细胞募集和M2极化,进一步促进局部免疫抑制,可能导致肿瘤进展。另外5组原发性和继发性肝癌患者独立队列(n = 423)的临床关联分析显示,侵袭区过表达SAAs的患者预后较差。进一步利用小鼠肝肿瘤模型原位进行的体内实验证实,敲低肝细胞中编码SAAs的基因可减少肿瘤周围巨噬细胞的聚集,延缓肿瘤生长。人类癌症患者中一个新的侵袭区的识别和表征不仅增加了对肿瘤侵袭和转移机制的重要理解,而且可能为开发晚期肝癌和其他实体肿瘤的新治疗策略铺平道路。

实体瘤是一个复杂的、高度异质性的生态系统,其中癌细胞与各种细胞类型相互作用,包括免疫细胞和基质细胞,以及细胞外基质(ECM)。确定实体瘤异质性是如何建立的以及功能性后果是至关重要的。肿瘤边缘区是肿瘤细胞侵入瘤旁组织并与其他细胞直接接触的区域,是肿瘤细胞浸润和侵袭最活跃的区域。因此,全面了解肿瘤组织的细胞组成、它们的空间异质性以及它们与肿瘤微环境(TMEs)(包括肿瘤边缘区域)的相互作用,不仅将揭示肿瘤如何发展和转移,还将加速新型癌症治疗方法的开发。
单细胞RNA测序(scRNA-seq)是一种强大的工具,可用于在单细胞水平上解剖细胞内和细胞间以及分子动力学。它已被广泛用于表征几种类型的实体瘤和相关的TMEs。然而,单独的scRNA-seq不能提供空间信息。此外,由于缺乏多区域采样,单细胞分辨率下的肿瘤内空间异质性仍然知之甚少。最近,该研究开发了空间增强分辨率组学测序(Stereo-seq),提供纳米级分辨率(直径,220 nm/点),可扩展的检测区域(10 mm × 10 mm),并通过结合DNA纳米球(DNB)模式阵列芯片和RNA原位杂交,能够捕获每个细胞几百个点的数据。Stereo-seq能够在单细胞水平上深入表征整个肿瘤生态系统的功能和位置信息,并精确揭示TME中,特别是肿瘤边缘区域的细胞组成、分布和细胞间通讯。
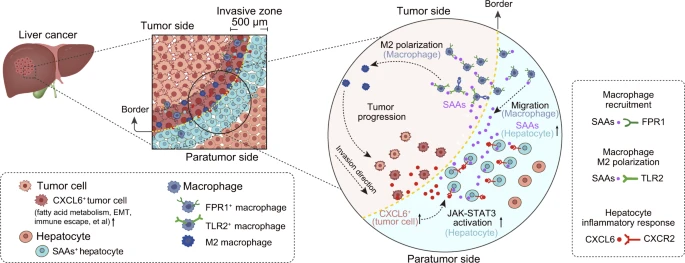
肝癌肿瘤边界的侵袭区的示意图(图源自Cell Research )
肝癌,包括肝细胞癌(HCC)和肝内胆管癌(ICC),是一些最常见和侵袭性的肿瘤类型,由于有限和无效的治疗方案,全球发病率和死亡率很高。肝脏也是其他癌症,特别是肺癌、胰腺癌和结直肠癌远处转移的常见部位。在这项研究中,该研究使用Stereo-seq和scRNA-seq,通过分析多个区域位点,包括肿瘤组织(T)、肿瘤边缘区域(M)、肿瘤旁组织(P)和正常或转移性淋巴结(LN),获得了肝癌肿瘤生态系统和细胞-细胞相互作用的全面全景视图。在将stero -seq数据与scRNA-seq数据整合,构建肿瘤边界扫描和数字化模型,并进行额外的生物信息学分析后,该研究在500µm宽的侵入区(定义为肿瘤边界两侧250µm内的区域)中检测到高度的细胞和转录异质性。
在该区域内,局部免疫微环境受到强烈抑制,肿瘤细胞代谢重编程,肝细胞严重受损,血清淀粉样蛋白A1和A2 (SAA1、SAA2,统称SAAs)高表达。机制上,侵袭性肿瘤细胞分泌C-X-C Motif趋化因子配体6 (CXCL6),激活JAK-STAT3通路,诱导肝细胞(Hep1细胞)中SAAs的表达增强。侵袭区Hep1细胞可分泌SAAs调节巨噬细胞募集,并通过SAAs- TLR2轴诱导M2极化,导致局部免疫抑制和肿瘤进展。该研究在另外5组原发性和转移性肝癌患者中证实了研究发现。
采用原发性肝癌和结肠腺癌肝转移小鼠模型的体内实验表明,腺病毒相关病毒(AAV)介导的肝细胞中SAAs的敲低可显著减少肿瘤周围巨噬细胞的积聚,延缓肿瘤的生长。利用高分辨率和空间分辨率转录组学,该研究精确地表征了肝癌中500 μ m宽侵袭区独特的局部生态系统,这为阐明肿瘤侵袭机制提供了有意义的生物学见解,并可能支持实体瘤新治疗策略的开发。
原文链接:
https://www.nature.com/articles/s41422-023-00831-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言