大脑是人类最重要的器官,不仅控制人体的行为活动,更主导了思考、感觉、语言等各种功能。然而,大脑的结构却柔软如豆腐,幸好大脑外面有坚硬的头骨、三层脑膜和血脑屏障(BBB)捍卫大脑安全。头骨,脑膜和脑脊液可以防止物理损伤,但血脑屏障可有效防止致命病毒和毒素进入大脑,保护中枢神经系统(CNS)免受外界物质损害。
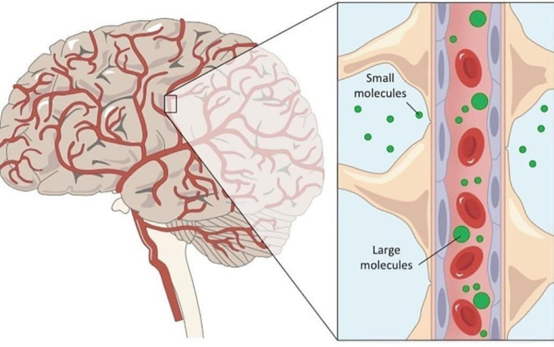
图1 血脑屏障的选择透过性(图源:网络)
BBB是由紧密相连的细胞(主要由周细胞、脑毛细管内皮细胞、基膜、星形胶质细胞足突和脑血管内皮细胞)组成的一层膜,将大脑与身体的其他部分分开。BBB限制性非常强,葡萄糖和其他维持大脑健康和正常运作所需的营养物质,可以通过血脑屏障进入大脑。血液中的毒素、大分子、炎性因子、免疫细胞和有害物质则不能穿过血脑屏障,这有助于预防脑炎症,防止脑损伤。多种中枢神经系统疾病,例如急性脑血管病、阿尔茨海默病(AD)、帕金森病(PD)、多发性硬化(MS)等疾病的发生、发展和转归,与BBB的结构和功能破坏程度密切相关。因此,要进入大脑,物质必须通过形成BBB的细胞,或直接与之相互作用。
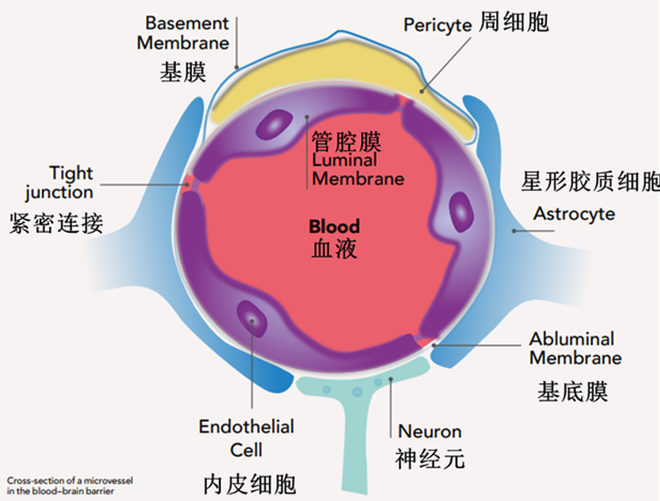
图2 血脑屏障细胞构成简图(图源:网络)
血脑屏障拦不住的HIV,在大脑里“伺机而动”
人类免疫缺陷病毒-1(HIV-1)就拥有穿透血脑屏障的能力。HIV-1可以通过感染血管内皮细胞或破坏血脑屏障进入脑组织,引起艾滋病性神经系统综合症(HNS)。研究表明在HIV-1患者体内,肠道正常菌群中组成成分脂多糖(LPS)含量会显著升高。LPS 进入血液后会侵蚀血脑屏障血管,导致血脑屏障出现裂缝,感染HIV-1的细胞乘机进入大脑;此外,HIV-1可以感染血脑屏障的组成细胞,如血管内皮细胞和巨噬细胞。通过感染和破坏这些细胞,病毒可以绕过血脑屏障,进入大脑组织。
HIV-1一旦进入人体,便将其遗传物质RNA转化为DNA并整合到宿主细胞的DNA中,然后劫持细胞RNA和细胞器,不断产生所需物质,组装新病毒。针对HIV-1的特性,抗逆转录病毒疗法(ART)应运而生。ART阻断HIV复制,将病毒载量降低到无法检测到的水平,且无法传播给他人。ART在抑制病毒方面非常成功,延长了艾滋病患者的寿命,提高了生活质量。ART并非治愈性方法,患者细胞DNA中仍然有病毒基因组的拷贝库。一旦停止治疗,病毒便会卷土重来,再次产生新病毒。
然而,由于BBB的阻隔,某些抗病毒药物在CNS不能达到有效药物浓度,使得这一部位成为病毒潜藏库。脑小胶质细胞(MG)可作为HIV-1的储存库,并在ART停止后引发病毒反弹,但尚未证明MG含有具有复制能力的HIV。
6月15日,北卡罗来纳大学医学院、加州大学圣地亚哥分校、埃默里大学和宾夕法尼亚大学艾滋病治疗中心联合研究小组在The journal of clinical investigation发表了题为“Brain microglia serve as a persistent HIV reservoir despite durable antiretroviral therapy”的研究成果。研究发现大脑MG内的HIV具有复制能力,HIV将MG作为大脑中的病毒潜藏库。

图3 研究成果(图源:[1])
直接测量大脑MG中含有复制能力的HIV,需要从接受抗逆转录病毒疗法HIV感染者(PWH)的中枢神经系统组织中,提取纯的有活力的细胞群。除了在人脑组织取样方面存在明显的伦理障碍外,在分离高纯度MG方面还存在技术障碍。联合团队首先研究了感染猴免疫缺陷病毒(SIV,一种与HIV密切相关的病毒)的猕猴大脑,并成功分离出脑髓细胞(BrMC)和MG;随后,根据从灵长类动物的脑组织中提取和纯化活细胞的经验,对接受ART的HIV感染者进行快速尸检,以探索人类BrMC是否产生具有复制能力的HIV。
利用来自PWH和无HIV人群的脑组织,研究人员成功地分离和体外培养了MG,主要是TEME119+ MG。此外,观察到脑源性MG可以在体外增殖,这可能会提高研究这些细胞的能力。因此,研究人员能够研究MG作为中枢神经系统中持久性HIV感染的“潜藏库”作用。
此项研究能够从一名接受抗逆转录病毒治疗的捐赠者的MG中回收接近FL的HIV,说明大脑MG可以作为HIV的持久性、可诱导的“潜藏库”。从顶叶皮层的MG中培养出的变体与大脑另一区域(基底神经节)的HIV在基因上是相似的,这表明这些库是在大约同一时间建立的,并没有发生实质性的分化。如果在一个脑区产生的病毒感染了其他区域的细胞,然后由于ART的开始或潜伏期的建立而停止复制,就可能发生这种情况。
尽管这项研究受到了来自人类抗逆转录病毒治疗捐赠者的少量样本的限制,但研究人员认为在这个罕见的、独特的队列中的发现是值得注意的。脑部MG是一个稳定的静止感染库,可能是治疗中断后病毒反弹的来源。未来,艾滋病的治疗必须评估HIV在中枢神经系统内的持久性。
此项研究的通讯作者蒋国春博士表示:“HIV非常聪明,随着时间的推移,它已经进化到对其表达有表观遗传控制,使病毒沉默,隐藏在大脑中,不被免疫清除。我们正开始揭开HIV在大脑小胶质细胞中潜伏的独特机制。试图治愈艾滋病,就像试图根除癌症一样。你必须全方面了解它,才能彻底打败它。”
参考文献:
[1]Tang Y, Chaillon A, Gianella S, et al. Brain microglia serve as a persistent HIV reservoir despite durable antiretroviral therapy. J Clin Invest. 2023 Jun 15;133(12):e167417. doi: 10.1172/JCI167417. PMID: 37317962; PMCID: PMC10266791.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言