清华学者在《自然》发文揭示新的non-stop mRNA翻译终止机制
2016-12-06 佚名 清华大学结构生物学高精尖创新中心
2016年12月1日,清华大学生命科学学院、结构生物学高精尖创新中心高宁课题组和合作者在《Nature》在线发表题为Mechanistic insights into the alternative translation termination by ArfA and RF2的研究论文。该论文报道了大肠杆菌中non-stop mRNA在核糖体上的翻译终止状态复合物的高分辨冷冻电镜结构,并揭示了A
2016年12月1日,清华大学生命科学学院、结构生物学高精尖创新中心高宁课题组和合作者在《Nature》在线发表题为Mechanistic insights into the alternative translation termination by ArfA and RF2的研究论文。该论文报道了大肠杆菌中non-stop mRNA在核糖体上的翻译终止状态复合物的高分辨冷冻电镜结构,并揭示了ArfA在non-stop mRNA翻译终止过程中的作用机制。
核糖体上的蛋白翻译是一个非常复杂的过程,包括翻译起始、延伸和终止等多步严密调控的步骤。在细菌中,当蛋白翻译进行到mRNA上的终止密码子时,翻译终止因子RF1或RF2可以直接识别终止密码子,结合到核糖体上的活性中心,催化释放共价偶联在肽酰tRNA 3’末端上的新生肽链,这个过程受RF1/RF2上保守的催化活性基序Gly-Gly-Gln(GGQ)序列的调控。在细胞中,由于转录提前终止、mRNA错误加工、药物或者物理损伤等会导致细胞中产生缺少终止密码子的mRNA,这类mRNA被称为non-stop mRNA。当核糖体移动到non-stop mRNA的3’末端时,由于缺少终止密码子对RF1/RF2的激活作用,核糖体会停滞在mRNA的3’末端并且不能够进行正常的翻译终止。细胞中积累过多停滞的核糖体会产生毒性,真核生物和原核生物都进化出了相应的质量控制体系来回收这些核糖体。在细菌中,一类针对non-stop mRNA的挽救系统依赖于一种小蛋白ArfA(alternative ribosome rescue factor A)。现有的少量遗传和生化数据表明,当核糖体停滞在non-stop mRNA的3’末端时,ArfA结合到核糖体上的解码活性中心,招募并激活RF2的肽酰水解活性,从而释放新生肽链。然而,众多机制相关的问题尚不清楚,例如ArfA是如何激活RF2的水解功能?ArfA如何区分不同长度mRNA结合的核糖体?
高宁课题组在体外组装了ArfA/RF2、non-stop mRNA、tRNA与70S核糖体的复合物,并获得了该复合物的高分辨冷冻电镜结构(3埃分辨率,核心区域接近2.6埃)。结构表明ArfA C端的loop结合于核糖体30S小亚基上的mRNA进入通道,并部分地占据了终止密码子的结合位点,而N端则直接与30S解码中心及RF2相互作用。进一步的分析表明ArfA扮演了两个重要的角色:其N端作为mRNA长度的感受器(Sensor),如果核糖体尚未行进到mRNA的3’末端,mRNA进入通道内的核苷酸会阻碍ArfA的结合;其C端则通过和RF2直接结合,从功能上补偿了终止密码子对RF2的激活效应。
这项研究展示了自然界的一种奇妙的功能模拟机制:具有极大结构柔性的小蛋白可以通过结构模拟来取代mRNA上的三碱基终止密码子的功能。值得一提的是,在这项工作发表的同一天,Nature和Science同时在线发表了来自德国(慕尼黑大学Wilson实验室)和英国(MRC Ramakrishnan实验室,2009 Nobel化学奖)科学家的相似的工作。
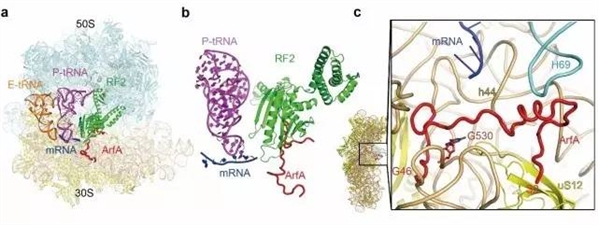
图:ArfA在核糖体上的结合位点
高宁研究组的博士生马成英和日本弘前大学(Hirosaki University)的Daisuke Kurita博士为该论文的共同第一作者。高宁和Hyouta Himeno教授为共同通讯作者。高宁研究组成员李宁宁和陈燕也参与了本课题的研究。冷冻电镜数据采集得到了国家蛋白质科学设施(北京)的清华大学冷冻电镜平台支持,数据处理得到国家蛋白质科学设施(北京)清华大学高性能计算平台的支持。部分计算处理也得到了了北京大学生命联合中心高性能计算平台的支持。本工作获得清华大学结构生物学高精尖创新中心、教育部蛋白质科学重点实验室、科技部重大科学研究计划专项、国家自然科学基金委等的经费支持。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









感谢分享一下!
60
#清华#
26