编者按:以匠心,敬初心。本期组稿由天津医科大学肿瘤医院张真发教授担任执行主编,特邀肺癌外科领域专家进行学术观点分享,共计4期,以供交流。
目前的肺癌外科,大部分是小结节的患者,对于小结节的手术方式,虽然有争议,但肺段/亚段切除以及楔形切除,必然有其适应症,也在临床中广泛应用。我们5年前提出“动脉先行-以动脉为核心的解剖性肺段切除”,随着时间的推移,我们觉得对于肺段切除的意义很大,可以使肺段切除变得更简单、准确。除了小结节,围手术期的治疗也是近年来的热点。辅助靶向治疗目前已有两项多中心临床研究证明能够延长总生存;而围手术期的免疫治疗,尽管有很多问题目前仍然弄不清楚,但是也给很多患者带来较大获益,正在获得大量的临床应用。
肺癌是我国发病率和死亡率最高的癌症,其中85%是非小细胞肺癌( NSCLC),约1/3诊断时为早期( I-IIIA期)。对于早期I-IIIA期患者,手术仍是其基础方案,然而术后仍存在复发或转移的风险,针对II-IIIA期和具有高风险的IB期患者进行术前新辅助或术后辅助治疗,是预防疾病复发的手段之一。
目前围手术期常见的治疗方式包括化疗、放疗等。虽然LACE荟萃分析结果确立了辅助化疗的地位,但NSCLC术后全身辅助化疗疗效有限,5年OS仅提高了5.3%。而根据Lung- ART研究结果显示,NSCLC术后全身辅助放疗DFS无显著获益,使辅助放疗疗效产生争议。在如今的精准治疗时代下,靶向辅助治疗提供了肺癌围术期治疗的全新视角。
1 术后辅助靶向治疗,为手术锦上添花
非小细胞肺癌治疗中EGFR突变阳性的NSCLC细胞靶向治疗效果显著,尤其是三代EGFR-TKIs在一线/后线和术后辅助治疗中扮演着重要角色。EGFR突变在亚裔人群中突变率高达40~50%,显著改变了肺癌的临床实践。
BR19研究开启了靶向辅助治疗的早期探索,但因试验设计中并未进行对EGFR敏感突变患者的精准选择,因此其研究结果显示,在未经选择的人群中,使用吉非替尼辅助治疗并未得到OS和DFS改善。
RADIANT研究首次进行了标志物的筛选,但因当时对EGFR-TKI获益人群认知的局限性,虽然最终结果为阴性,但也发现在 EGFR突变患者中使用TKI呈现获益趋势,靶向辅助治疗初见曙光。
此后,SELECT研究开始精准选择EGFR敏感突变患者,研究结果显示,厄洛替尼辅助治疗2年DFS率为88%,并且在停药后复发的患者中厄洛替尼仍然有效。
ADJUVANT研究是首个报道OS结果的II期随机临床试验,研究显示,对比化疗辅助治疗组,吉非替尼可显著延长患者DFS达10.7个月。但是,3年左右DFS曲线出现明显汇合,这可能与药物规定治疗时间仅为2年有关,提示部分患者需要延长治疗时间,否则可能会出现复发。然而,2020 ASCO会议上公布的OS数据显示两组没有显著差异,这可能与样本量计算以及后续治疗有关。
EVIDENCE研究是国内首个NSCLC术后辅助治疗领域的注册临床研究,对比了埃克替尼与化疗在Ⅱ-ⅢA期伴EGFR突变NSCLC完全切除术后辅助治疗的疗效和安全性,结果显示,埃克替尼组中位DFS为47.0个月,化疗组中位DFS为22.1个月(HR=0.36),两组3年DFS率分别为63.9%和32.5%;安全性方面,埃克替尼组不良反应发生率明显低于化疗组。这提示,埃克替尼用于EGFR敏感突变的NSCLC患者术后辅助治疗的疗效明显优于标准辅助化疗,且安全性更优。但该研究的OS尚未成熟,仍需等待更多研究结果。
EVAN研究是我中心牵头完成的一项多中心临床研究,也是第一个获得OS获益的辅助靶向研究,纳入完全切除(R0)术后的ⅢA期EGFR突变NSCLC患者,1:1随机分组,术后予以厄洛替尼对比VP化疗,结果显示,与化疗相比,厄洛替尼提高了2年DFS率(81.4% vs 44.6%,P=0.0054),并改善患者的OS(84.2个月 vs 61.1个月,HR=0.318)和5年OS率(84.8% vs 51.1%),为患者带来了明显的生存延长。但该研究也存在一定局限性,仅为Ⅱ期研究,且仅覆盖ⅢA期NSCLC患者,未来可能需要纳入更多分期患者,开展更大型Ⅲ期临床研究继续探索。
ADAURA研究最新的研究结果在2023年ASCO会议上公布,奥希替尼辅助治疗与安慰剂相比,对已切除的EGFRm IB-IIIA期的NSCLC治疗具有统计学意义和临床意义上的DFS改善,IB期、II期和IIIA期患者中,无论既往是否使用辅助化疗,后续使用奥希替尼辅助治疗均有显著DFS获益,提示了相比辅助化疗,靶向辅助治疗的价值。并且,从各分期患者DFS曲线可知,随着分期的增加,生存获益也增加。因此,提示复发风险越高的人群越需要加以靶向药物,进行更为强化的治疗。同时还改善中枢神经系统转移患者的DFS且安全性可耐受。
ADAURA中的DFS获益已转化为奥希替尼辅助治疗对比安慰剂在统计学意义上的OS获益:在主要人群(II-IIA期)中:OS HR 0.49;95.03% CI 0.33,0.73;P=0.0004。总人群(IB-IIIA期)中:OS HR 0.49:95.03% CI 0.34,0.70;P<0.0001。奥希替尼辅助治疗对比安慰剂的OS获益在各亚组中基本一致,包括按疾病分期(IB/II/IIIA)与辅助化疗史(是/否)亚组。
ADAURA是全球首个证实在完全切除术后EGFRmIB-IIIA期NSCLC中采用靶向治疗获得具有统计学意义和显著临床改善OS获益的III期研究,夯实了奥希替尼辅助治疗作为这类患者治疗标准的地位。
2 术前新辅助靶向治疗,初见曙光,未来可期
与术后辅助治疗相比,新辅助治疗主要在术前进行,除消除微转移病灶外,还可达到缩小肿瘤、增加手术切除可能性等目的,从而提高患者生存。术前新辅助化疗可降低疾病复发和远处转移风险,将早期可手术NSCLC患者的5年生存率绝对值提高约5%。即便如此,早期NSCLC患者的5年生存率也只提高到了45%,仍有较大提升空间。
随着三代EGFR-TKI的蓬勃发展,NSCLC的治疗格局也在不断改变,但新机遇中也同时面临许多新挑战。荟萃分析显示新辅助化疗可使患者有一定的获益,但这种方案具有明显的局限性包括与辅助化疗类似的无病生存及其毒性可能影响手术切除。围术期靶向治疗在EGFR突变患者中无论是疗效,还是安全性,相比新辅助化疗均显示出较好的临床趋势,亦成为我们临床讨论的焦点,但迄今为止EGFR-TKIs用于NSCLC的围术期治疗的有效性和安全性尚不明确。
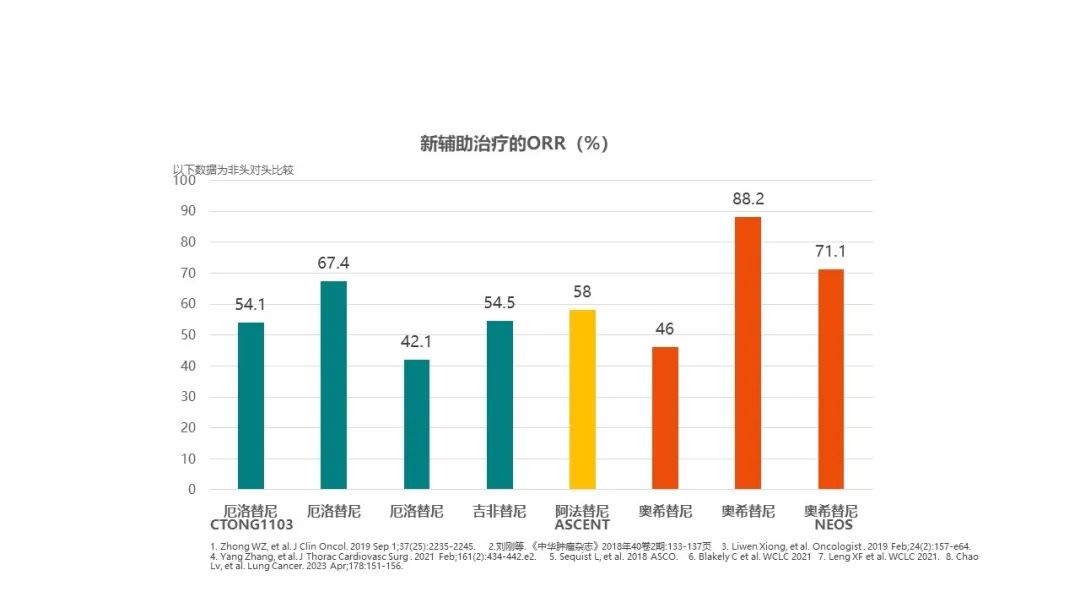
CTONG 1103试验是一项多中心开放、II期随机对照试验,研究厄洛替尼与吉西他滨加顺铂(GC化疗)作为新辅助/辅助治疗IIIA-N2期第19或21外显子EGFR突变非小细胞肺癌患者的疗效。结果表明,研究结果显示:厄洛替尼组和化疗组的主要终点ORR分别为54.1%和34.3%,从数值上来看,靶向治疗组ORR高于化疗组,但P值没有统计学意义(P=0.092)。厄洛替尼组有9.7%患者达到了MPR(主要病理缓解),而化疗组无人达到。同时,厄洛替尼组的中位PFS显著长于化疗组,降低了61%的进展或死亡风险(21.5 vs 11.4个月,HR 0.39,95%Cl 0.23-0.67,P<0.001)。
三项一/二代EGFR TKI新辅助治疗的小样本研究(NCT01217619,NCT01833572, NCT01553942)报道了和CTONG1103研究相似的ORR率,为42.1~69%。
奥希替尼用于II-IIIB期EGFR突变可切除肺腺癌新辅助治疗的NEOS研究。研究显示,奥希替尼新辅助治疗的客观缓解率(ORR)达71.1%,R0切除率达94%,46%的患者病理缓解≥50%,并且安全性与既往奥希替尼研究结果一致。作为三代EGFR-TKI作为新辅助治疗取得了更好的疗效,实现了在较短的时间内使肿瘤缩小,以提高手术完全切除率,最终有望改善患者长期生存。该研究中,32例患者接受了手术,其中50%为胸腔镜/机器人辅助胸腔镜手术,50%为开胸手术;94%(30例)手术患者实现了R0切除。而以往一二代EGFR-TKI新辅助治疗后的R0切除率约为60%-80%。
目前开展的NeoADAURA研究,旨在评估奥希替尼新辅助治疗EGFRm可切除的II-IIIB N2期 NSCLC患者的疗效与安全性,该研究首次采用MPR作为主要研究终点,或可为后续围手术期研究设计提供参考。
一项三代TKI新辅助治疗研究(ANSWER研究),是阿美替尼对比标准化疗或厄洛替尼新辅助治疗IIA期EGFR突变NSCLC的研究,在一定程度上可以解答三代TKI与一代 TKI之间的对比问题,填补该研究领域的空白。
我中心也牵头开展了“甲磺酸伏美替尼用于可切除的 IIIA-IIIB 期( N1-N2) EGFR 突变肺腺癌围手术期治疗的开放标签,单臂 II 期临床研究”(FRONT研究),初步结果表明,三代EGFR-TKI新辅助治疗效果好,不良反应轻,缩瘤率高。结果有待进一步公布。
3 ALK阳性新辅助靶向相关研究
一项小样本量的回顾性研究评估了ALK融合的N2期NSCLC患者术前接受克唑替尼(Crizotinib)的疗效。结果表明:ORR高达91.0%,18.2%达到完全缓解(pCR),27.3%在克唑替尼新辅助治疗后实现N降期。证明新辅助克唑替尼对局部晚期疾病的完全切除可能是可行的,且耐受性良好。但还需大规模的前瞻性试验证明其在新辅助治疗中的有效性。
一项多中心、单臂、Ⅱ期SAKULA临床试验,评估了塞瑞替尼(Ceritinib)作为术前新辅助治疗药物治疗可切除ALK阳性局部晚期(LA)NSCLC的疗效及安全性。结果显示:主要病理反应率(MPR)达57%,2例(29%)患者实现完全缓解。塞瑞替尼用于新辅助治疗存在一定临床获益。
一项Ⅱ期伞状NAUTIKA1研究(NCT04302025)旨在探索(Alectinib)阿来替尼用于Ⅱ-Ⅲ期ALK+可切除NSCLC患者的新辅助和辅助治疗的有效性和安全性。NAUTIKA1研究公布新辅助治疗中ALK+队列的初步数据。共8例ALK阳性患者纳入研究,其中5例完成阿来替尼新辅助治疗。所有患者均在窗口期内(第57天±10天)完成手术,手术达到R0切除(R0切除率:100%),无延误或严重手术并发症。在ALK+队列的初步分析中,阿来替尼在Ⅱ-Ⅲ期ALK+ NSCLC患者中的耐受良好,是新辅助治疗的可行方案。
4 小结
NSCLC是一种分子水平上异质性的疾病,随着精准医学的发展,靶向治疗逐步成为有靶点患者的优选方案,成为驱动基因阳性患者新辅助治疗的研究探索方向。虽然围术期靶向治疗并未常规推荐,但大量临床试验已显示出较好的疗效:对于EGFR突变人群,尤其是中国人群的高突变率,无论是疗效,还是安全性,围术期靶向治疗相比新辅助化疗都更具优势,将为EGFR突变NSCLC围术期治疗提供更多治疗选择,带来新的获益。但仍有很多问题值得进一步研究,比如TKI用药疗程?总生存是否有获益?若存在突变基因共存用药方案如何选择?TKI联合化疗或放疗能否取得更大疗效等等?期待有更多Ⅲ期临床研究以获得更高级别证据。
此外,ALK是晚期NSCLC的重要治疗靶点,已然是围术期治疗研究热点。ALK-TKI进军早期NSCLC已呈势不可挡之势,期待更多试验数据或真实世界数据验证的出炉,为早期ALK患者的临床应用提供更多的证据。对于外科医生而言,我们也关注了一些问题,比如部分患者术中出现了较为严重的粘连,血管鞘膜无法分离,增加手术难度及中转开胸的可能及出血的风险。术前靶向药物停药时间的选择,手术时间窗的把握都没有一个定论,这都是围术期靶向治疗需要关注和解决的问题。
主编评语
随着ADAURA研究结果最新公布,以及天津肿瘤医院EVEN研究的发表,越来越多的研究证明辅助靶向治疗对II-IIIA肺癌患者可以做到OS的延长。肺癌的辅助靶向治疗越来越多的获得了关注和肯定。而新辅助靶向治疗,尽管还没有研究获得OS的延长,但是一些三代药物的临床试验正在进行中,我们也期待有好的结果。不过,新辅助靶向治疗对手术难度的影响,也是外科医生关注的问题。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言