读书报告 | TITAN-TCC研究:含铂化疗后进展的尿路上皮癌患者接受定制的纳武利尤单抗联合伊匹木单抗免疫治疗的II期临床试验
2024-01-01 iCombo iCombo 发表于上海
本研究目的是探索纳武利尤单抗诱导和大剂量伊匹单抗作为转移性尿路上皮癌患者的二线治疗手段的安全性和活性。
导读
背景:纳武利尤单抗可用于接受过铂类化疗的转移性尿路上皮癌患者。既往研究表明,高剂量的伊匹木单抗可提高双免疫检查点抑制的疗效。本研究目的是探索纳武利尤单抗诱导和大剂量伊匹单抗作为转移性尿路上皮癌患者的二线治疗手段的安全性和活性。
方法:TITAN-TCC研究是一项多中心、单臂、II期临床试验。研究主要纳入的是18岁及以上经组织学证实为膀胱、尿道、输尿道或肾盂的转移性或手术无法切除的尿路上皮癌患者。患者必须在一线铂类化疗期间或之后有进展,且同时接受最多一次二线或三线治疗。入组患者首先接受240mg纳武利尤单抗单药诱导治疗,每2周一次,共4次后,疗效评估为部分缓解或完全缓解的患者继续接受纳武利尤单抗维持治疗,而疗效评估为疾病稳定或进展的患者则接受纳武利尤单抗1mg/kg,伊匹木单抗3mg/kg联合治疗,每3周一次,共2次或4次。当接受纳武利尤单抗维持治疗的患者疾病进展后,同样采用上述联合治疗方案。研究的主要终点是经研究者评估的客观缓解率。
结果:在2019年4月8日至2021年2月15日期间共有83例符合条件的转移性尿路上皮癌患者入组,且均接受了纳武利尤单抗诱导治疗。入组患者的中位年龄为68岁,其中57例(69%)为男性,26例(31%)为女性,共有50例(60%)患者接受了至少一剂联合治疗。83例患者中有27例(33%)确认客观缓解(包括6例(7%)有完全缓解的患者),ORR高于预先设置的ORR 20%门槛。最常见的3-4级治疗相关不良事件是免疫介导的小肠结肠炎(9例,11%)和腹泻(5例,6%)。报告了2例(2%)与治疗相关的死亡病例,死因均为免疫介导的小肠结肠炎。
结论:TITAN-TCC的研究结果表明,接受过铂类化疗的转移性尿路上皮癌患者接受纳武单抗单药诱导治疗后,早期无反应者或后期进展患者接受纳武利尤单抗1mg/kg联合伊匹木单抗3mg/kg治疗,可以有效提高ORR(Lancet Oncol.2023 Feb 28; S1470-2045(23)00053-0. doi: 10.1016/S1470-2045(23)00053-0)。
研究背景及目的
研究背景
纳武利尤单抗已经获批用于接受过铂类化疗后局晚期/转移性尿路上皮癌患者的二线治疗。
CheckMate-275:纳武利尤单抗二线单药治疗接受过铂类化疗后转移性尿路上皮癌患者,其ORR可达20.7%。
既往研究显示,在部分黑色素瘤患者和肾细胞癌患者中,双免疫检查点抑制剂显示出比单免疫检查点抑制剂更好的疗效。
CheckMate-032:双免疫检查点抑制剂治疗尤其是伊匹木单抗剂量较高时(nivo 1mg/kg + ipi 3mg/kg)可改善转移性尿路上皮癌患者生存,其ORR可达38% 。
2022年3月,TITAN-TCC试验部分结果(队列1)发表于J Clin Oncol,证实了纳武利尤单抗联合伊匹木单抗一线治疗晚期尿路移行上皮细胞癌的有效性和安全性。
研究目的
探索纳武利尤单抗联合伊匹木单抗用于转移性尿路上皮癌二线治疗的疗效和安全性(队列2)。
研究方法
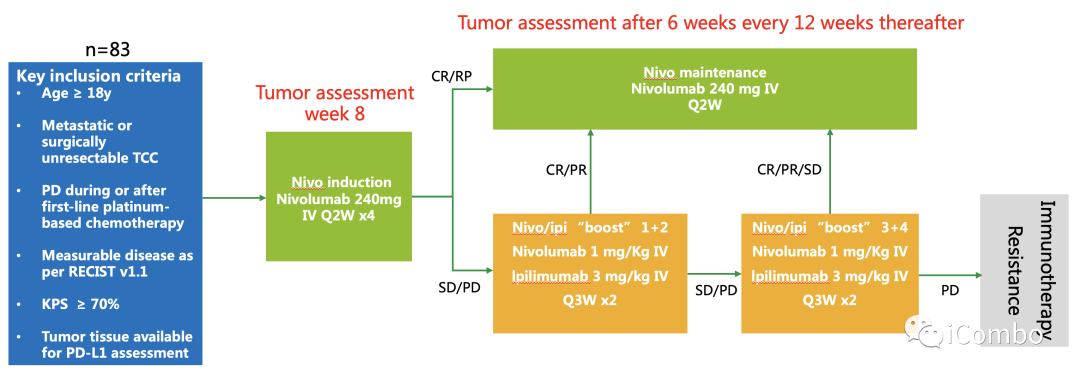
Primary endpoints: ORR
Key secondary endpoints: RR,PFS, OS, safety (trAE)
研究假设
相对于纳武利尤单抗单药治疗,本临床试验中“定制”的治疗方案将提高接受过含铂化疗后的转移性尿路上皮癌患者的ORR(相较于CheckMate-275 和CheckMate-032研究中的ORR)。
患者基线特征
研究共纳入83例转移性尿路上皮癌患者,所有患者均接受纳武利尤单抗诱导治疗(意向治疗人群)。50例患者(60%)接受至少1剂纳武利尤单抗联合伊匹木单抗治疗。
患者中位年龄为68岁,57例男性,26例女性。
对意向治疗人群的中位随访时间为5.6个月,对数据截止时仍存活患者中位随访时间为13.9个月。
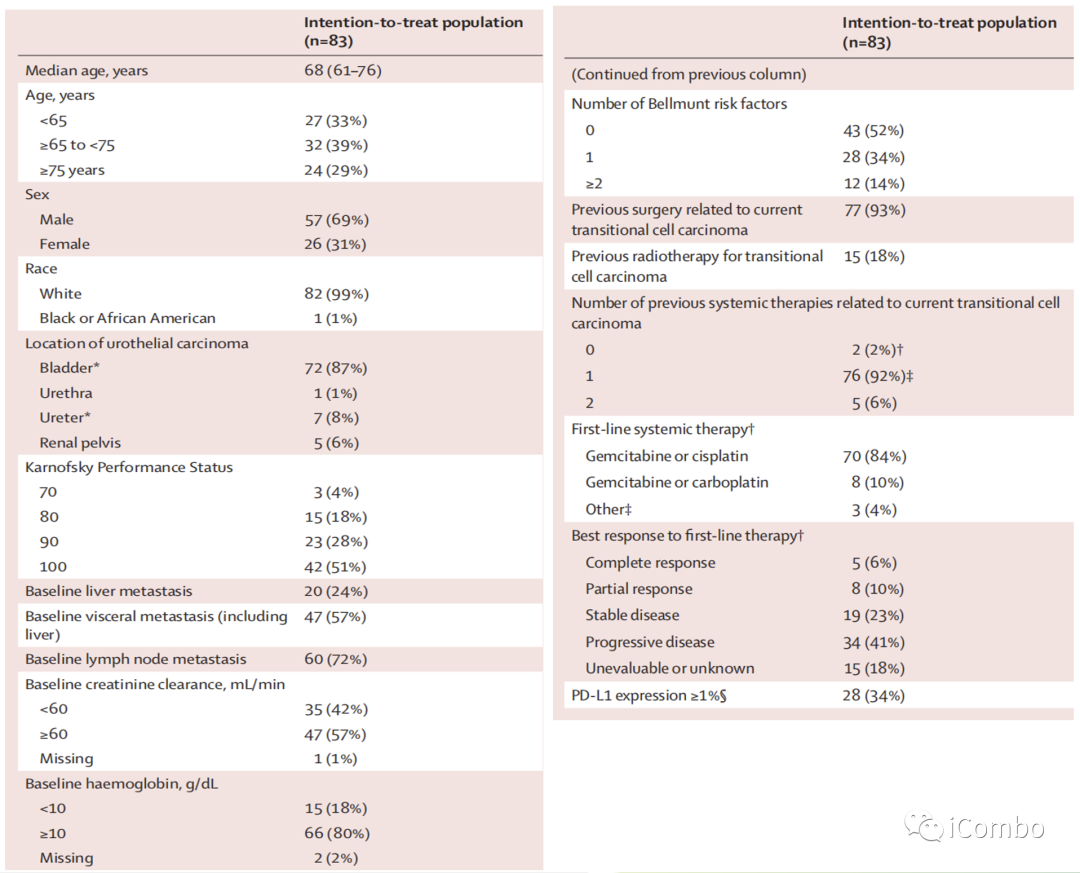
研究结果
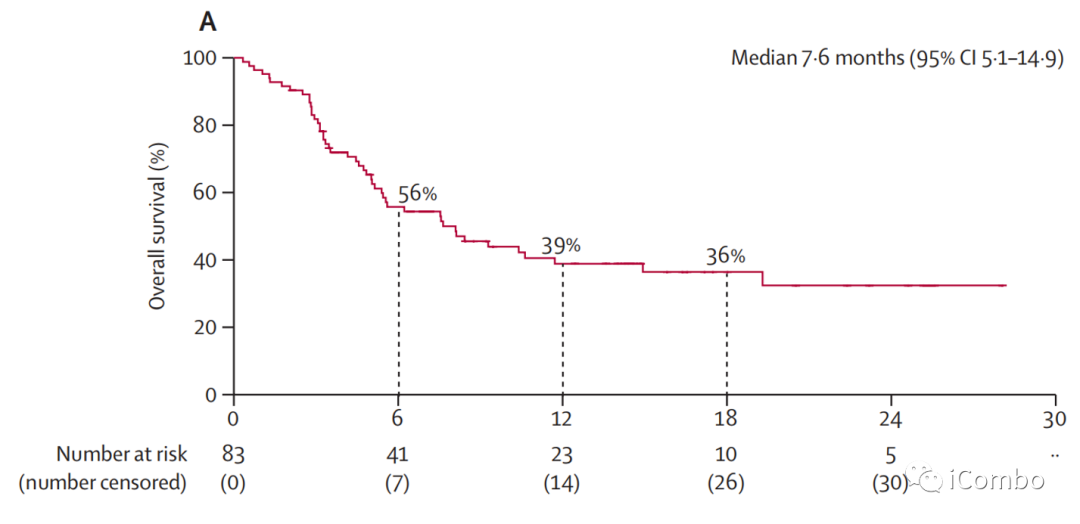
数据截止时,48例(58%)患者死亡,中位OS为7.6个月(95%CI,5.1~14.9)
6个月OS率为56%(95%CI,44~66)
12个月OS率为39%(28~50)
18个月OS率为36%( 95%CI, 25~48)
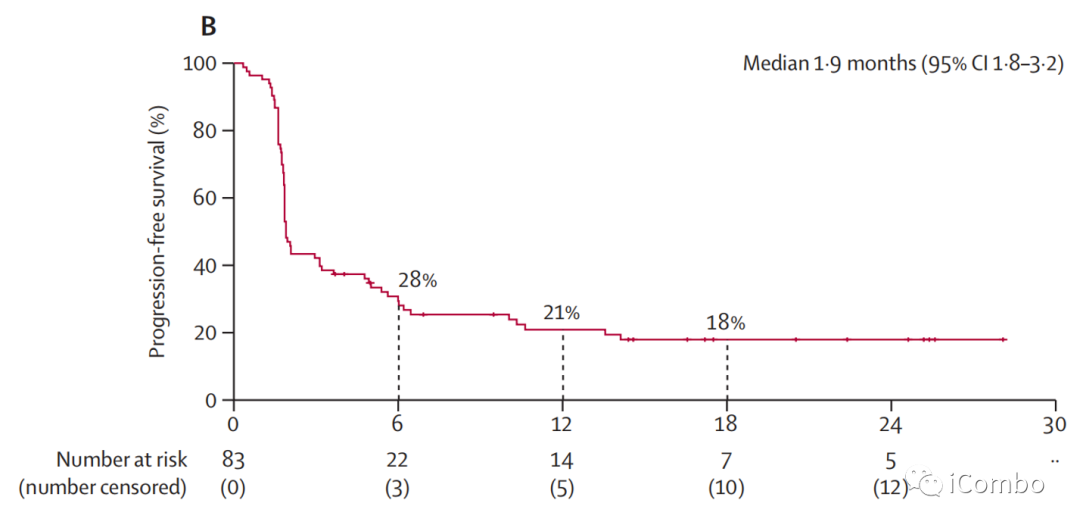
数据截止时,83例患者中有66例(80%)发生了疾病进展或死亡。其中位PFS为1.9个月(1.8~3.2个月)
6个月PFS率为28% (95%CI,19~38)
12个月时PFS率为21%( 95%CI,13~31)
18个月时PFS率为18%( 95%CI,10~27)
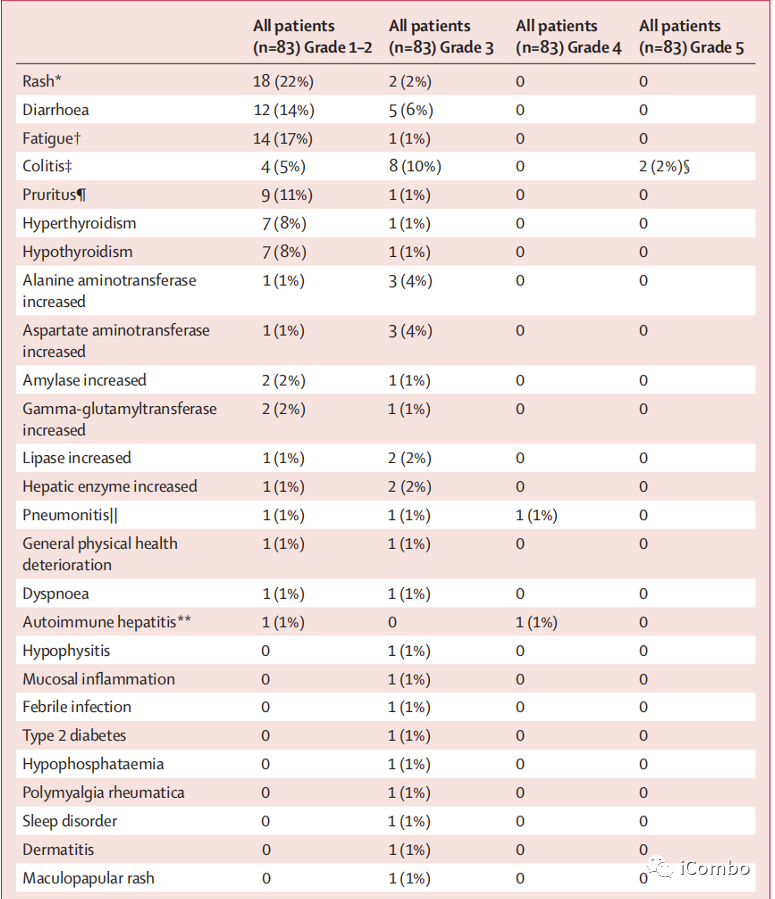
任何级别中最常见的治疗相关不良事件是全身皮疹、腹泻、疲劳或虚弱、结肠炎、免疫介导的肠炎 和全身瘙痒。
最常见的3-4级治疗相关不良事件是免疫介导的结肠炎和腹泻。
讨论
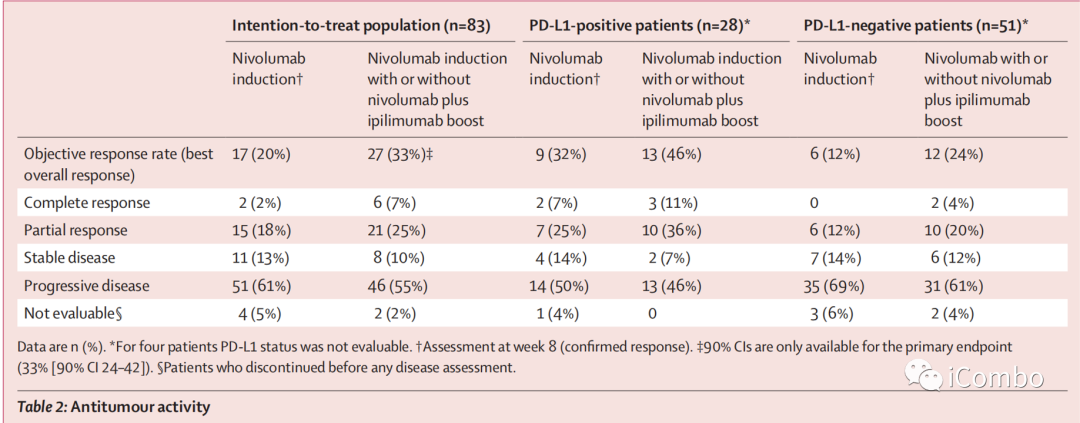
在TITAN-TCC研究中显示在意向治疗人群中的ORR为33%,在PD-L1阳性患者中ORR为46%,而在CheckMate-275中报道的相关ORR则分别为20.7%和24%,提示这种定制的免疫疗法显示出良好的临床活性。
在TITAN-TCC中,所有患者接受纳武利尤单抗单药诱导治疗后的ORR为20%,与其他研究报道的基本一致(ORR:13%~21%)。
DANUBE ,一项针对转移性尿路上皮癌的III期临床试验结果也证实,双免联合治疗( tremelimumab+ durvalumab )比单免( durvalumab )有着更高的ORR(36% vs 26%),并且与TITAN-TCC结果类似,PD-L1阳性亚组的患者似乎通过双免联合治疗获益更大(ORR:47%)。
CheckMate-032研究显示,nivo 1mg/kg + ipi 3mg/kg 较nivo 3mg/kg + ipi 1mg/kg有着更高的ORR,这在TITAN-TCC cohort1中也得到了验证。然而,较高的伊匹木单抗剂量同时也导致了更多与治疗相关的3-4级不良事件的发生。
尽管ORR有所提高,但与CheckMate-032和CheckMate-275研究相比,患者的OS和PFS却无明显改善。
结论
与CheckMate-275的报道的纳武利尤单抗作为二线单药治疗的研究结果相比,纳武利尤单抗诱导后接受 1mg/kg纳武利尤单抗+3mg/kg伊匹木单抗治疗显著提高了含铂化疗后转移性尿路上皮癌患者的ORR,并且,PD-L1 阳性肿瘤患者似乎从中获益更多。尽管其长期结果仍需进一步随访,但本研究为高剂量伊匹木单抗(3mg/kg)在转移性尿路上皮癌患者中的潜在应用价值提供了研究证据,并且为在现有疗法的背景下构建双免疫疗法奠定了基础。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#伊匹单抗# #转移性尿路上皮癌# #纳武利尤单抗#
26