2023 ESMO|李茵茵教授:小细胞肺癌免疫治疗进展
2023-12-28 医悦汇 医悦汇 发表于上海
本期,【医悦汇】特邀沈阳市肺癌临床诊治中心李茵茵教授分享小细胞肺癌免疫治疗进展,以供交流。
编者按:2023年ESMO年会有颇多肺癌相关研究成果展出,包括肺癌的免疫联合治疗以及基于多组学的治疗疗效预测等重要议题。本期,【医悦汇】特邀沈阳市肺癌临床诊治中心李茵茵教授分享小细胞肺癌免疫治疗进展,以供交流。
正文如下
1 EXTENTORCH 研究:特瑞普利单抗对比安慰剂,联合化疗一线治疗广泛期小细胞肺癌
EXTENTORCH 研究是一项随机、双盲、安慰剂对照、多中心、III 期临床研究,在全国 48 家中心纳入 442 例经组织学或细胞学证实为广泛期小细胞肺癌(ES-SCLC)、既往未接受过全身系统治疗、ECOG 评分为 0 或 1、且根据 RECIST v1.1 标准至少存在一个可测量肿瘤病灶的患者。根据性别、ECOG-PS 评分作为分层因素,患者以 1:1 比例随机接受特瑞普利单抗(n = 223)或安慰剂(n = 219)联合依托泊苷及铂类方案诱导治疗 4-6 个周期,此后受试者继续接受特瑞普利单抗或安慰剂维持治疗,直至疾病进展或出现无法耐受的不良反应。研究的主要终点为研究者评估的PFS(RECIST v1.1)和OS;次要终点为盲化独立评审的PFS, ORR, DCR, DoR (缓解持续时间),TTR (至缓解时间)和安全性。
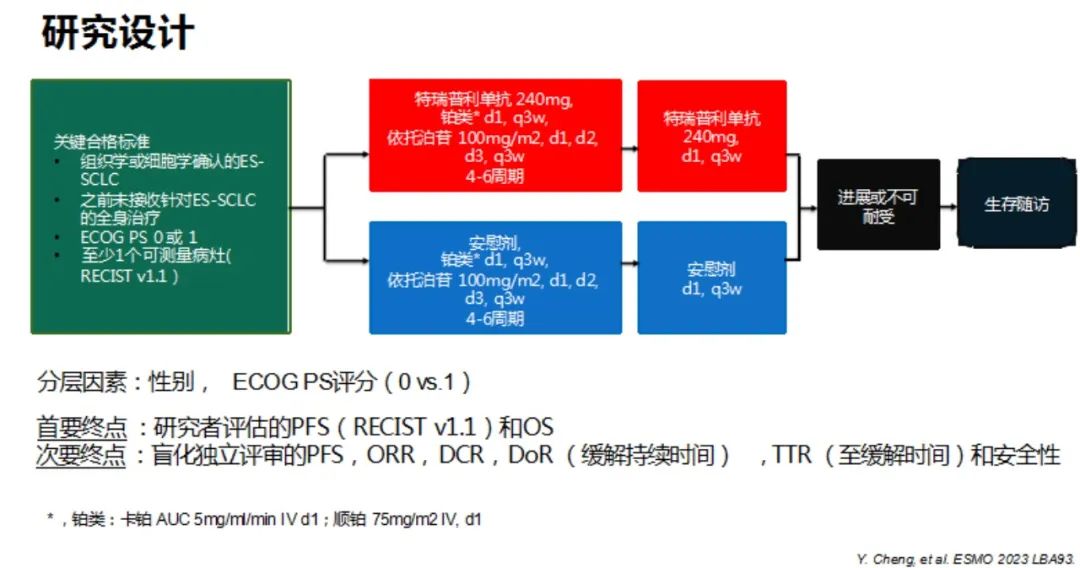
研究结果显示:ES-SCLC一线化疗基础上,联合特瑞普利单抗对比安慰剂, 提供了显著更好的临床结局:中位PFS:5.8 vs. 5.6 个月,HR=0.667(95%CI:0.539 ,0.824), p=0.0002;中位OS:14.6 vs. 13.3 个月,HR=0.798(95%CI:0.648 ,0.982),p=0.0327。全外显子测序结果提示PFS和OS的改善在不同TMB状态间相似。整合素介导黏着斑复合物的基因组改变与特瑞普利单抗组更差的PFS和OS预后相关。特瑞普利单抗联合化疗整体耐受性可, 安全谱与各单药一致,应该作为ES-SCLC一线标准治疗。我们医院作为分中心也参与了本项研究,目前仍有受试者处在生存随访阶段,取得临床获益。


2 GOIRC-01-2019 CeLEBrATE ML41241研究:卡铂依托泊苷贝伐珠单抗联合阿替利珠单抗治疗广泛期小细胞肺癌
这是一项由GOIRC申办罗氏支持的研究者发起的II期单臂研究。共纳入53名患者接受卡铂(AUC 5),依托泊苷(100 mg/m2),贝伐珠单抗(7.5 mg/kg),联合阿替利珠 单抗(1200mg)诱导治疗4-6个周期,随后予以贝伐珠单抗联合阿替利珠单抗维持治疗,一线治疗每3周最多总计18个周期。主要研究终点:1-年生存率,次要研究终点:ORR,PFS和安全性。

研究结果显示:中位随访19.1个月后,中位OS为12.7个月(95%CI:11.6-16.1),1年OS率为61.8%(90%CI:50.7-72.8),p=0.04;ORR为67.9% (95%CI:53.7-80.1), PFS为6.2个月(95%CI:5.1-6.6),在安全性方面,报告的不良事件中共发生16例SAE,包括中性粒细胞减少症(n=4),发热性粒缺(n=3)和肺栓塞(n=3)。
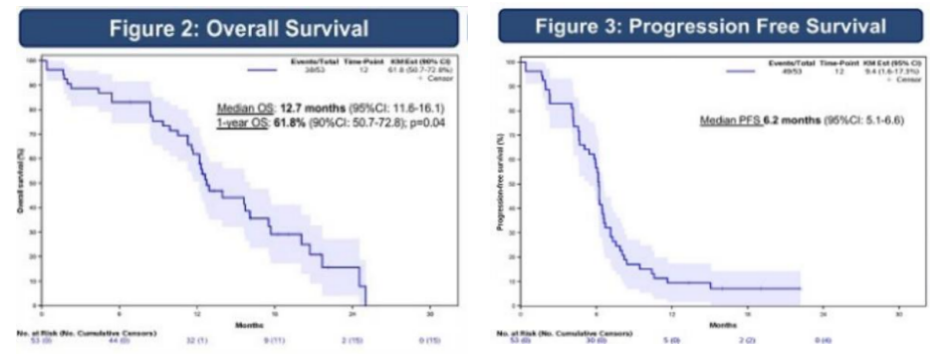
结论:阿替利珠单抗、依托泊苷卡铂联合贝伐珠单抗治疗ES-SCLC患者总体耐受性好且方案可行。该研究达到其主要研究终点,提示在标准免疫化疗治疗模式上增加贝伐珠单抗可改善OS,但该结果需要此联合方案的进一步研究证实。
3 一项多中心回顾研究:广泛期小细胞肺癌一线免疫治疗后胸部放疗的有效性和安全性
在过去几年中,免疫治疗联合化疗已成为广泛期小细胞肺癌(ES-SCLC)的标准一线治疗选择。然而,患者在一线免疫治疗后是否能从巩固性胸部放疗(TRT)中获益仍未确定。本研究纳入了2020年2月至2022年12月期间在中国3家癌症中心接受标准一线免疫联合化疗加/ 不加后续TRT的ES-SCLC患者,评价了其临床结局以及安全性。共有258例ES-SCLC患者符合分析条件, 其中158例在化疗后接受了TRT和维持免疫治疗 , 100例仅接受维持免疫治疗。研究结果显示:TRT显著改善了PFS(10.7mVS.8.4m),并降低了胸内病变进展率(8.86%与38.00%),但TRT未带来OS的获益。
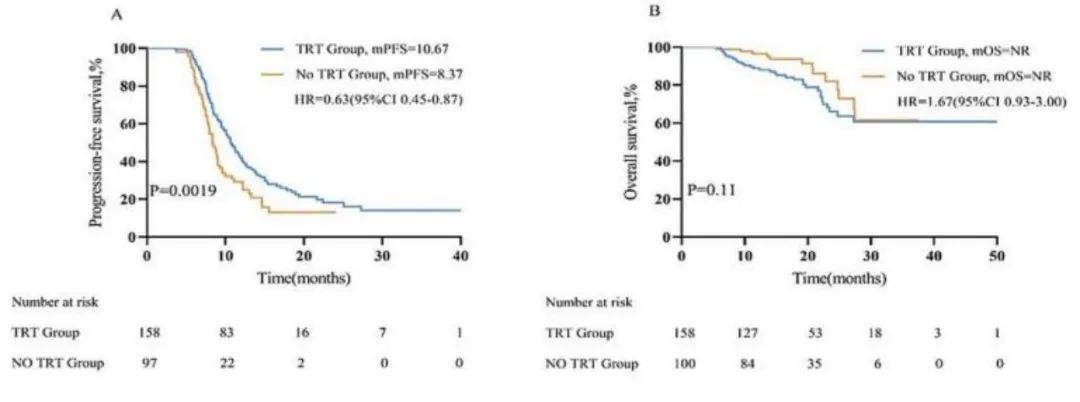
进一步分析显示:不同剂量或剂量分割模式的TRT未影响PFS的获益;化疗后3-6周内添加TRT产生的PFS显著优于一线治疗 肿瘤进展后再添加TRT(mPFS 10.9m VS 8.3m, HR = 0.36 [95%CI:0.13-1.00], p = 0.00);无肝转 移的患者更有可能从TRT中获益(p < 0.01);TRT轻度增加≥3级不良反应(33.54%VS 24.00%)。值得注意的是TRT组肺炎发生率高于维持免疫治疗组(23.42%VS 8.00%)。
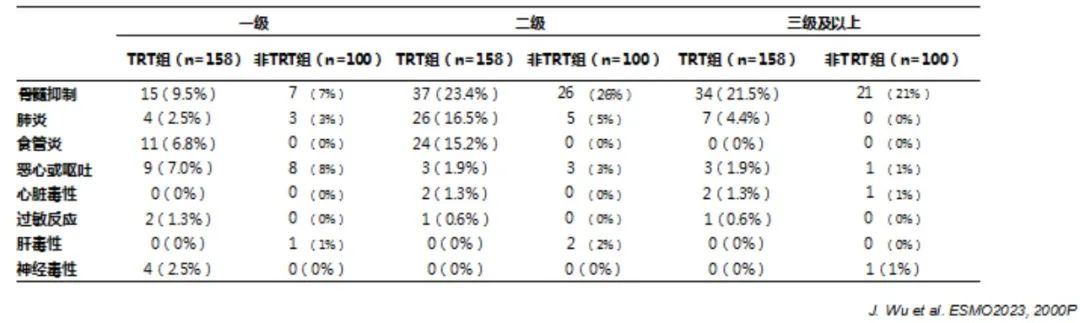
结论:一线免疫治疗后加用TRT尽管不能改善患者的OS,但可改善ES-SCLC患者的PFS和局部控;TRT应在化疗后3-6周进行;无肝转移的患者从TRT中获益更多;除肺炎发生率增加外,TRT的应用通常是安全的。
4 意大利南部一项回顾性研究:一线免疫联合化疗时代广泛期小细胞肺癌的巩固性胸部放射治疗
过去几年中 ,胸部巩固放疗常用于广泛期小细胞肺癌(ES-SCLC) ,但在一线免疫联合化疗的III 期临床试验中排除了这些治疗方法。然而 ,强有力的生物学理由支持胸部放疗来增强抗肿瘤免疫反应的持续效果。目前 ,免疫联合化疗治疗后胸部放疗的获益仍不清楚。该研究回顾性分析了自2019年以来接受免疫联合化疗治疗的120例ES-SCLC患者。纳入的所有患者在一线治疗后均无PD。其中,59例接受了胸部放疗的患者接受了多学科会诊决策。进行胸部放疗前评估了患者 特征、免疫联合化疗方案和首次放疗的时间。该研究主要终点为安全性,次要终点为OS和PFS。
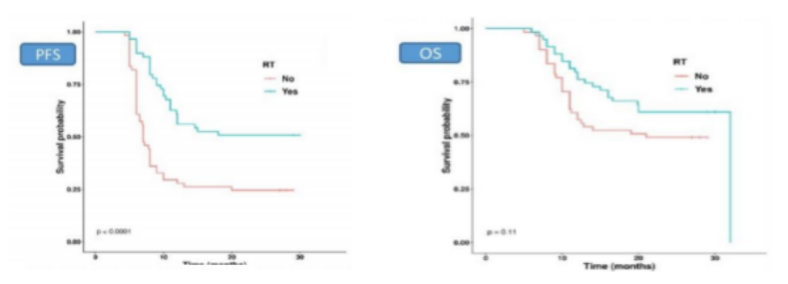
结果显示:胸部放疗具有良好的安全性特征。放疗组未报告≥3级的AE ,对照组有2例。在59名接受放疗的患者中,仅有8.47%患者发生了放射性毒性 ,其中2例为G2放射性肺炎。3例为G2放射性食管炎,未发生≥G3的放射性AEs。4个周期的免疫联合化疗治疗后,开始放疗的中位时间为62天(10-184天)。根据医生决定,19/59例患者在TR期间停止维持免疫治疗。放疗和分次范围包括30Gy(分10次) 至选定患者的确定剂量。巩固性放疗的PFS显著长于单纯全身治疗(1年PFS率62.5%vs.29.7%, p<0.0001)。但仅观察到较好OS的趋势(1年OS率81.5%vs.60.7%,p=0.11)。该多中心真实世界经验证实:基于多学科临床决策,在免疫联合化疗后使用胸部放疗作为巩固策略具有普遍价值。由于回顾性分析的局限性,结果支持这种治疗的可行性,鼓励进行前瞻性试验验证。
5 回顾性多中心分析:广泛期小细胞肺癌一线免疫维持治疗期间的巩固性胸腔内放疗
尽管最近创新疗法涌现 ,但ES-SCLC的预后仍然较差。一线化疗联合免疫治疗(CT-IT)改善了临床结局 ,且未增加毒性。相反,在很大程度上 ,胸部放疗(TRT)在这种情况下的作用是未知的。该研究目的是评价ES-SCLC患者一线CT-IT联合或不联合巩固性TRT的临床结局和安全性。研究者回顾性评价了2020年2月至2023年3月在5家意大利中心接受治疗的103例ES-SCLC患者,中位年龄为67岁,除11例PS评分为2外,所有患者的ECOG PS均为0-1,采用Kaplan-Meier法分析总生存期(OS)和无进展生存期(PFS),单因素分析探讨影响临床疗效的患者、肿瘤或治疗相关预后因子,同时根据CTCAE 4.0量表记录毒性。
结果显示:中位随访11个月时, 103例ES-SCLC患者接受了含铂化疗联合免疫治疗, 随后接受阿替利珠单抗免疫维持治疗。33例缓解患者接受了巩固性放疗,14例患者接受了颅预防性治疗。中位OS及1年和2年OS率分别为14.2个月,52.6%(SE±5.6%)和31.4%(SE±6.0%)。中位PFS 及12个月和18个月PFS率分别为7.1个月,27.5%(SE±4.8%)和14.4(SE±4.8%)。在单变量分析中,巩固性放疗、ECOG PS、诊断时无脑或骨转移是OS阳性的具有统计学意义的预后因素,放疗在OS多变量分析中仍具有显著性。23例患者(22.3%)报告毒性大于G2,最常见的是血液学毒性,仅报告了1例G5毒性(肺炎)。
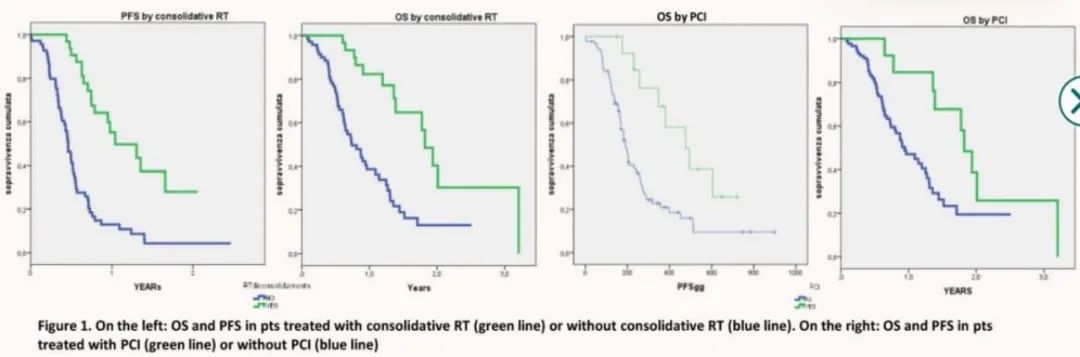
结论:免疫联合化疗被证实是ES-SCLC患者的有效治疗选择。巩固性放疗在OS和PFS显示了不错的结果 ,在大样本“真实世界”人群中也是可行和安全的。需要进行随访时间更长的前瞻性试验来进一步评估放疗对局部疾病控制和生存期的影响。
6 芦比替定联合阿替利珠单抗I/II期研究
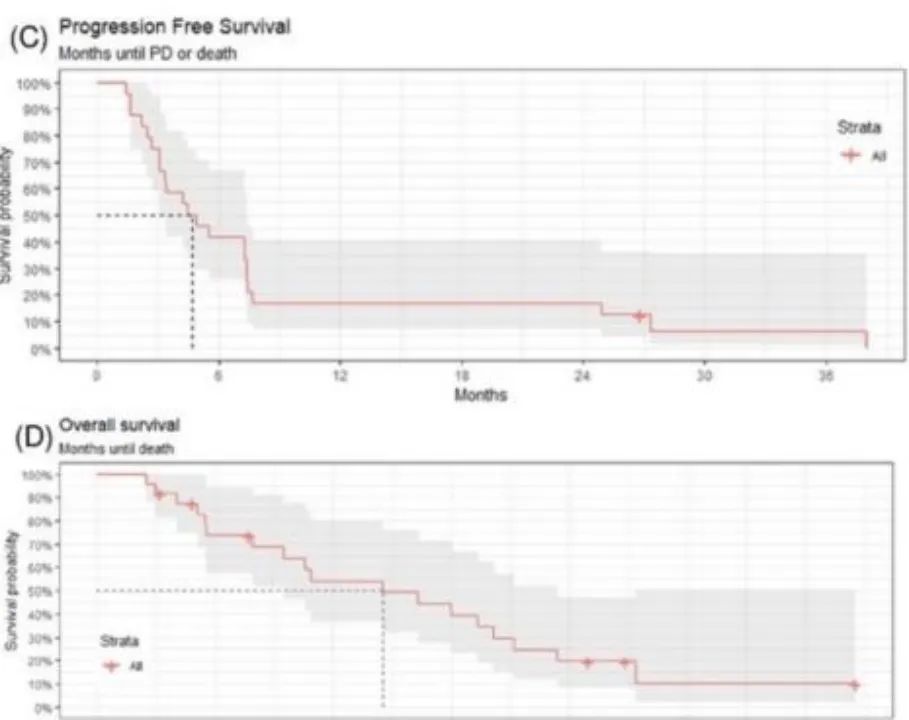
该研究旨在评估芦比替定(lurbinectedin,LUR)与阿替利珠单抗 (atezolizumab ,ATZ)联合用于广泛期SCLC二线治疗的安全性、耐受性和有效性。I/II期研究针对既往一线含铂治疗失败(不包含抗PD-1/PD-L1治疗),且不允许再挑战。其中I期:LUR剂量递增联合阿替利珠单抗固定剂量;II期:I期研究推荐剂量下的单臂研究(3.2mg/m2)。结果显示:I期:LUR与阿替利珠单抗联合治疗耐受性良好,未出现非预期毒性。LUR后续研究的推荐剂量是3.2mg/m2,第一天+ 阿替利珠单抗1200mg,第一天+粒细胞集落刺激因子。II期:抗肿瘤活性显著。ORR达到66.67%,中位PFS为4.7个月,中位OS为14.5个月。LUR与ATZ的组合具有良好的耐受性并且未出现非预期的毒性。

7 总结
免疫检查点抑制剂开启了肿瘤免疫治疗的新时代,改变了肿瘤整体肿瘤思路、诊疗模式、治疗模式和疗效评价体系。免疫治疗具有良好的毒副作用和持久的反应,在SCLC的治疗方面取得了重要突破。而免疫单药治疗的有效率相对较低,因此,联合免疫治疗和免疫联合化疗、放疗、靶向治疗,是治疗SCLC的一种新的治疗方式,通过多种协同机制达到更好的治疗效果。相信随着临床经验的不断积累,临床试验数据的不断丰富,免疫治疗必然会在不久的将来在小细胞肺癌治疗中起到越来越重要的作用。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#小细胞肺癌# #免疫治疗#
18