Mol Cancer:常熟理工学院张杰等团队合作发现肾细胞癌中血管生成的调控新机制
2023-11-23 iNature iNature 发表于上海
该研究发现ELF5通过稳定WDTC1在肾细胞癌中驱动血管生成抑制。
肾细胞癌(RCC)是泌尿系统常见的恶性肿瘤。血管生成是肿瘤发生的主要因素。E74样转录因子5 (E74-like transcription factor 5, ELF5)已被证实参与不同癌症的进展,并可调节血管生成。
2023年11月18日,常熟理工学院张杰、安徽医科大学古月及浙江中医药大学药学院Yang Yanzi共同通讯在Molecular Cancer在线发表题为“ELF5 drives angiogenesis suppression though stabilizing WDTC1 in renal cell carcinoma”的研究论文,该研究发现ELF5通过稳定WDTC1在肾细胞癌中驱动血管生成抑制。ELF5在RCC细胞和组织中低表达。高表达ELF5显著抑制RCC细胞的增殖、迁移和侵袭能力,抑制血管生成。ELF5过表达可抑制小鼠肿瘤生长。
ELF5在RCC中高度甲基化,DNA甲基转移酶(DNA methyltransferases, DNMT )可促进ELF5在RCC细胞中的高甲基化水平。进一步证实ELF5在RCC中转录激活USP3。此外,USP3抑制WDTC1泛素化。ELF5可以促进USP3介导的WDTC1稳定。此外,WDTC1沉默逆转了ELF5过表达对RCC进展的作用。DNA超甲基化导致的ELF5下调通过RCC中的USP3/WDTC1轴抑制RCC的发展。

肾细胞癌(Renal cell carcinoma, RCC)是一种起源于肾小管的常见恶性肿瘤。其发病率仅次于前列腺癌和膀胱癌,近十年来呈上升趋势。由于缺乏特异性症状,RCC通常诊断较晚,因此治疗难度较大。转移性RCC患者比例较高,生存率较低,仅为13%左右。目前,根治性手术仍是早期RCC患者的主要治疗方法。由于RCC对放疗不敏感,基因靶向治疗为其治疗提供了一个有希望的新方向。因此,鉴定新的可行的生物标志物是开发更好的治疗方法和提高RCC患者生存率的关键。
血管生成是指原有血管生成新血管,是组织修复和发育的重要生理过程。越来越多的研究表明,血管生成是实体瘤发展的关键过程。它为肿瘤提供生长所需的氧气和营养,同时允许二氧化碳和代谢物的排泄。此外,血管生成支持恶性细胞从原发肿瘤部位转移到远处器官。血管内皮生长因子(Vascular endothelial growth factor, VEGF)由于具有促有丝分裂功能,是最有效的促血管生成因子。在RCC中,有报道称TNF受体相关因子1可通过促进血管生成来促进舒尼替尼耐药。F-Box蛋白22通过抑制细胞迁移侵袭和VEGF介导的血管生成,抑制RCC的肿瘤转移。沉默表皮生长因子样结构域蛋白7可通过抑制RCC血管生成来抑制肿瘤生长。因此,血管生成的调控对于制定新的RCC治疗策略至关重要。
ELF5属于ETS家族,可以调控人类癌症中参与细胞增殖、分化、凋亡和转移的基因。此外,ETS家族已被证实在胚胎血管生成、血管生成和造血中发挥重要作用。ELF5主要表达于上皮细胞,是癌细胞EMT的抑制因子。大多数证据表明,ELF5在抑制不同人类癌症的肿瘤发生和发展中发挥重要作用。例如,ELF5缺失可通过干扰素-γ信号传导促进乳腺癌转移。ELF5通过灭活SMAD3抑制前列腺癌上皮-间质转化过程。ELF5抑制卵巢癌细胞迁移和侵袭。重要的是,ELF5 mRNA和蛋白在RCC中已被证实降低,重新表达ELF5可抑制细胞增殖和存活,这表明ELF5在肾脏中具有抑瘤活性。然而,ELF5在RCC血管生成中的作用尚不清楚。
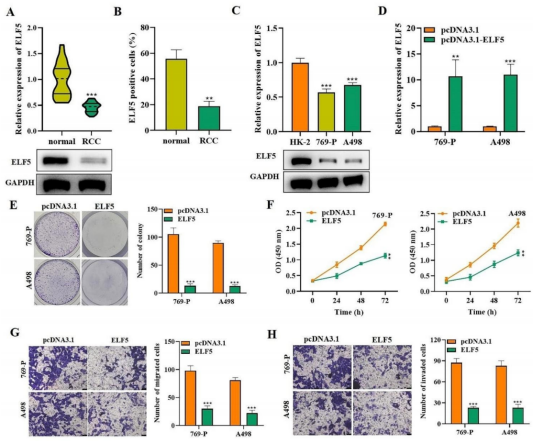
高ELF5表达抑制RCC细胞增殖、迁移和侵袭(图源自Molecular Cancer )
表观遗传改变是癌症发展的重要因素。DNA甲基化是最常见的表观遗传学形式,它可以改变基因表达而不改变DNA序列。越来越多的研究证实,基因启动子区域的高甲基化可直接导致基因表达水平的降低。DNA甲基化是由DNA甲基转移酶(DNA methyltransferases, DNMTs)建立的。5-Aza-2-脱氧胞苷(5-Aza-dC)是一种DNMTs抑制剂,可引起全基因组低甲基化并抑制癌细胞生长。
有报道称,ELF5在尿路上皮癌中的下调与DNA甲基化有关,并可通过5-Aza-dC逆转。因此,DNA甲基化也可以解释低表达的ELF5在RCC中调节肿瘤活性的作用。该研究证明ELF5在RCC中由于DNA超甲基化而下调表达。ELF5通过激活USP3的转录来稳定RCC中的WDTC1,作为肿瘤抑制因子。这些发现可能为RCC提供新的治疗靶点。
原文链接:
https://doi.org/10.1186/s12943-023-01871-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#肾细胞癌# #尿路上皮癌# #ELF5# #血管生成抑制#
39