Oncol Lett:肿瘤细胞与正常组织RAGE的表达差异
2012-07-02 Beyond 生物谷
高迁移率族蛋白B1(high mobility group protein,HMGB1)是一种高度保守的核蛋白,广泛分布于哺乳动物细胞。随着其晚期促炎作用的发现,HMGB1成为近年来危重医学研究的热点之一。 近日Oncol Lett杂志上刊登的一则研究归纳总结了HMGB1蛋白与癌症发展之间的关系。 研究人员总结认为HMGB1表达的升高与某些原发性肿瘤类型包括恶性黑色素瘤、结肠癌、前列腺癌、胰腺癌
高迁移率族蛋白B1(high mobility group protein,HMGB1)是一种高度保守的核蛋白,广泛分布于哺乳动物细胞。随着其晚期促炎作用的发现,HMGB1成为近年来危重医学研究的热点之一。
近日Oncol Lett杂志上刊登的一则研究归纳总结了HMGB1蛋白与癌症发展之间的关系。 研究人员总结认为HMGB1表达的升高与某些原发性肿瘤类型包括恶性黑色素瘤、结肠癌、前列腺癌、胰腺癌和乳腺癌等都有关,并在大多数情况下,HMGB1的表达水平与肿瘤细胞的侵袭和转移能力呈正相关性。
HMGB1通过与晚期糖化终产物受体(RAGE)相互作用来发挥促肿瘤作用。有些数据表明,RAGE和HMGB1表达升高不一定是肿瘤发展、预后差的一个先决条件,配体/受体的细胞定位也需要考虑。但这些数据只关注了HMGB1蛋白以及其受体RAGE在各种组织和肿瘤细胞中的整体表达情况。然而,并没有提及他们的细胞定位情况,也没有提供直接证据能证明两者之间能形成络合物。
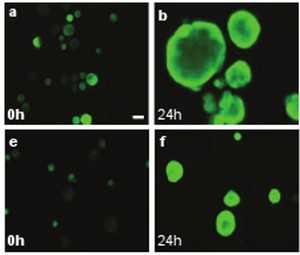
而在本研究中,研究人员着重分析大鼠各个器官中HMGB1及其受体RAGE的分布,对照组为Guerin腹水肿瘤细胞。在正常组织中,HMGB1蛋白质以其可溶性形式存在,而在肿瘤细胞中,他们是不溶性、具有结合细胞膜能力的形似存在。HMGB1主要于与RAGE形成稳定的蛋白片段络合物,存在于癌细胞膜上。(生物谷:Bioon.com)

doi:10.3892/ol.2011.459
PMC:
PMID:
High mobility group B1 protein interacts with its receptor RAGE in tumor cells but not in normal tissues.
Todorova J, Pasheva E.
The high mobility group box 1 (HMGB1) protein is an abundant non-histone component of chromatin well known for its two DNA binding domains, HMG box A and HMG box B. The main characteristics of the HMGB1 protein as an 'architectural' factor are its ability to recognize and bind with high affinity to distorted DNA and its ability to induce kinks in linear DNA fragments. The HMGB1 protein has been correlated to cancer progression. An elevated expression of HMGB1 occurred in certain types of primary tumor, including melanoma and colon, prostate, pancreatic and breast cancers, and in the majority of cases HMGB1 is associated with invasion and metastasis. The main signaling pathway is activated through the interaction of HMGB1 with its Receptor for Advanced Glycation End products (RAGE). Certain data indicate that an elevated expression of RAGE and HMGB1 is not always a prerequisite of poor prognosis of tumor development. The cellular localization of the ligand/receptor pair also requires consideration. The data concerning the expression of HMGB1 protein and its receptor RAGE in various tissues and tumor cells reflect the overall production of the proteins. However, they do not refer to their cellular localization and there is no direct evidence for the formation of a stable complex between them. In the present study, we investigated the subcellular distribution of HMGB1 and its receptor RAGE in various rat organs compared to Guerin ascites tumor cells. In the normal tissues the proteins exist in their soluble form, whereas in the tumor cells they are insoluble and membrane-bound. HMGB1 forms a stable complex with RAGE only in the protein extract derived from the cancer cells predominantly in the membrane fraction.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#表达差异#
37
#Oncol#
29
#肿瘤细胞#
22