临床新探索!一代EGFR-TKI一线治疗耐药后加用阿帕替尼,PFS不逊三代TKI
2023-12-26 苏州绘真医学 苏州绘真医学 发表于上海
我们开展了一项单臂前瞻性研究,评估阿帕替尼联合EGFR-TKI在一线EGFR-TKI治疗后缓慢进展的患者中的疗效和安全性。
表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)获得性耐药是NSCLC治疗中不可避免的事件。为此,天津医科大学总医院开展了一项单臂前瞻性研究,纳入了12例第一代EGFR-TKI一线治疗后缓慢进展的NSCLC患者,接受每日250mg阿帕替尼联合初始EGFR-TKI治疗,评估疗效和安全性。进行循环肿瘤DNA(ctDNA)分析,动态监测治疗效果。7例患者被纳入疗效分析。阿帕替尼联合EGFR-TKI的中位PFS2为8.2个月(95% CI,7.3 m-NA),加上PFS1,总PFS达20.9个月(95% CI,17.3 m-NA)。所有不良事件均可控。ctDNA清除患者(8.4个月;95% CI,8.2-NA)的中位PFS显著长于ctDNA未清除患者(7.1个月;95% CI,6.9-NA)(p = 0.0082)。加用阿帕替尼改善了第一代EGFR-TKI治疗的有效时间,且长于第三代EGFR-TKI一线治疗。当患者在初始EGFR-TKI治疗后缓慢进展时,加用阿帕替尼可能是一种较好的治疗选择,并且副作用是可控的。可以使用ctDNA监测治疗效果。
研究背景
在美国,晚期肺癌的总体 5 年生存率低至 18%。临床上表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)的使用改善了肺癌患者的生存预后。然而,EGFR-TKI耐药性是不可避免的问题。大多数第一代EGFR-TKI,如吉非替尼和厄洛替尼,在约12个月后产生耐药性。
已经揭示了第一代EGFR-TKI获得性耐药的许多机制,例如EGFR T790M守门人突变,MET扩增,STAT3过度激活,STST3激活,PIK3CA,转化为小细胞肺癌和细胞周期失调。奥希替尼是第三代EGFR-TKI,对T790M突变患者有效,但大多数患者在6个月内出现耐药性。因此,在肺癌治疗中,克服对第一代靶向药物的获得性耐药仍然是一个挑战。
阿帕替尼是一种新型 VEGF 受体 2 TKI,是一种抗血管生成药物,在多种恶性肿瘤中表现出良好的抗肿瘤活性和良好的耐受性。在 EGFR 突变晚期 NSCLC 中,阿帕替尼联合吉非替尼一线治疗的 PFS 为 13.7 个月,而吉非替尼为 10.2 个月。同时使用阿帕替尼和 EGFR-TKI 可改善 PFS, 而我们认为,序贯加用阿帕替尼也许可以实现更长的PFS。本研究探索了在 NSCLC 患者使用 EGFR-TKI 后缓慢进展时加用阿帕替尼的临床有效性。
在临床实践中,目前通常使用 CT 成像和血清癌胚抗原(CEA)评估 NSCLC 对治疗的反应,但这些方法并不能完全反映治疗期间肿瘤发生的分子和病理变化。主要由凋亡和坏死癌细胞释放的循环肿瘤DNA(ctDNA)也被证明可用于监测NSCLC靶向治疗、化疗和免疫治疗的疗效。
我们开展了一项单臂前瞻性研究,评估阿帕替尼联合EGFR-TKI在一线EGFR-TKI治疗后缓慢进展的患者中的疗效和安全性。同时,我们全面分析ctDNA,动态监测治疗效果。
患者和方法
招募2018年7月至2021年3月在天津医科大学总医院肺部肿瘤外科新诊断的原发性肺癌患者。共纳入12例一线EGFR-TKI治疗后缓慢进展的NSCLC患者,接受每日250mg阿帕替尼联合初始EGFR-TKI治疗,直至疾病进展或出现不可接受的毒性。缓慢进展定义为:每隔 2-4 个月进行一次 CEA 检测和影像学检查,与 EGFR-TKI 治疗前的 CEA 水平相比,连续三次检测 CEA 水平异常升高,或者根据 RECIST 1.1,与之前的评估相比,靶病灶相对增大 0%-20%。在基线和开始联合治疗后每隔 2-4 个月收集外周血用于 CEA 和 ctDNA 检测。
研究结果
基线临床病理特征
12例患者中,7例(58.3%)为女性,5例(41.7%)为男性,中位年龄为66岁,范围为44至78岁。大多数患者为非吸烟者(9/12,75%)。三分之二(66.7%)的患者为IIIB期,其余为IVa期或IVb期。所有患者均诊断为腺癌。三分之二的患者(8/12)没有转移,1例脑转移,2例骨转移和1例胸膜转移。接受的一线EGFR-TKI药物包括吉非替尼、埃克替尼和厄洛替尼。中位PFS1为13.1个月(95% CI,10.6m-NA),范围为8.9-16.4个月(图1A)。
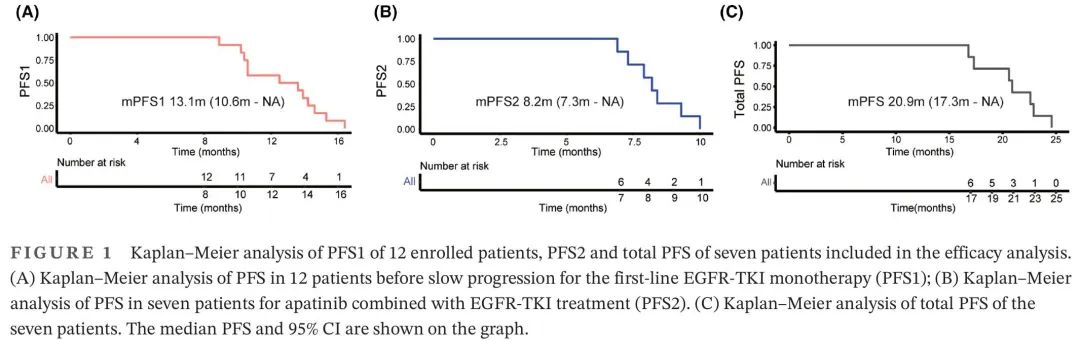
图1
治疗和疗效
所有 12 例患者均接受口服阿帕替尼(250 mg/日)联合初始 EGFR-TKI(剂量由主要研究者确定)治疗。其中7例患者至少进行了一次影像学随访,被纳入疗效分析。5例患者被排除在外,其中2例失访,3例未遵从研究方案。7例患者均实现SD。直到 2021 年 5 月的最后一次随访,这 7 例患者都还活着。中位PFS2为8.2个月(95% CI,7.3 m-NA),加上每位患者的PFS1,总PFS达20.9个月(95% CI,17.3 m-NA)(图1B,C)。
不良事件
最常见的不良事件(AE)包括1/2级高血压(6,50%)、手足综合征(4,33.3%)、厌食(3,25%)、大便潜血(3,25%)和蛋白尿(2,16.7%),未观察到3/4级不良事件,所有不良事件均可控制。
基线样本基因突变谱和KEGG通路富集
对12例患者在阿帕替尼联合EGFR-TKI治疗前收集血浆作为基线样本。基因检测显示,EGFR(25%)、FAT3(17%)和TP53(17%)基因突变频率最高。接下来,KEGG通路富集分析显示,突变基因显著富集于FoxO和内分泌抵抗信号通路。
ctDNA动态监测联合治疗疗效
开始联合治疗以来,7 例患者每隔 2-4 个月收集血浆样本,以动态监测 ctDNA 和 CEA 的变化。ctDNA变异丰度(VAF)的动态如图2A所示,5例患者:P01、P02、P04、P05和P06在监测期间有至少一次ctDNA清除。而患者 P07 和 P03,ctDNA 始终是可检测到的。我们发现,ctDNA清除患者(8.4个月,95% CI,8.2-NA)的mPFS显著长于ctDNA未清除患者(7.1个月,95% CI,6.9-NA,p = 0.0082)(图2B)。患者P05和P07疾病进展后继续监测ctDNA,均检测到ctDNA,特别是P07的ctDNA VAF大幅增高(图2A)。每mL血浆ctDNA拷贝数的变化与ctDNA VAF几乎相同。关于CEA监测,患者P04和P06的浓度始终在正常范围内(<5 ng/mL),而其他患者则超出正常范围(≥5 ng/mL)。正常CEA组(9.65个月;95% CI,9.3-NA)的mPFS长于异常CEA组(7.9个月;95% CI,7.3-NA;p = 0.041)(图2C)。患者P07疾病进展后,ctDNA增加了很多,而CEA保持稳定,提示CEA不是反映疾病进展的可靠标志物。
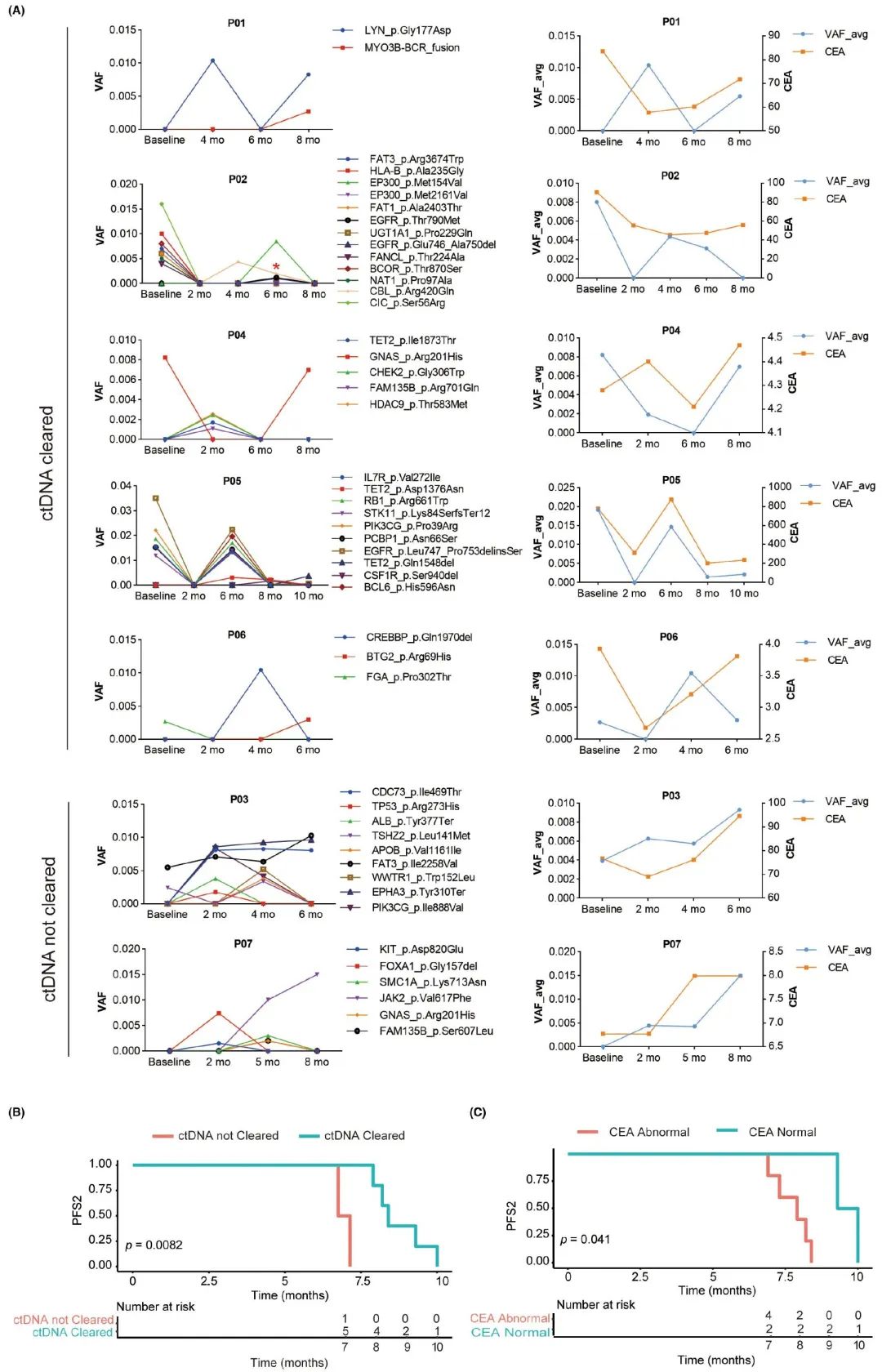

图2
讨 论
本研究旨在通过序贯加用阿帕替尼来延长EGFR-TKI一线治疗的有效时间。既往研究WJTOG3405、NEJ002和OPTIMUM表明,第一代EGFR-TKI作为EGFR突变晚期NSCLC一线治疗的mPFS仅为9-13个月,这限制了EGFR-TKI的临床应用。
ARTEMIS(CTONG1509)、NEJ026、RELAY 和 ACTIVE(CTONG 1706)研究显示,与单独使用 EGFR-TKI 相比,EGFR-TKI 联合抗血管生成药物可延长 PFS。本研究结果表明,加用阿帕替尼使总 mPFS 延长至 20.9 个月(95% CI,17.3-NA),比这些先前研究中的 PFS 更长或相似。这些先前研究与本研究的区别在于抗血管生成药物的干预时间。在这些先前研究中,抗血管生成药物与EGFR-TKI同步使用,而在本研究中,在EGFR-TKI单药治疗后缓慢进展时加用抗血管生成药物,即序贯模式。结果表明,尽管同步模式和序贯模式都延长了EGFR-TKI的PFS,但序贯模式可以降低医疗成本,并可能减少抗血管生成药物的不良反应。
使用第三代EGFR-TKI作为一线治疗选择也是延长EGFR-TKI有效时间的一种方法。例如,奥希替尼的mPFS为18.9个月,阿美替尼为19.3个月。提示第三代EGFR-TKI作为一线治疗方案的PFS与本研究中的PFS相当。
我们从安全性和有效性的角度考虑了阿帕替尼的剂量。在Zhou等人的临床试验中,阿帕替尼剂量为每日 500 mg或 750 mg。CTONG1706研究表明,与其他类似临床试验相比,每日 500 mg阿帕替尼联合吉非替尼导致更多的 ≥3 级不良事件。为了确定阿帕替尼的剂量,我们首先尝试以每日 250 mg或 500 mg的剂量治疗一些病例,发现与EGFR-TKI联用时,250mg与500mg阿帕替尼一样有效,但耐受性更好。因此,我们确定剂量为250mg。在研究期间,当患者AE严重时,我们以两种方式调整阿帕替尼剂量:每周5日或每2日一次。如果 AE 没有减弱,建议停药。大多数患者可以适应这种剂量调整。
在本研究中,ctDNA清除组和未清除组的PFS存在显著差异(图2A)。ctDNA的这种反应作用在几项研究中也有报道。一项研究探索了 NSCLC 靶向治疗的 ctDNA 反应,发现应答者ctDNA几乎完全消除,而无应答者 ctDNA 水平变化有限,PFS 显著较短。在免疫治疗和化疗疗效监测中也观察到类似的结果。
本研究的主要局限性是样本量小,可能导致分析偏倚。但是本研究提供了宝贵信息,表明阿帕替尼能够延缓EGFR-TKI耐药性,ctDNA分析可用于监测疗效。首先,加用阿帕替尼可延长第一代EGFR-TKI治疗的有效时间,为解决临床TKI耐药问题提供参考。其次,ctDNA可作为监测治疗效果的生物标志物,作为非侵入性液体活检,未来可能在疗效监测方面发挥更大的作用。为了得到更可靠的结论,需要进一步开展大规模、多中心临床试验。
参考文献:
Liu M, Li X, Zhang H, Ren F, Liu J, Li Y, Dong M, Zhao H, Xu S, Liu H, Chen J. Apatinib added when NSCLC patients get slow progression with EGFR-TKI: A prospective, single-arm study. Cancer Med. 2023 Nov 30. doi: 10.1002/cam4.6737. Epub ahead of print. PMID: 38033095.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#非小细胞肺癌# #阿帕替尼# #表皮生长因子受体酪氨酸激酶抑制剂#
41