盘点 2023|黄慧强教授:2023年度淋巴瘤领域进展
2024-02-08 医悦汇 医悦汇 发表于陕西省
2023年度,淋巴瘤治疗领域继续向前迈进,不断涌现出新的治疗方法和技术,这些进展将为淋巴瘤患者带来更好的生存率和生活质量,为最终实现淋巴瘤的精准治疗提供更坚实的基础。
盘点2023 淋巴瘤进展
淋巴瘤作为一种全世界常见的恶性肿瘤之一,一直是医学研究和临床治疗的重要领域。淋巴瘤的多样性和复杂性给治疗带来了挑战。在过去的几年中,淋巴瘤治疗领域经历了快速的发展,细胞治疗(CAR-T和CAR-NK)、双特异性抗体(CD3-CD20双抗)、抗体偶联药物(CD79b、CD30和CD25 ADC药物)、小分子靶向药物(PI3K、BTK、XPO-1和BCL2抑制剂等)和新靶点单抗药物(CCR4单抗等)的进展为淋巴瘤患者带来了新的希望,淋巴瘤患者的预后持续改善。
2023年度,淋巴瘤治疗领域继续向前迈进,不断涌现出新的治疗方法和技术,这些进展将为淋巴瘤患者带来更好的生存率和生活质量,为最终实现淋巴瘤的精准治疗提供更坚实的基础。(本文根据个人的判断选取关键的临床进展文章或会议摘要。)
1 CAR-T细胞:ZUMA研究随访更新
CART细胞是一种非常有前景的肿瘤细胞治疗手段,目前广泛应用于血液肿瘤。ZUMA-7研究对比了Axicabtagene Ciloleucel(Axi-Cel)和标准治疗(SOC)用于治疗二线R/R DLBCL,既往已报道了中位随访24.9个月的生存数据[1],最新的随访数据于2023年7月发表在《新英格兰医学杂志》[2]。中位随访47.2个月时,Axi-cel组和SOC分别有82例和95例患者死亡。Axi-cel组的中位总生存期(OS)未达到,而SOC组为31.1个月;预估4年OS分别为54.6%和46.0%(图1)。而中位无进展生存期(PFS)在Axi-Cel组为14.7个月,SOC组为3.7个月,预估4年的PFS分别为41.8%和24.4%(图2)。长期随访的结果仍然显示,Axi-cel组的PFS及OS均于SOC组。
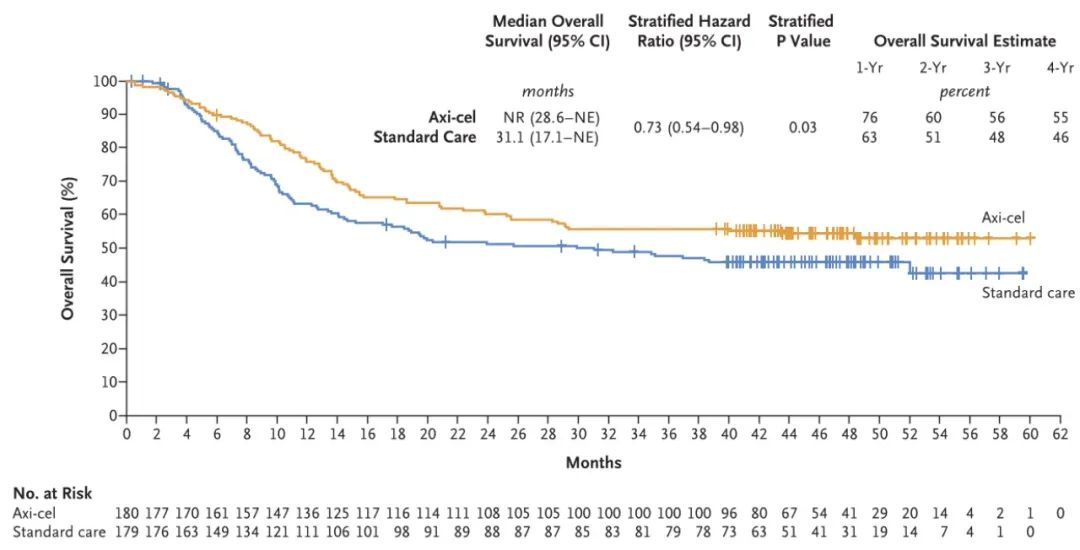
图1:Axi-cel组和SOC组总生存(OS)的Kaplan-Meier曲线
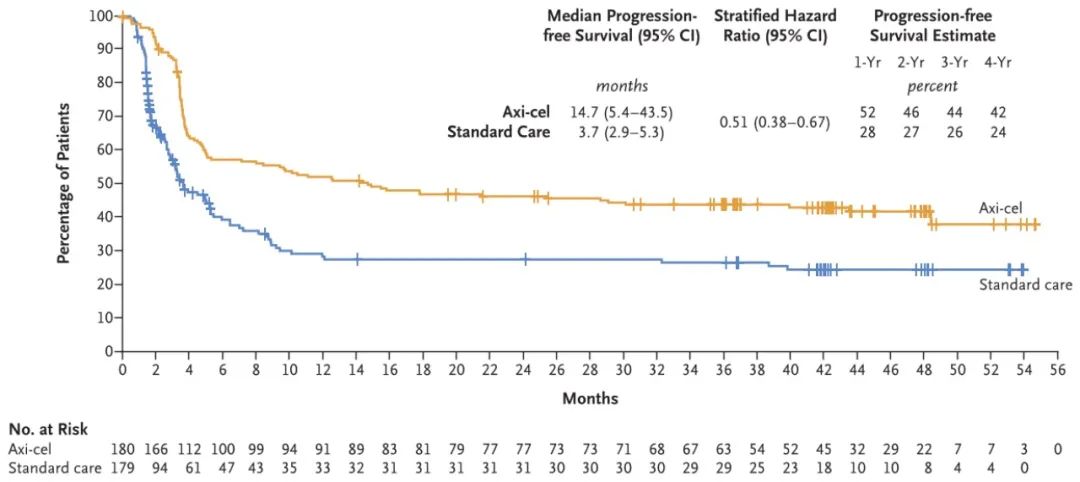
图2:Axi-cel组和SOC组无进展生存(PFS)的Kaplan-Meier曲线
CAR-T治疗改变了R/R DLBCL患者的的治疗现状,然而由于有效性和安全性数据有限,它在老年患者中的应用仍然不足。一项多中心回顾性研究评估了CART在老年患者中的实际结果[3]。研究共纳入209名年龄≥65岁的R/R LBCL患者接受了商业化CART产品。CART回输中位年龄为71岁(65-89岁),既往治疗的中位数为2线(范围1-8)。患者接受的商业化CART产品最多的是Axi-Cel(63%,n=131),其次是liso-cel(24%, n=49)和tisa-cel(13%,n=27)。75%的患者发生细胞因子释放综合征(CRS),少数患者(6%)≥3级。55%的患者发生免疫效应细胞相关神经毒性综合征(ICANS),29%为≥3级。195名患者可评估第30天的反应,ORR为84%,CR为52%。82%的应答者在3个月的随访中仍然有应答。输注后中位随访19.1个月,中位PFS为6.7个月,6个月和12个月PFS率分别为54%和43%。中位生存期为16.5个月,6个月和12个月的生存期分别为70%和61%。该研究显示,CART治疗显示出与注册临床试验相当的良好疗效和安全性。无论患者年龄(包括年龄≥80岁的患者)和使用的CART产品类型如何,生存结果似乎相似。与年轻患者相似,在CART输注时,高肿瘤负荷和不良状态与较低的生存率相关。该分析证实,老年患者不应仅仅因为实足年龄而被排除在接受CART治疗之外。
大量临床研究和真实世界临床观察长期随访结果,再次证明恶性淋巴瘤CART的确是一种独特、持久有效和安全的细胞治疗方法。
2 CD20×CD3双抗成为CAR-T失败患者新选择
CAR-T细胞疗法已经在临床中显示出显著的疗效,然而,40%-60%的R/R DLBCL患者在接受治疗后出现复发或病情进展,其中位OS短于6个月。CAR-T治疗后进展的患者可选的方案较少。格菲妥单抗是一种CD20×CD3(2:1)双特异性抗体。今年的美国血液学会(ASH)年会报告了一项针对CAR-T细胞治疗失败的R/R B-NHL患者接受格菲妥单抗治疗的II期多中心研究主要结果4。
截至2023年6月2日,该研究共入组了67例CAR-T细胞治疗无效的B-NHL患者,其中63例患者接受了≥1个剂量的治疗,入组患者分为DLBCL(队列1,44例)或non-DLBCL(队列2,19例)。患者既往治疗线数的中位数为3线(范围:2-6),13例(20.6%)为难治性(对CAR-T细胞治疗无反应),50例(79.4%)为复发/进展,复发/进展主要是发生在CAR-T细胞输注后的1~3个月(15例,30%),3-6个月(18例,36%)和6个月以上(17例,34%)。队列 1 和队列 2 的总体ORR分别为 65.9%(CMR:36.4%)和 57.9%(CMR:52.6%)。队列1和队列2的中位PFS分别为4.9个月和4.1个月。同时,格菲妥单抗安全性可控。主要的不良反应(AEs)为血液性毒性,9例患者(14.3%)发生CRS(1级:3例,2级:6例),2例出现神经相关事件(2级)。总的来说,格菲妥单抗治疗可显著延长CAR-T细胞治疗后复发或进展B-NHL患者的生存,为患者带深度且持久的缓解,且安全性可控。
Epcoritamab是一种皮下、现成的CD3xCD20双特异性抗体,最近在美国被批准用于治疗R/R DLBCL。由于缺乏直接比较CAR-T与双抗的临床研究,有研究者对EPCORE NHL-1中接受epcoritamab治疗中未接受CAR-T治疗的患者进行了间接比较[5]。经符合条件匹配调整间接比较后,显示epcoritamab和CAR-T细胞治疗组的ORR有显著差异(77.9%和53.0%;P = 0.002),CRR分别为52.3%和39.1%(P = 0.174)。此外,在未经CAR-T治疗队列中,调整后epcoritamab与CAR-T组有PFS获益的趋势(HR:0.725;P = 0.194)。在适宜CAR-T亚组中,epcoritamab与CAR-T组相比ORR(80.8% vs 53.0%;P = 0.001)和CRR(61.9% vs 39.1%;P = 0.036)有显著差异。此外,OS的生存获益也有统计学意义(HR:0.450;P = 0.022)和PFS获益趋势(HR:0.548;P = 0.051)。在缺乏头对头数据的情况下,未经CAR-T治疗的R/R DLBCL中接受epcoritamab与CAR-T治疗的患者,数据调整后的亚组分析,显示出缓解率和生存结果得以改善。但间接比较可能因交叉试验差异而产生偏倚,需要进行更长时间随访的进一步比较。
3 淋巴瘤免疫疗法的发展
免疫治疗在淋巴瘤中取得了良好的临床疗效,包括霍奇金淋巴瘤、原发纵隔大B细胞淋巴瘤等。现阶段,复发/难治性外周T细胞淋巴瘤(R/R PTCL)的治疗选择较为有限,其有效率较低。由中国学者发起的多中心GEMSTONE-201研究评估了舒格利单抗(PD-L1)在R/R ENKTL中的疗效和安全性[6]。该研究共纳入80例R/R ENKTL患者,中位随访时间为18.7个月,ORR为44.9%,CRR为35.9%,12个月持续缓解率为82.5%,仍有多例患者长期无病生存近3年。治疗过程中,患者发生的AEs大多为1-2级,只有5例患者的评级大于3级SAEs,无治疗相关死亡和治疗延迟,该研究为R/R ENKTL患者提供了新的免疫治疗选择,值得期待。
由于该临床研究的良好结果,舒格利单抗(PD-L1)2023年获得中国药监局NMPA批准治疗复发难治NKT淋巴瘤的适应症,是国内外首个获得该适应症的免疫检查点抑制剂。因此,我们仍需持续关注PD-1/PDL-1单抗在其他淋巴瘤亚型的研究进展。
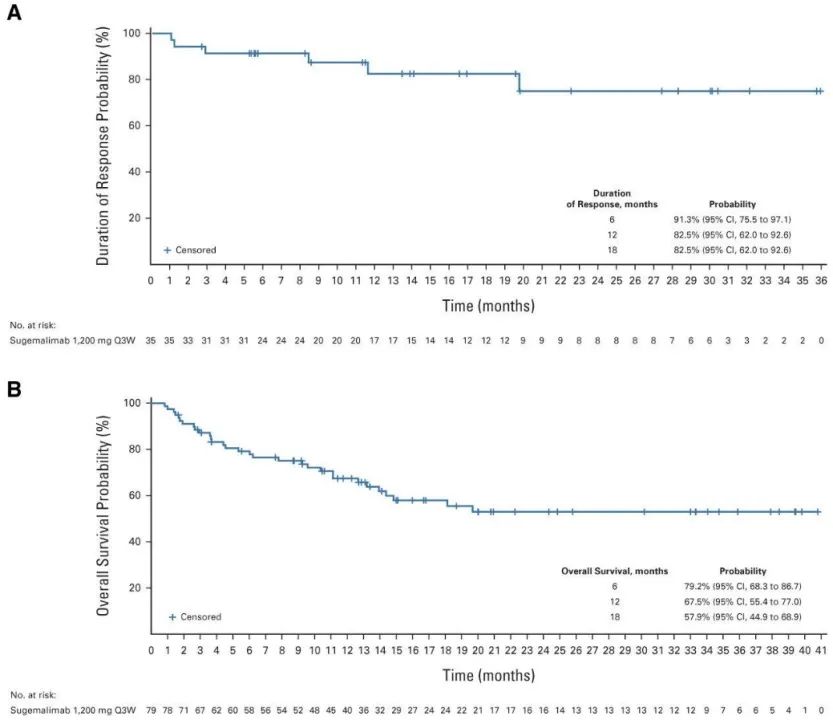
图3:R/R ENKTL患者的有效持续时间和总生存期
此外,LYMA试验证实利妥昔单抗维持(RM)可改善年轻套细胞淋巴瘤(MCL)生存。近期该研究7.5年的长期随访结果于JCO杂志发表7。整个人群的中位PFS和OS尚未达到,7年PFS为55.5%,OS为69.5%。RM组的无时间生存(中位EFS NR vs 5.8年,P<0.0001;HR=0.39)仍然优于观察组。同样,RM延长了PFS(估计7年PFS为78.5% vs 47.4%,HR=0.36,P<0.0001)。估计7年OS分别为83.2%和72.2% (P < 0.05,HR=0.63)。总体而言,年轻患者ASCT后RM的PFS益处在7年随访后仍然存在,并且RM未观察到感染相关死亡率的增加,使该策略成为长期随访的安全标准护理。国际顶尖杂志刊登高水平临床研究长期随访结果,强烈提示传统的免疫治疗仍是现阶段淋巴瘤治疗的有效可靠的治疗手段。
4 靶向治疗进展:BTK、BCL-2、PI3K、JAK1抑制剂新应用
针对淋巴瘤的靶向治疗药物也在2023年度取得了新的进展。既往研究显示,伊布替尼(Ibr)联合维奈克拉(Ven,BCL-2抑制剂)在套细胞淋巴瘤(MCL)中显示出有希望的临床活性。今年的ASH会议上,SYMPATICO作为大会突破性研究(LBA)报告了Ibr+Ven与Ibr+安慰剂(Pbo)在R/R MCL患者中的疗效[8]。共有267名患者入组,1:1随机分配接受Ibr+Ven (n=134)或Ibr+Pbo (n=133)治疗。入组患者中位年龄为68岁,两组患者基线特征大体相似。研究的中位时间为51.2个月,Ibr+Ven显著提高了CR率(54% vs 32%)和研究者评估的中位PFS (31.9 vs 22.1个月),HR为0.65 (P = 0.0052)。Ibr+Ven和Ibr+Pbo的24个月PFS率分别为57%和45%。Ibr+Ven组84%的患者发生≥3级AEs,而Ibr+Pbo组为76%。最常见的AEs是中性粒细胞减少症(31% vs 11%)、肺炎(13% vs 11%)、血小板减少症(13% vs 8%)、贫血(10% vs 3%)。两组中各有60%的患者发生严重不良反应。与Ibr+Pbo相比,Ibr+Ven联合治疗显著改善R/R MCL患者的CR率和PFS,研究结果表明Ibr+Ven在R/R MCL患者中具有良好的获益风险特征。
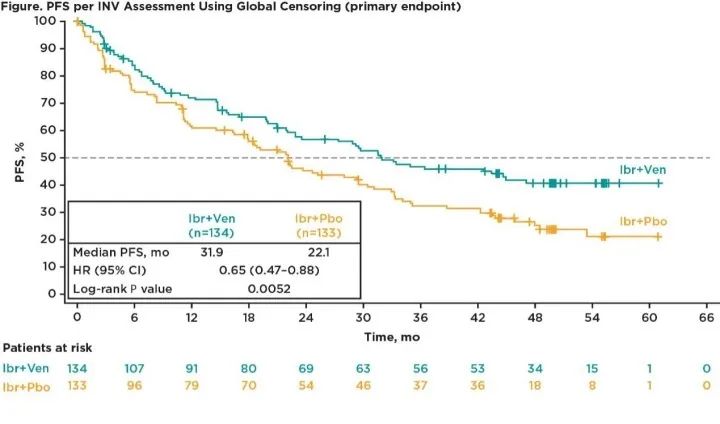
图4:伊布替尼联合维奈克拉对比伊布替尼联合安慰剂R/R MCL的无进展生存
2023年ASH年会上中国学者报道了林普利赛在R/R PTCL II期临床研究的关键结果[9]。共有88例患者用于疗效评估的完整分析集(FAS),入组患者主要为AITL(48例)和PTCL- nos(24例)。纳入分析的患者中位年龄为57岁,既往系统治疗中位数为2次。88例FAS患者中,ORR为48%,其中CRR为30%,PRR 18%,疾病控制率为68%。截至2023年4月24日,中位反应持续时间尚未达到, mPFS为5.5个月。截至中位随访时间13.9个月时,6个月的OS率为75%,中位OS为14.2个月,16例患者继续接受林普利赛治疗。95.9%的患者观察到治疗相关不良事件(TRAE),最常见的TRAE(≥30%)为中性粒细胞减少症(59%)、白细胞减少症(47%)、血小板减少症(32%)。最常见的SAE是肺炎(11%)。研究显示林普利赛对R/R PTCL具有良好的有效率和安全性,与其他PI3K药物相比,严重的胃肠道和肝脏毒性水平较低。
Golidocitinib是首个进入关键临床开发的JAK1选择性抑制剂,用于治疗R/R PTCL。JACKPOT8研究初步分析显示golidocitinib具有良好的抗肿瘤疗效和安全性[10]。该研究招募了至少接受过一种全身治疗的R/R PTCL患者。共有88例疗效可评估的R/R PTCL患者纳入分析。主要病理亚型包括PTCL NOS(56.8%)、AITL(18.2%)和ALCL(11.4%)。根据基于CT成像的IRC评估,39例患者达到肿瘤缓解,ORR为44.3%,26例患者(29.5%)达到完全缓解。DoR的中位随访时间为10.4个月,59%的应答者仍然无事件发生。中位DoR尚未达到,估计12个月DoR率为70.2%。PFS的中位随访时间为9.6个月,中位PFS为5.6个月。最长的PFS为20个月,患者仍有反应。根据研究者的评估,34例患者达到肿瘤缓解(ORR: 38.6%)。中位OS随访时间为15.1个月,约60%的患者仍然存活,估计中位OS为19.2个月。共有112例患者被纳入安全性分析组。共有62名患者(55.4%)报告了≥3级AEs。最常见的药物相关≥3级AEs是血液学不良事件,包括中性粒细胞减少(25%)、白细胞减少(23.2%)和淋巴细胞减少(18.8%)。该关键研究表明Golidocitinib可以作为R/R PTCL患者的有效治疗选择,具有可管理的安全性。
5 早期诊断和监测技术的改进
循环肿瘤DNA(ctDNA)是一种新型的肿瘤标志物。有学者探索了ctDNA MRD检测用于预测DLBCL标准治疗(SOC)治疗后生存[11]。研究入组了99名患者,在3个时间点(基线、中期[C4D1]和治疗结束[EOT])进行ctDNA分析。通过PET/CT、PFS和OS比较MRD水平的标准化反应。所有患者均接受基于蒽环类药物的治疗,其中94%接受RCHOP治疗,6%接受DA-EPOCH-R治疗。结果显示,治疗前ctDNA可显著预测预后(PFS:P=0.004, HR=2.7;OS:P=0.0004, HR=5.1)。在C4D1和EOT时,患者被分为可检测到的和不可检测到的ctDNA-MRD。这两个时间点对患者的预后都有显著的分层,包括C4D1和EOT。研究表明ctDNA-MRD在DLBCL SOC诱导治疗期间和之后使用超灵敏ctDNA-MRD检测的可行性和预后效用。与PET/CT相比,可重复动态检测的ctDNA-MRD具有更高的预测价值和准确性,这表明有机会将此类检测整合到淋巴瘤反应标准中,从而有有望为未来的临床治疗决策提供新的信息。
可测量残留病(MRD)广泛用于指导慢性淋巴细胞白血病(CLL)的治疗。然而,伊布替尼联合维奈克拉根据MRD个性化治疗是否优于氟达拉滨-环磷酰胺-利妥昔单抗(FCR),目前这点尚不清楚。一项多中心三期随机试验比较了MRD指导下伊布替尼联合维奈克拉对比FCR的疗效[12]。研究共入组523例患者,随机分为两组。中位43.7个月时,伊布替尼联合维奈克拉组中有12名患者出现疾病进展或死亡,FCR组中有75名患者出现疾病进展或死亡(HR 0.13;P<0.001)。伊布替尼联合维奈克拉组有9例患者死亡,FCR组有25例患者死亡(HR 0.31)。在3年时,58.0%的伊布替尼联合维奈克拉组患者由于无法检测到MRD而停止治疗。经过5年的伊布替尼治疗,65.9%的患者骨髓MRD检测不到,92.7%的患者外周血MRD检测不到。研究表明,与FCR相比,MRD导向的伊布替尼联合维奈克拉改善了PFS和OS。NGS ctDNA的动态监测,逐渐成为临床监测淋巴瘤等恶性肿瘤MRD的敏感稳定的手段。
6 结论
在2023年度,淋巴瘤领域取得了一系列重大进展,涵盖了细胞治疗、免疫治疗、靶向治疗和诊断技术等多个方面。这些进展为淋巴瘤患者带来了新的治疗选择和希望,为实现淋巴瘤的精准治疗提供了重要的支持。
鸣谢:中山大学肿瘤医院平丽琴博士
参考文献
1.Locke, F. L.; Miklos, D. B.; Jacobson, C. A.; Perales, M. A.; Kersten, M. J.; Oluwole, O. O.; Ghobadi, A.; Rapoport, A. P.; McGuirk, J.; Pagel, J. M.; Muñoz, J.; Farooq, U.; van Meerten, T.; Reagan, P. M.; Sureda, A.; Flinn, I. W.; Vandenberghe, P.; Song, K. W.; Dickinson, M.; Minnema, M. C.; Riedell, P. A.; Leslie, L. A.; Chaganti, S.; Yang, Y.; Filosto, S.; Shah, J.; Schupp, M.; To, C.; Cheng, P.; Gordon, L. I.; Westin, J. R., Axicabtagene Ciloleucel as Second-Line Therapy for Large B-Cell Lymphoma. The New England journal of medicine 2021.
2.Westin, J. R.; Oluwole, O. O.; Kersten, M. J.; Miklos, D. B.; Perales, M. A.; Ghobadi, A.; Rapoport, A. P.; Sureda, A.; Jacobson, C. A.; Farooq, U.; van Meerten, T.; Ulrickson, M.; Elsawy, M.; Leslie, L. A.; Chaganti, S.; Dickinson, M.; Dorritie, K.; Reagan, P. M.; McGuirk, J.; Song, K. W.; Riedell, P. A.; Minnema, M. C.; Yang, Y.; Vardhanabhuti, S.; Filosto, S.; Cheng, P.; Shahani, S. A.; Schupp, M.; To, C.; Locke, F. L., Survival with Axicabtagene Ciloleucel in Large B-Cell Lymphoma. The New England journal of medicine 2023, 389 (2), 148-157.
3.Chimeric Antigen Receptor T-Cell Therapy in Elderly Patients with Relapsed or Refractory Large B-Cell Lymphoma: A Multicenter Study,https://ash.confex.com/ash/2023/webprogram/Paper179509.html
4.Glofitamab Monotherapy in Patients with Non-Hodgkin B-Cell Lymphoma after Failing CAR T-Cell Infusion: Primary Analysis of the Bicar Study, a Phase II Lysa Study,https://ash.confex.com/ash/2023/webprogram/Paper177703.html
5.Efficacy of Subcutaneous Epcoritamab Vs Tisa-Cel in R/R LBCL CAR T-Naive and CAR T-Eligible Patients: An Indirect Comparison,https://ash.confex.com/ash/2023/webprogram/Paper180047.html
6.Huang, H.; Tao, R.; Hao, S.; Yang, Y.; Cen, H.; Zhou, H.; Guo, Y.; Zou, L.; Cao, J.; Huang, Y.; Jin, J.; Zhang, L.; Yang, H.; Xing, X.; Zhang, H.; Liu, Y.; Ding, K.; Qi, Q.; Zhu, X.; Zhu, D.; Wang, S.; Fang, T.; Dai, H.; Shi, Q.; Yang, J., Sugemalimab Monotherapy for Patients With Relapsed or Refractory Extranodal Natural Killer/T-Cell Lymphoma (GEMSTONE-201): Results From a Single-Arm, Multicenter, Phase II Study. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 2023, Jco2202367.
7. Sarkozy, C.; Thieblemont, C.; Oberic, L.; Moreau, A.; Bouabdallah, K.; Damaj, G.; Gastinne, T.; Tessoulin, B.; Ribrag, V.; Casasnovas, O.; Haioun, C.; Houot, R.; Jardin, F.; Van Den Neste, E.; Cheminant, M.; Morschhauser, F.; Callanan, M.; Safar, V.; Gressin, R.; Hermine, O.; Le Gouill, S., Long-Term Follow-Up of Rituximab Maintenance in Young Patients With Mantle-Cell Lymphoma Included in the LYMA Trial: A LYSA Study. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 2023, Jco2301586.
8.Ibrutinib Combined with Venetoclax in Patients with Relapsed/Refractory Mantle Cell Lymphoma: Primary Analysis Results from the Randomized Phase 3 Sympatico Study, https://ash.confex.com/ash/2023/webprogram/Paper191921.html
9.A Multicenter Phase2 Trial of Linperlisib in Relapsed or Refractory Peripheral T/NK Cell Lymphomas, https://ash.confex.com/ash/2023/webprogram/Paper180137.html
10.Golidocitinib in Treating Refractory or Relapsed Peripheral T- Cell Lymphoma: Full Analysis of the Multinational Pivotal Study Results (JACKPOT8). https://ash.confex.com/ash/2023/webprogram/Paper172962.html
11.Prognostic Utility of Minimal Residual Disease (MRD) after Curative Intent Induction Therapy for DLBCL: A Prospective Real-World Ctdna Study,https://ash.confex.com/ash/2023/webprogram/Paper187650.html
12.Munir, T.; Cairns, D. A.; Bloor, A.; Allsup, D.; Cwynarski, K.; Pettitt, A.; Paneesha, S.; Fox, C. P.; Eyre, T. A.; Forconi, F.; Elmusharaf, N.; Kennedy, B.; Gribben, J.; Pemberton, N.; Sheehy, O.; Preston, G.; Schuh, A.; Walewska, R.; Duley, L.; Howard, D.; Hockaday, A.; Jackson, S.; Greatorex, N.; Girvan, S.; Bell, S.; Brown, J. M.; Webster, N.; Dalal, S.; de Tute, R.; Rawstron, A.; Patten, P. E. M.; Hillmen, P., Chronic Lymphocytic Leukemia Therapy Guided by Measurable Residual Disease. The New England journal of medicine 2023.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#淋巴瘤# #精准治疗#
22