JCO:veliparib并不能改善BRCA/PALB2基因突变的晚期胰腺癌患者预后
2020-03-16 医者仁心 医者仁心
胰腺导管细胞癌占恶性肿瘤死亡率的第四位,50%的患者诊断时已处于晚期。细胞毒类药物的联合治疗,如亚叶酸、氟尿嘧啶、伊立替康及奥沙利铂、吉西他滨和紫杉醇等药物改善了患者预后,但5年OS率仍低于10%。5
胰腺导管细胞癌占恶性肿瘤死亡率的第四位,50%的患者诊断时已处于晚期。细胞毒类药物的联合治疗,如亚叶酸、氟尿嘧啶、伊立替康及奥沙利铂、吉西他滨和紫杉醇等药物改善了患者预后,但5年OS率仍低于10%。5-9%的晚期胰腺癌患者携带BRCA1/2和PALB2基因突变,而BRCA基因突变导致的肿瘤与铂类药物化疗敏感性有关且与PARPi抑制剂(PARPi)有协同作用。PARPi在BRCA基因突变的乳腺癌及卵巢癌中的应用已经获得批准,而III期POLO研究则证实,PARPi可以作为BRCA基因突变的晚期胰腺癌患者的维持治疗。 这是一项II期临床研究,纳入携带胚系BRCA/PALB2突变的晚期胰腺癌患者(AJCC分期为III期或IV期),年龄大于18周岁,PS评分为0-1分。允许术后复发的患者入组,但末次化疗时间距离复发时间应当超过6个月。既往接受过铂类药物或PARPi治疗的患者不允许入组,存在活动性脑转移的患者同样不允许入组。符合入组标准的患者接受吉西他滨(600mg/m2,第3和第10天用药,21天一个周期)联合顺铂(25mg/m2,第3和第10天用药,21天一个周期)联合或者不联合veliparib(80mg,口服,每日两次,第1-12天用药,21天一个周期)。治疗应当持续进行,直至疾病进展、患者出现不可耐受的不良反应或撤销知情同意。研究期间,每6周进行一次疗效评估,6个月及18个月后,分别每9周和12周进行一系疗效评估。研究的主要终点为ORR,次要研究终点包括DCR、PFS、OS、安全性、耐受性及反应持续时间。 研究结论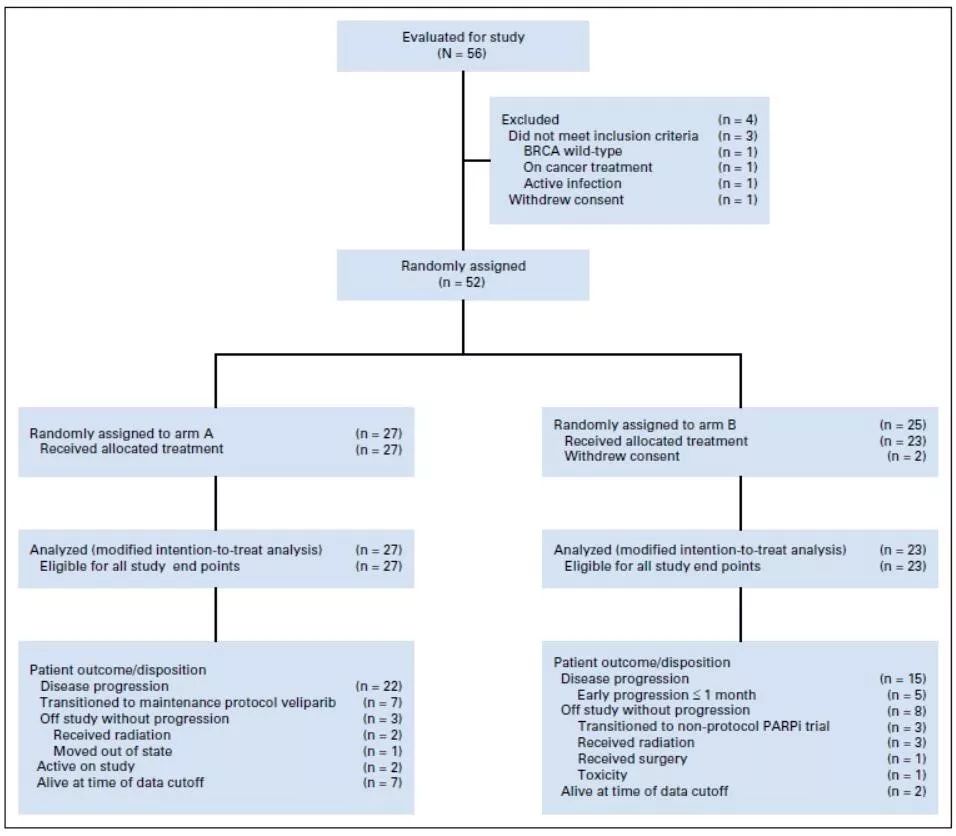
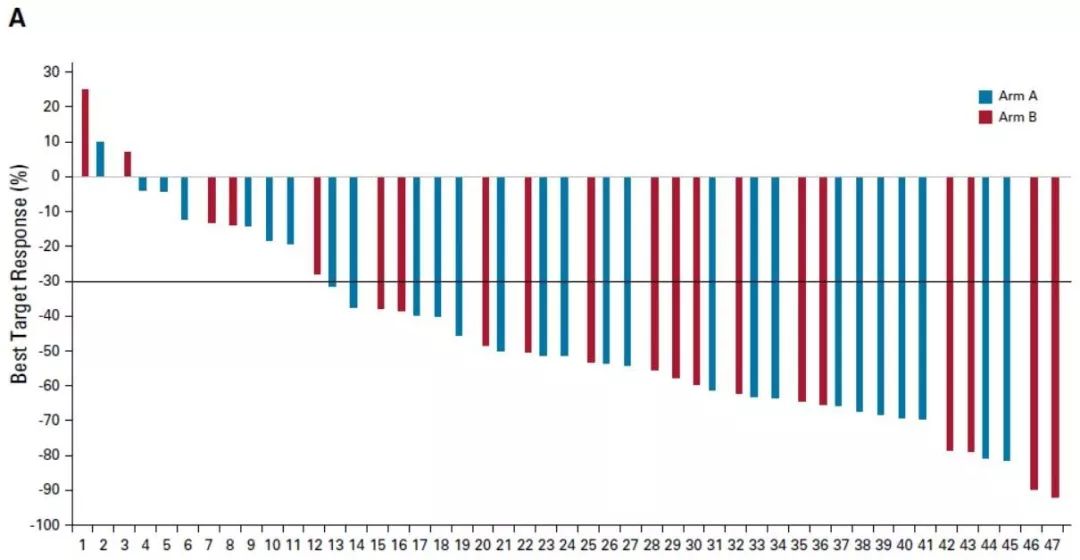
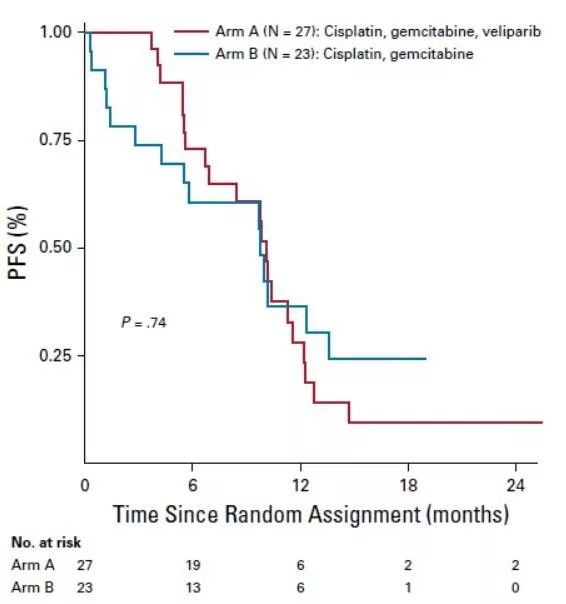
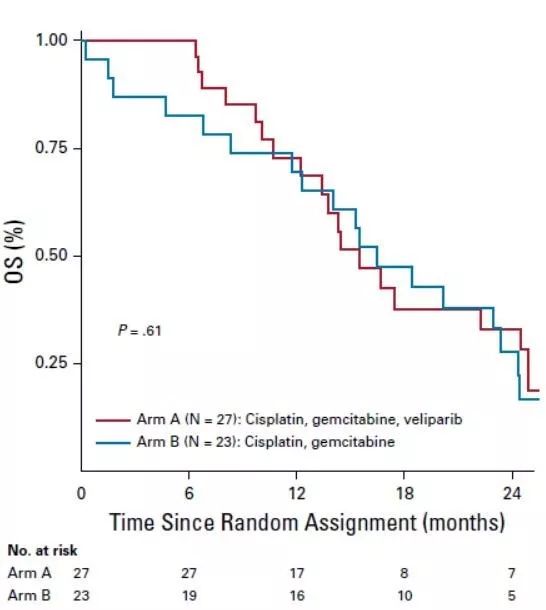
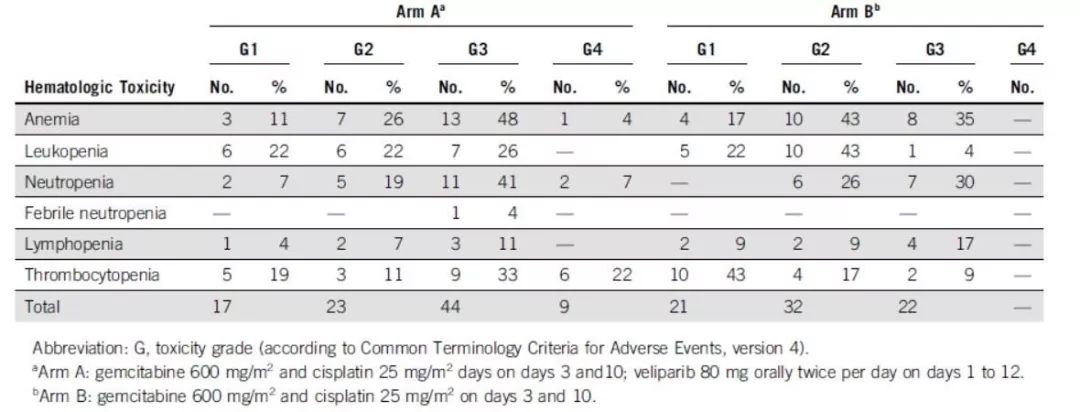
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#JCO#
38
#患者预后#
29
#Veliparib#
31
#晚期胰腺癌#
31
#BRCA#
36
#PALB2#
33