JBC:发现新的抗糖尿病药物GQ-16
2012-05-19 Deepblue 生物谷
过氧化物酶体增殖物激活受体(PPARg)属核激素受体超家族成员,是调节脂肪细胞分化和能量代谢的关键因子。 研究发现,很多抗糖尿病药物主要通过抑制Cdk5介导PPARg的磷酸化来发挥效用。因此,对PPARg的研究能够提供一个新的视角来评估发展更有效的胰岛素敏化剂。 近日,来自巴西利亚大学的研究人员发现了新的抗糖尿病噻唑烷二酮类药物GQ-16,它与阿托伐他汀效用类似,但是不会引起体重增加或者是水肿

过氧化物酶体增殖物激活受体(PPARg)属核激素受体超家族成员,是调节脂肪细胞分化和能量代谢的关键因子。
研究发现,很多抗糖尿病药物主要通过抑制Cdk5介导PPARg的磷酸化来发挥效用。因此,对PPARg的研究能够提供一个新的视角来评估发展更有效的胰岛素敏化剂。
近日,来自巴西利亚大学的研究人员发现了新的抗糖尿病噻唑烷二酮类药物GQ-16,它与阿托伐他汀效用类似,但是不会引起体重增加或者是水肿这些与PPARg活化有关的常见副作用。
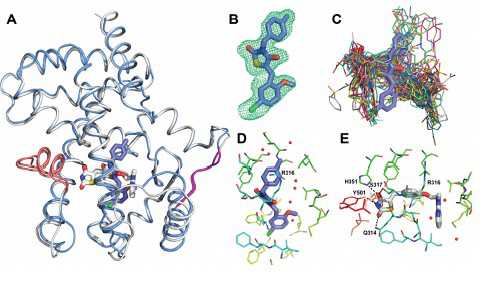
进一步的研究表明,GQ-16能够有效的抑制Cdk5介导的PPARg的磷酸化。对与PPARg结合的GQ-16的结构研究表明,虽然它具有与其它的局部激动剂(如MRL-24或者PA-082,也能够促进胰岛素增敏同时不会引起体重增加)类似的结构特征,这种复合物利用了一个与其它已知的PPARg的配体不同的结合模式。
氢氘交换结果显示,GQ-16能够强烈的稳定PPARg的β片层区域,这可能解释了这种复合物为什么能够抑制Cdk5介导的S273的磷酸化作用。
分子动力学模拟确定了GQ-16的部分激动剂活性,这表明GQ-16能够阻止helix12在活性构象的有效对接。
Kevin J. Phillips表示,该研究阐明了一个新的模型,基于PPARg的治疗能够稳定β片层/S273区域,抑制Cdk5的磷酸化作用,同时最低限度的减少脂肪形成及激动作用,这对发展改良的PPARg调节剂,在保持抗糖尿病活性的同时最大程度的降低副作用,提供了良好的视角。

doi: 10.1074/jbc.M111.332106
PMC:
PMID:
GQ-16, A novel PPARγ ligand, promotes insulin sensitization without weight gain
Angelica A. Amato, Senapathy Rajagopalan, Jean Z. Lin, Bruno Melo Carvalho, Ana Carolina M. Figueira, Jenny Lu, Stephen D. Ayers, Melina Mottin, Rodrigo L. Silveira, Paulo C. T. Souza, Rosa H. V. Mourao, Mario J. A. Saad, Marie Togashi, Luiz A. Simeoni, Dulcineia S. P. Abdalla, Munir S. Skaff, Igor Polikarpov, Maria C. A. Lima, Suely L. Galdino, Richard G. Brennan, John D. Baxter, Ivan R. Pitta, Paul Webb, Kevin J. Phillips and Francisco A. R. Neves.
The recent discovery that PPARg targeted anti-diabetic drugs function by inhibiting Cdk5 mediated phosphorylation of the receptor has provided a new viewpoint to evaluate and perhaps develop improved insulin sensitizing agents.Herein we report the development of novel thiazolidinediones that retain similar anti-diabetic efficacy as rosiglitazone, yet do not elicit weight gain or edema, common side effects associated with PPARg activation.Further characterization of one these compounds show GQ-16 to be an effective inhibitor of Cdk5 phosphorylation of PPARg. The structure of GQ-16 bound to PPARg demonstrates that the compound utilizes a binding mode distinct from other reported PPARg ligands, although it does share structural features with other partial agonists such as MRL-24 and PA-082 that have similarly been reported to dissociate insulin sensitization from weight gain.Hydrogen-deuterium exchange studies reveal that GQ-16 strongly stabilizes the β-sheet region of the receptor, presumably explaining the compounds efficacy in inhibiting Cdk5 phosphorylation of S273.Molecular dynamics simulations affirm the partial agonist activity of GQ-16 indicating that the compound prevents helix 12 from docking efficiently in the active conformation.Our results here suggest that the emerging model, whereby "ideal" PPARg-based therapeutics stabilize the β-sheet/S273 region and inhibit Cdk5 phosphorylation while minimally invoking adipogenesis and classical agonism, is indeed a valid framework to develop improved PPARg modulators that retain anti-diabetic actions while minimizing untoward effects.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#JBC#
34
#糖尿病药物#
26
#抗糖尿病药物#
35