拉罗替尼新辅助治疗NTRK重排骨肉瘤效果如何?基因检测助力罕见肿瘤临床诊疗
2024-02-12 苏州绘真医学 苏州绘真医学 发表于陕西省
本文报告了一例接受拉罗替尼治疗的EML4-NTRK3重排未分化梭形细胞骨肉瘤患者病例,同时讨论了NTRK基因融合阳性骨肉瘤的发病率和临床表现、前期治疗的潜在价值、NTRK抑制剂新辅助治疗的作用。
神经营养性酪氨酸受体激酶(NTRK)基因融合靶向分子药物彻底改写了不同组织学亚型癌症可用治疗有限的格局。恩曲替尼和拉罗替尼在携带NTRK重排的癌症患者中产生了前所未有的缓解率。这一证据使得这些药物近期获批用于泛肿瘤治疗,并且相关证据正在不断出现。本文报告了一例接受拉罗替尼治疗的EML4-NTRK3重排未分化梭形细胞骨肉瘤患者病例,同时讨论了NTRK基因融合阳性骨肉瘤的发病率和临床表现、前期治疗的潜在价值、NTRK抑制剂新辅助治疗的作用,以及多学科肿瘤会诊的意义。尽管这些重排在原发骨肉瘤患者中很少见,但NTRK抑制剂治疗代表了一种高效的治疗策略,即使在新辅助治疗的情况下,也可以在特定的病例中使用。这些十分罕见的癌症治疗应在多学科讨论中进行。
背 景
神经营养性酪氨酸受体激酶1、2和3(NTRK1、NTRK2和NTRK3)基因编码三种酪氨酸激酶受体(分别为TRKA、TRKB和TRKC),并在明确定义的癌症亚组中作为致癌驱动因素。涉及这些基因的融合会导致酪氨酸激酶活性异常升高,从而激活PI3K/AKT/mTOR、Ras/Raf/MAPK和PLCγ信号通路,并最终导致细胞增殖和存活。NTRK基因的其它类型突变(如体细胞点突变)已被报道,但更为罕见。尽管不常见,但NTRK重排可发生在多种癌症中,有报告显示,在总共 26,000 种组织学不常见的癌症中,NTRK重排的频率为 0.28%。
在软组织中,婴儿纤维肉瘤的特征是ETV6:NTRK3易位。此外,在最新的世界卫生组织软组织和骨肿瘤分类中,NTRK重排梭形细胞肿瘤(婴儿纤维肉瘤之外)的新类别被描述为一种新兴实体瘤。这些是以可变的梭形细胞形态为特征的软组织肿瘤。脂肪纤维瘤病样神经肿瘤影响儿童,其组织学特征是以网状模式浸润脂肪的单形态梭形细胞增殖。另一个亚型影响的年龄更加广泛,其特征是中等或高度细胞梭形细胞增殖,具有独特的突出基质带和瘢痕样透明质化胶原血管环。最后一个亚组显示了可变的组织学分级(从低级到高级);它还可以表现出类似于恶性周围神经鞘瘤(“MPNST样”)或纤维肉瘤(“FS样”)的特征。所有NTRK重排肿瘤的特征是CD34和S100的免疫组织化学阳性,以及NTRK1、NTRK2和NTRK3基因与可变伴侣的融合;还描述了RAF1和BRAF融合。虽然脂肪纤维瘤样神经肿瘤是局部侵袭性肿瘤,没有转移潜力,但在其它亚型中,预后似乎与组织学分级相关,在较高级别的病变中会发生肺和其它器官的转移。
最后,NTRK重排在其它肉瘤中已有报道,3/21(14%)的恶性周围神经鞘瘤(MPNST)伴有NF1变异,而在其它成人肉瘤亚型中则非常罕见(<1%,表1)。
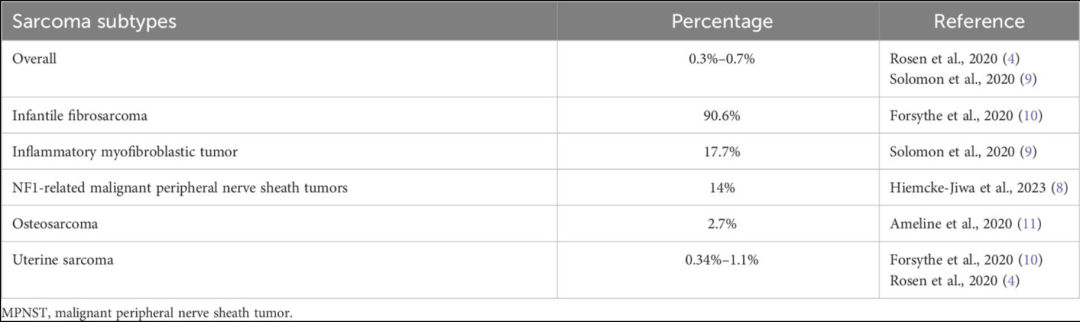
▲表1 肉瘤中NTRK重排的频率
拉罗替尼是一种首创的原肌球蛋白受体激酶(TRK)抑制剂,在三项实体瘤临床试验的pooled分析(也称poled分析)中实现了 75% 的客观缓解率(ORR)和 35 个月的中位无进展生存期(PFS)。此外,在儿童软组织肉瘤中,ORR为 94%,但仍未达到中位PFS。在后续的一个系列研究中,一名骨肉瘤患者出现部分缓解(PR),另一名患者病情稳定(SD)。没有关于骨肉瘤的详细数据。
病 例
患者男,30 岁,因右脚疼痛加剧和功能障碍就诊于意大利里佐利骨科研究所。患者称右脚疼痛是在意外摔倒后出现的。既往病史无异常,无长期服用药物史,无癌症易感综合征家族史或增加癌症罹患风险的疾病。X射线显示跟骨有大的溶解性病变,但没有硬化边缘。足部CT扫描显示跟骨存在大的溶解性病变(图1A),PET-CT扫描显示右脚脚跟处有一个FDG摄取增加的区域(SUV 19.5,图1A)。病变在跟骨附近的软组织上有一个大的隔室外成分,可达皮肤平面。MRI分别显示T1低信号病变和T2/T1脂肪饱和高信号病变。
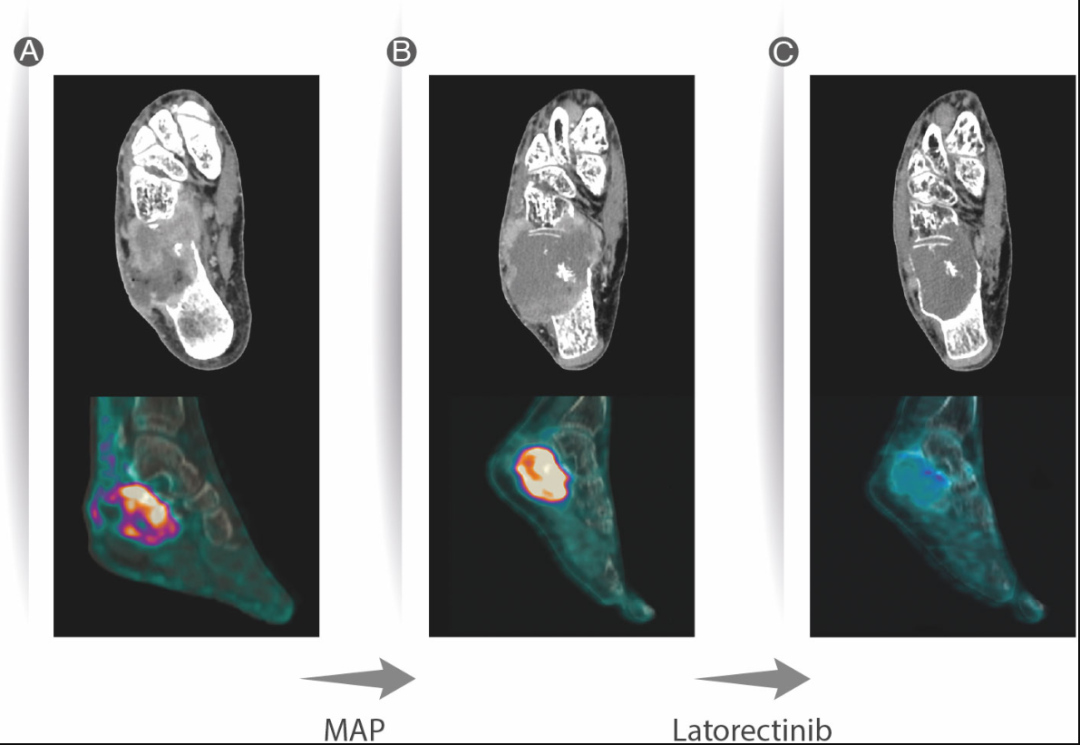
▲图1 影像学结果
患者接受了活检(图2)。形态学方面以及免疫组织化学和分子结构类似未分化的高级梭形细胞肉瘤(图3A,B)。肿瘤显示平滑肌肌动蛋白、MDM2(局灶性)和 pan-TRK呈阳性(图3C),而Caldesmon、CD31、CK AE1/AE3、Desmin、ERG、S100、SATB2、STAT6、H3F3A(G34V)、H3F3A(G34W)、H3F3A (G34R)、SS18-SSX、SSX、STAT6和CD34均为阴性。
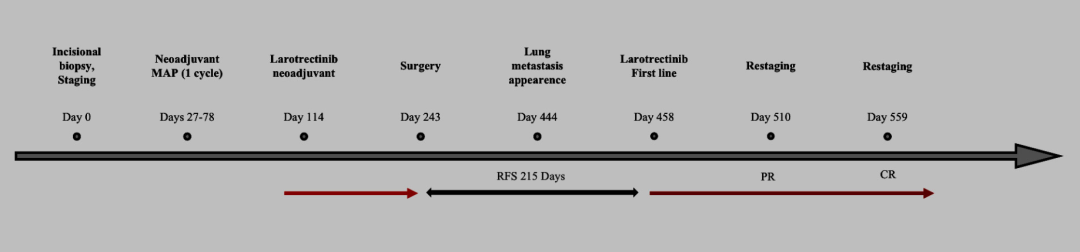
▲图2 患者治疗时间线
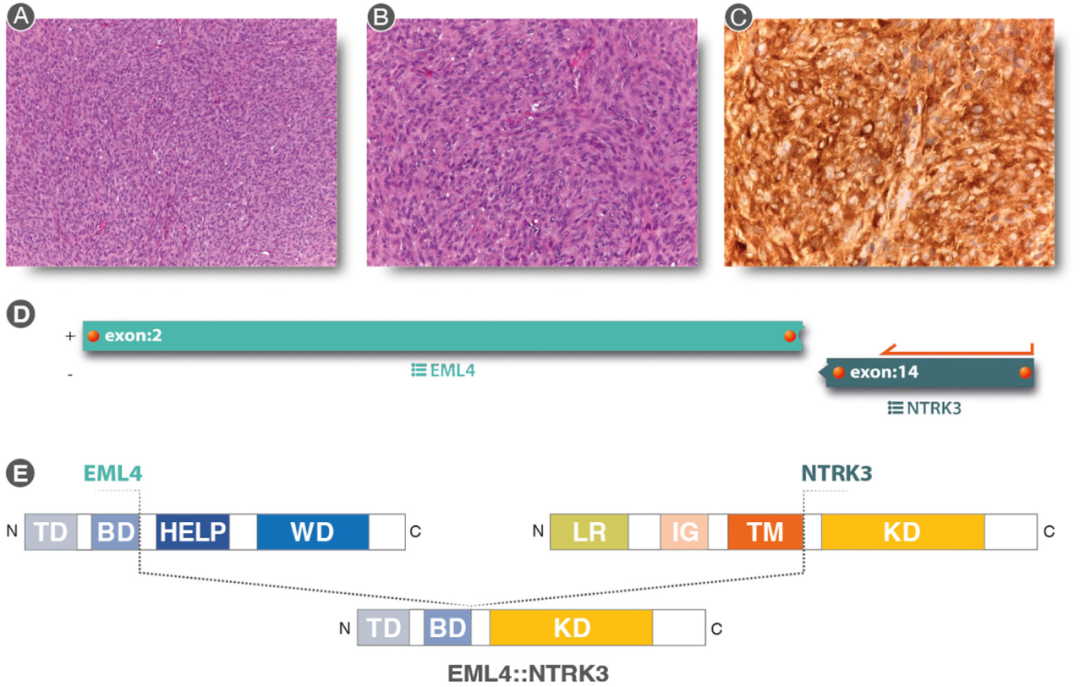
▲图3 病理检查结果、PCR结果和EML4::NTRK3重排示意图
由于pan-TRK阳性,进行了NGS测序。检测到EML4::NTRK3基因融合(断点chr2:42472827、chr15:88576276)(图3D、E)。尽管这种易位属于婴儿纤维肉瘤的范围,但考虑到患者已经成年以及发病位置,研究人员认为该肿瘤是NTRK重排的高级骨肉瘤。其它部位没有报告存在病理性FDG摄取。胸部CT扫描阴性。
经过多学科讨论后,肿瘤委员会决定开始使用甲氨蝶呤、阿霉素和顺铂(MAP)进行前期化疗,类似原发性传统高级别骨肉瘤方案。第 1 天给予甲氨蝶呤 12 g/㎡,随后在 48 小时连续输注(ci)顺铂 120 mg/㎡,并在第 13-16 天给予阿霉素 75 mg/㎡(24h,ci)。顺铂治疗 24 天后出现暂时性急性肾衰竭,使治疗过程变得复杂。
2 个月后的CT扫描显示病变扩大(60 × 63 mm vs. 53 × 51 mm),溶骨成分和骨外延伸均有增加,并累及神经血管束(图1B)。此外,患者还报告了疼痛(NRS等级从 3 级到 6 级)和肿胀的加深。经过多学科讨论后,提出采用拉罗替尼治疗的方案。基线PET-CT显示除了已知的跟骨病变(SUV 11.6),没有任何淋巴结或其他远端转移(图1B)。
2021 年 7 月至 11 月期间,患者口服拉罗替尼,剂量为 100 mg,每日两次。患者报告疼痛和肿胀逐渐减轻。2 个月后进行的PET-CT显示,根据PERCIST标准(实体瘤治疗疗效PET评价标准)对原发灶的代谢反应进行了评估(SUV 3.7 vs. 11.6),没有任何其它病理性FDG摄取迹象(图1C)。足部CT扫描显示部分缓解(基于RECIST v1.1标准),皮质上有硬化改变,而额外的隔室成分不再明显,实现完全缓解(图1C)。没有报告与药物相关的毒性。
治疗开始 4 个月后,患者接受了手术。对右腿进行了经胫骨截肢。术前CT扫描显示存在大量坏死成分。手术标本的组织病理学评估表明 80% 肿瘤坏死。经过多学科讨论后得出的结论是,由于没有可测量的病灶,尽管临床和影像学反应非常好,但不应建议使用拉罗替尼辅助治疗。随后患者开始了随访。7 个月后(2022 年 6月)的胸部CT扫描显示出现两个肺转移瘤(分别为 4.7 mm和 5.1 mm)。PET-CT扫描排除了其它远端转移,并确认了 2 个结节(由于尺寸小,未摄取FDG)。于是恢复拉罗替尼治疗(100 mg,BID),2 个月后新的胸部CT扫描显示两个肺结节尺寸减小。在 4 个月后的CT扫描中,肺部病变完全消失。目前,该患者再次接受拉罗替尼 14 个月后仍在继续接受治疗,没有任何疾病相关证据。图2显示了患者管理时间表。
讨 论
骨梭形细胞肉瘤是一种单一实体的间质肿瘤,通常作为高级别骨肉瘤进行治疗。NTRK重排梭形细胞肿瘤在最新的WHO软组织和骨肿瘤分类中被描述为一种发生在软组织中的新兴实体瘤。仅有故事性病例报道了原发性NTRK重排骨肿瘤。本文报告了一例不寻常的NTRK重排高级别梭形细胞肉瘤,主要发生在骨骼中,在化疗进展后对拉罗替尼有反应。
由于极其罕见,NTRK阳性骨肿瘤的患病率尚不清楚,报告之间的差异也可能取决于不同的检测方法。Lam等人最近报道,在通过pan-Trk筛选的一系列 354 个原发性骨肿瘤中,免疫组织化学染色的阳性率为 5%,但分子检测未发现到NTRK融合。另一份报告显示骨肉瘤患者中NTRK融合的患病率为 2.7%。Siozopoulou等人在 70 名骨和软组织肉瘤患者中发现了两例NTRK3融合,值得注意的是,这两名患者都患有梭形细胞肿瘤。
2018 年,在一项关键的 I-II 期试验结果之后,拉罗替尼成为FDA基于分子靶点而非癌症类型批准的第二款药物。恩曲替尼也在次年获得批准。在获批试验中,这两种泛癌种分子药物的使用在疾病反应和长期控制方面都取得了显著的成果。
研究人员以肉瘤患者为重点进行了查证。在一项儿科研究中拉罗替尼的缓解率为 93%,患者中位年龄为 4.5 岁(IQR 1.3-13.3),其中包括 47% 的婴儿纤维肉瘤、41% 的软组织肉瘤和 0% 骨肉瘤。在纳入两名肉瘤患者的实体瘤合并分析中,拉罗替尼缓解率高达 79%。
在本文病例中,拉罗替尼被用作新辅助治疗。虽然拉罗替尼作为新辅助药物用于新诊断的婴儿纤维肉瘤患者的 II 期试验已经启动,但没有关于新辅助治疗其他实体瘤和肉瘤的数据,尽管有关于软组织NTRK阳性患者的病例报告报道。
本文报告了一名接受化疗的NTRK+未分化高级别梭形细胞肉瘤患者的疾病的影像学和临床进展。由于化疗是骨肉瘤的标准治疗,并已用于其它梭形细胞骨肉瘤,但最大SUV仅减少了 40%。有趣的是,使用拉罗替尼后,最大SUV降低了 60% 以上,并且肿瘤明显缩小。
NTRK+骨肿瘤的治疗有几个悬而未决的问题:首先,靶向治疗在新辅助治疗中作为标准化疗的补充或替代会带来怎样的效果;其次,新辅助治疗的持续时间、肿瘤反应的评估以及影像学充分缓解该如何定义,从而避免切除手术;最后,尚不清楚手术后是否应进行辅助治疗,以及在晚期环境中实现完全缓解后应继续治疗多长时间。
考虑到目前的情况,研究人员认为可以考虑预先使用NTRK抑制剂进行新辅助治疗。新辅助治疗持续时间应根据代谢和影像学反应进行调整。在转移性环境中正在进行的拉罗替尼试验的长期结果可能会支持未来的治疗决策。
尽管携带NTRK基因融合的肉瘤患者很少见,但这些治疗发现证明了在特定病例中通过分子或免疫组织化学检测NTRK的合理性。本案例强调了多学科团队讨论以及分子委员会线上支持对于指导肿瘤治疗决策的重要性。
参考文献:
Palmerini E, Frega G, Gambarotti M, Frisoni T, Cesari M, Bazzocchi A, Miceli M, Donati DM, Fanti S, Nanni C, Benini S, Longhi A, Paioli A, Marrari A, Hakim R, Righi A and Ibrahim T (2023) NTRK rearranged sarcoma of the bone. Role for larotrectinib in the neoadjuvant setting of an ultra-rare tumor: a case report. Front. Oncol. 13:1252359. doi: 10.3389/fonc.2023.1252359

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#基因检测# #骨肉瘤# #拉罗替尼#
25