Alzheimer's & Dementia:纠正微管缺陷药物有望治疗阿尔兹海默症
2020-09-13 haibei MedSci原创
最近,研究人员在Alzheimer's & Dementia上发文,研究了脑穿透性MT稳定化合物CNDR-51657是否可以减少斑块相关的轴突萎缩和Aβ的释放。
阿尔茨海默病(AD)患者的大脑特点是存在由淀粉样β(Aβ)肽组成的细胞外衰老斑块,以及由tau蛋白形成的细胞内包裹体,后者通常被称为神经纤维缠结。形成斑块的Aβ肽是由β位APP切割酶(BACE)和γ-分泌酶对淀粉样前体蛋白(APP)进行蛋白切割后生成的。
已有的研究发现,APP和构成γ-分泌酶复合物内酶活性的presenilin(PS)蛋白的突变会导致了家族性AD的发生,这导致了 "淀粉样蛋白级联 "假说的提出。该假说假定Aβ斑块启动了一系列事件,导致AD疾病中的神经元丧失和认知障碍。
Aβ衰老斑块可能通过促进脑中tau病理学从最初的内皮层/海马区扩散到新皮质区,从而促进AD神经变性。值得注意的是,tau病理学的程度,而不是衰老斑块的负担,与AD认知状态相关,这与tau病理学导致AD神经变性一致。
衰老斑块如何增强tau病理学的分子机制在很大程度上是未知的。Tau通常是一种微管(MT)相关的蛋白质,被推测可以提供远端唇状区域中稳定的轴突MTs,同时也阻止MT被切断。
MTs在神经元中起着至关重要的作用,因为它们是细胞成分通过轴突运输过程沿轴突延伸运输的渠道。Tau在AD中变得高磷酸化,这促进其脱离MTs,并增加MT的动态性,也许会导致MT断裂,以及轴突运输的损害。减少tau与MTs的结合也可能影响参与轴突运输的分子马达的相互作用。
因此,tau的MT调节功能的损失,以及不溶性tau沉积物的形成,可能导致了在AD和相关的tau疾病,如Pick病,进行性核上性麻痹,和皮质基底变性,中观察到的神经元损失。

根据以上现象可以推测,脑渗透性MT稳定化合物可以使tau病理的小鼠模型中的MT和轴突运输正常化,从而减少神经元损失,降低tau病理。在与Aβ斑块相邻的萎缩轴突中也观察到MT功能障碍,导致淀粉样前体蛋白(APP)和BACE1的积累,并有可能增强局部Aβ的生成。
最近,研究人员在Alzheimer's & Dementia上发文,研究了脑穿透性MT稳定化合物CNDR-51657是否可以减少斑块相关的轴突萎缩和Aβ的释放。其使用的模型是可以形成丰富的Aβ斑块的5XFAD小鼠。
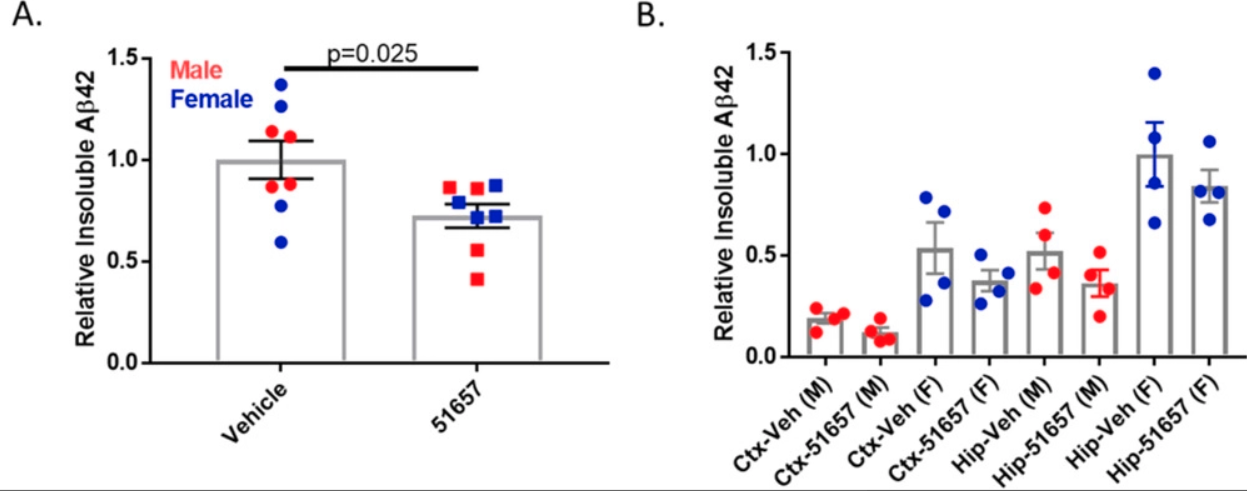

研究人员给1.5月龄的雄性和雌性5XFAD小鼠施用CNDR-51657,发现连续给药4周或7周可以减少可溶性脑Aβ的量,与APP和BACE1水平降低相一致,并进一步导致不溶性Aβ沉积物形成减少。
这些数据表明了一个恶性循环,初始Aβ斑块的形成导致附近轴突的MT破坏,导致APP和BACE1的局部积累,促进了额外的Aβ生成和斑块沉积。MT稳定化合物能够减弱这种循环,也能减少tau与MTs结合缺陷导致的损伤,这表明这种类型的分子有希望成为潜在的AD治疗药物。
原始出处:
Yuemang Yao et al. Correction of microtubule defects within Aβ plaque‐associated dystrophic axons results in lowered Aβ release and plaque deposition. Alzheimer's & Dementia (2020). DOI: https://doi.org/10.1002/alz.12144
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#dementia#
51
#阿尔兹海默#
41