Nat Rev Drug Discov:瞄准下一个KRAS突变
2023-02-14 精准药物 精准药物 发表于上海
众所周知KRAS是长久以来追求但又难成药的靶点,同样众所周知近年来靶向KRAS有了突破性的进展,并分别于前年及去年各上市了一个KRAS-G12C抑制剂。
以下来源于近日Nat Rev Drug Discov一篇展望文章,以及Mirati公司之前披露的presentation,此外也夹杂一些个人观点。
众所周知KRAS是长久以来追求但又难成药的靶点,同样众所周知近年来靶向KRAS有了突破性的进展,并分别于前年及去年各上市了一个KRAS-G12C抑制剂。
KRAS-G12C由于有一个可共价的cysteine,相对容易靶向,那其它突变呢?相信大家心中也有答案,下一个很可能是G12D,pan-KRAS及其它某些突变,也是有可能的。
图1是近日Nat Rev Drug Discov文章总结的一些处于临床或临床前的KRAS抑制剂(或degrader及molecular glue),以靶向KRAS-G12D为主,也包括G13C或pan-KRAS抑制剂,及两个新的靶向KRAS-on的G12C抑制剂。
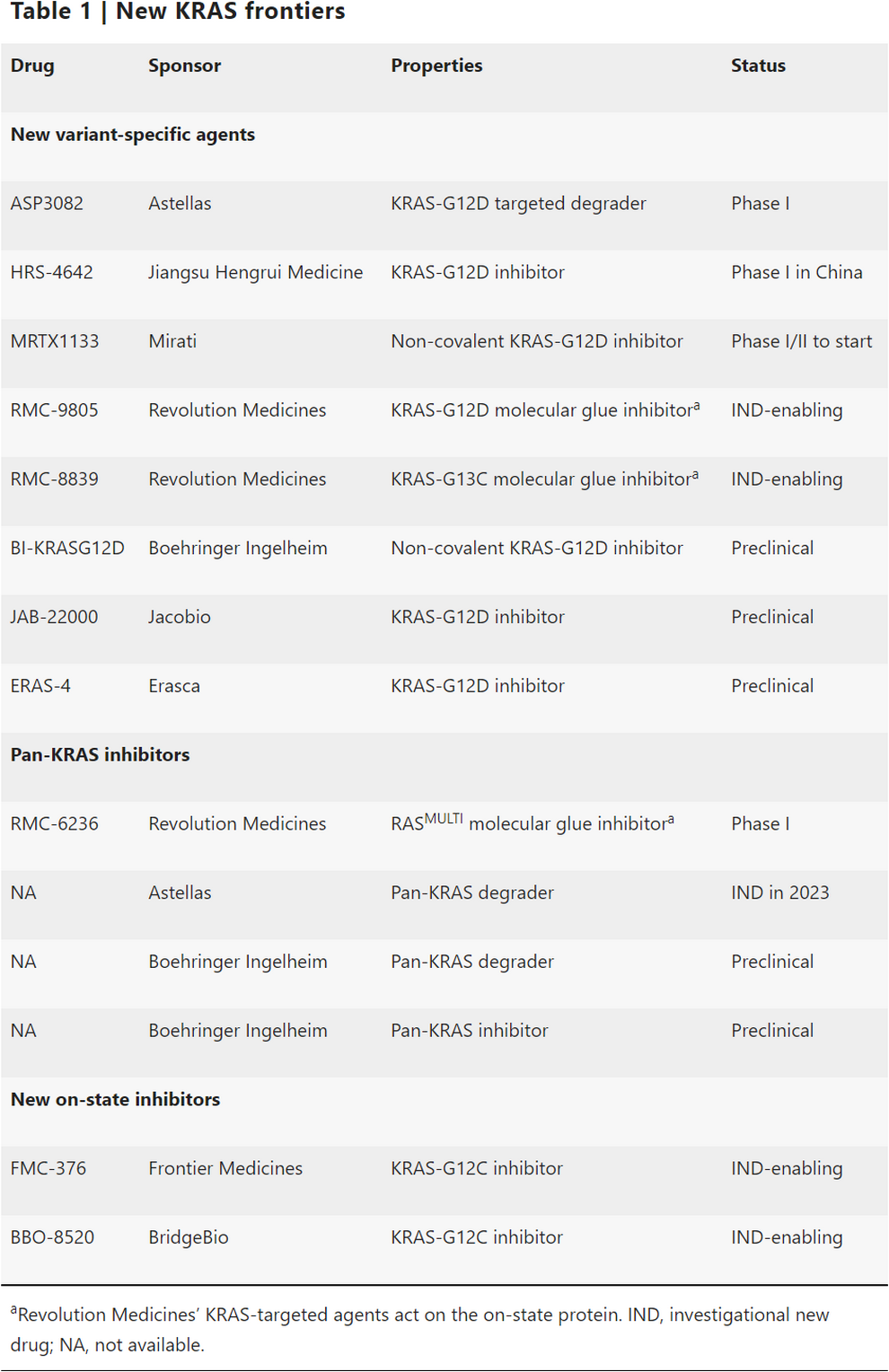
图1 文章总结的代表性前沿KRAS分子
提到KRAS-G12D抑制剂,不得不提Mirati公司的MRTX1133,它应该是最早报道的、活性足够推上临床的G12D抑制剂。而且不管事实上有没有借鉴关系,单从结构来看,它是后来几乎所有KRAS-G12D SWII pocket抑制剂的“祖先”;如果有与它明显不同、而活性足够好的分子,还望告知。
KRAS-G12D抑制剂首先难在活性上,尽管已经有优化过的G12C抑制剂骨架可供借鉴。但如图2所示,这仍需在此基础上提高至少上万倍的活性。
图2左是Mirati去年刚上市的G12C抑制剂,活性已经不错,但单看Ki也只有3.7 μM (对G12C)。去掉warhead,通过哌嗪引入静电吸引,Kd则仅有19 μM (对G12D),但总算有一定希望。
不过考虑到这已经是在比较优势的骨架上改动,想要继续提高上万倍甚至更多,恐怕还是让人觉得前路漫漫。另外右侧分子去掉了哌嗪环上的乙腈基,尽管它在左侧G12C抑制剂中很重要,但在右侧G12D分子中反而降低活性。
简而言之,Mirati公司研究人员通过对他们的G12C抑制剂全面改造,保留骨架但每一部分都升级优化,终于得到活性非常不错的MRTX1133 (如图3、图4所示)。每一处改造都很重要,但各自单独都不足以达到理想的活性。
考虑到SWII pocket本身druggability并不是很好,能够达到这种活性,可以认为分子已经非常优化。这可能也是后续各家公司都很难跳出这一模板分子框架的原因之一,Mirati自己也没能找到一个兼顾活性与口服利用度的分子,最终还是通过制剂手段解决。
具体分子优化过程就不谈了,不是这里主要内容,而且应该之前也都看过了。
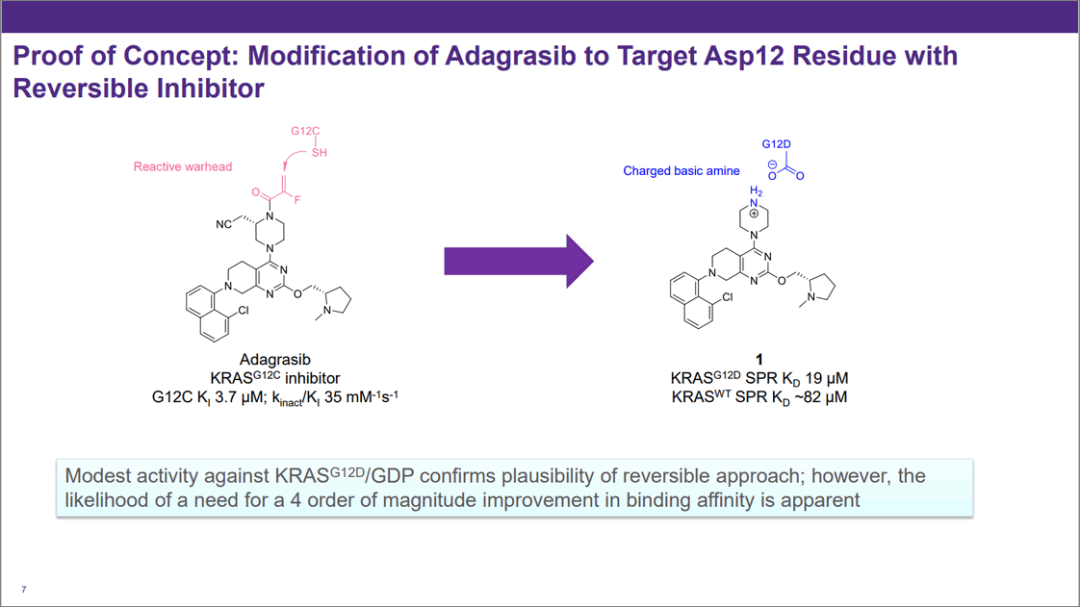

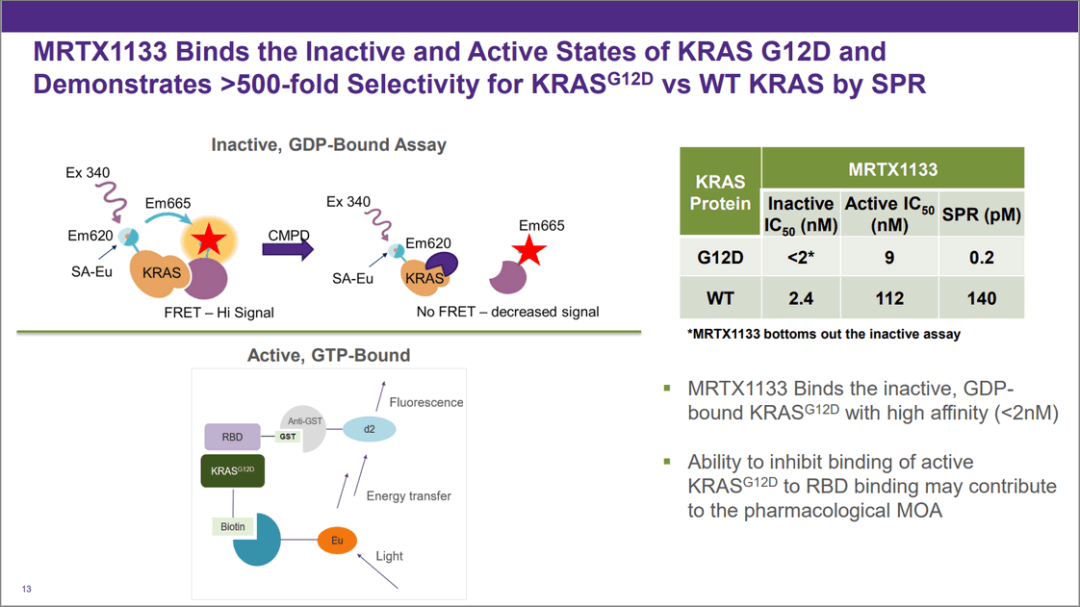
图2、3、4 Mirati公司FIC G12D抑制剂的优化过程示意
如前所述,由于靶点的难度,Mirati公司并未能在分子结构角度同时解决活性与口服利用度,好在近期他们公布通过制剂方面的进展,已经可以实现口服,并将很快进入临床试验。
考虑到G12D比G12C更大的突变比例,而且包括很大比例的胰腺癌患者,还是很令人期待。
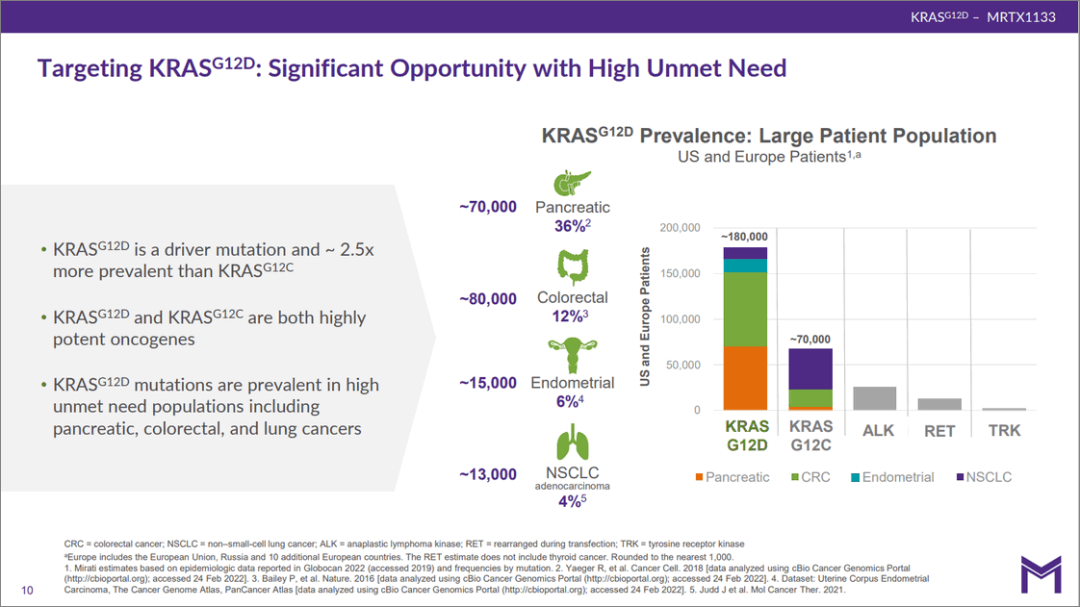
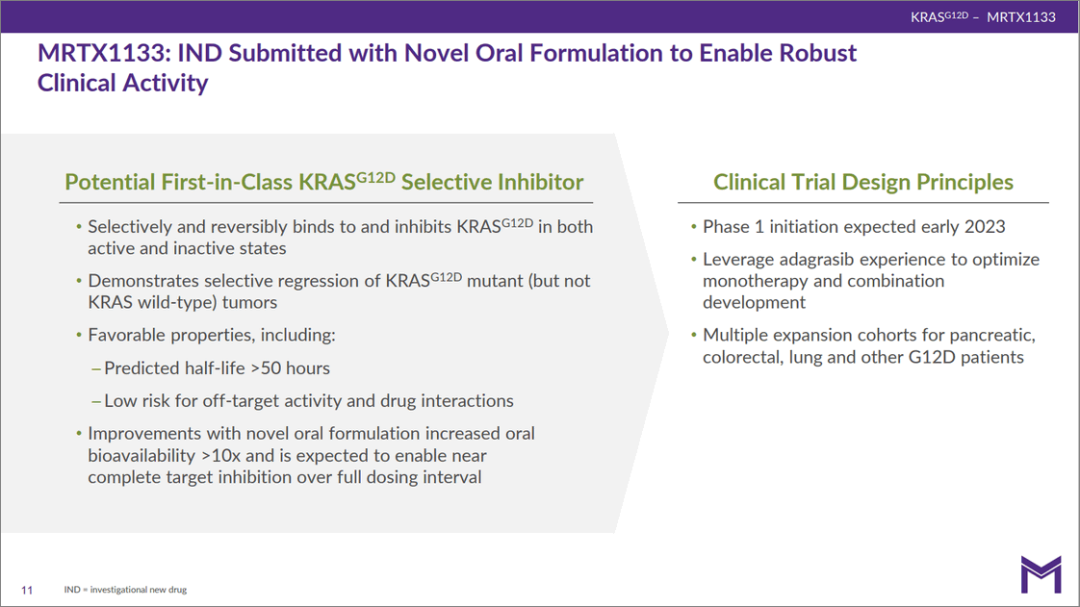
图5、6 Mirati G12D抑制剂即将进入临床
图1其它SWII口袋G12D抑制剂,虽然大多未披露结构,但从专利分子看,或者与MRTX1133很接近,或者保留1133关键部分比如桥环哌嗪,同时借鉴其它G12C抑制剂优势片段。有的看起来是在细微处找自己的IP空间,有的改动大一些,但实则是套用之前G12C的经验,前些天还看到一个关大环的分子,比较有意思,IP应该不错,但仍是在1133或相似分子的基础上。当然也有分子可能是独立发展来的。
另外是G12D degrader,比如安斯泰来,他们的分子做抑制剂嫌活性不够,做成degrader,虽然牺牲了口服(静脉注射),但三周给药一次也还可以。结构没有公布,但应该是PROTAC,且连接点位置大概相当于1133并环F取代那里,并非显而易见,这可能也跟他们G12C的经验有关。
Mirati也探索过PROTAC,但可能因为抑制剂已经足够强,degrader未见明显优势(且估计更难口服),故没有选择。顺便一提,MRTX1133的半衰期也很长(图6)。
再谈谈pan-KRAS抑制剂。
从1133数据其实已经能看出囊括wildtype的可能性(图4),1133对WT是有一定抑制的,尽管没有对G12D那么好。这应该是因为对分子其它部分优化的结果,因此在其基础上继续调整优化,是可能进一步提高对WT及部分其它突变体的活性的,尽管未必能够达到1133对G12D的活性水平,这在一些专利中已经有报道。
那对WT的抑制是好是坏呢?目前还难有定论。但据文章报道,囊括对WT的抑制可能是不坏甚至是好的 (综合疗效与副作用的考量),即pan-KRAS抑制剂是可行或者可以尝试的。但与此同时,对还囊括NRAS、HRAS的pan-RAS抑制剂,仍担忧其副作用。
另外一提,图1表中BI公司的pan-KRAS抑制剂及degrader,不知是不是基于他们自己开发的SWI/SWII口袋那个系列。
最后是Revolution公司的molecular glue系列,包括G12D、G13C及pan-RAS,当然也包括G12C,大致原理就是召集另一个细胞内富集的蛋白与KRAS结合(分子胶),通过空间位阻阻断KRAS与下游蛋白比如RAF的结合。除Revolution之外,图1还有两个较新的针对KRAS-on的G12C抑制剂,不过文章提及很少,没什么细节内容。
此外还有去年Shokat组报道的共价KRAS-G12S及G12R抑制剂,很有意思,但这两个突变占比小,分子也早期,离临床估计还远。
The KRAS crowd targets its next cancer mutations, Nat Rev Drug Discov, Jan 23, 2023
Mirati Therapeutics presentation, ENA conference, Oct 7-10, 2021
Mirati Therapeutics presentation, 41st JPM conference, Jan 9, 2023
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言