度伐利尤单抗是一种选择性、高亲和力、人源性IgG1单克隆抗体,能阻断程序性死亡配体-1(PD-L1)与程序性死亡蛋白-1(PD-1)及CD80的结合,从而使得T细胞能够识别和杀灭肿瘤细胞。小编整理了度伐利尤单抗在非小细胞肺癌(Non Small Cell Lung Cancer,NSCLC)和小细胞肺癌(Small Cell Lung Cancer,SCLC)中的系列研究,有助于我们更深入的认识PD-L1抗体—度伐利尤单抗。
系列研究概要
非小细胞肺癌
新辅助免疫治疗
1. AEGEAN研究:I药+化疗 vs 化疗,EFS达到主要终点,具体数据暂未公布
同步放化疗后巩固治疗
2. PACIFIC研究:改变不可切除的Ⅲ期治疗模式,5年OS率高达42.9%
一线治疗
3. POSEIDON研究:一线,III期,度伐利尤单抗±tremelimumab+化疗,TTD更长
4. MYSTIC研究:Ⅲ期,双免 VS 化疗,一线治疗、OS无差异
三线治疗
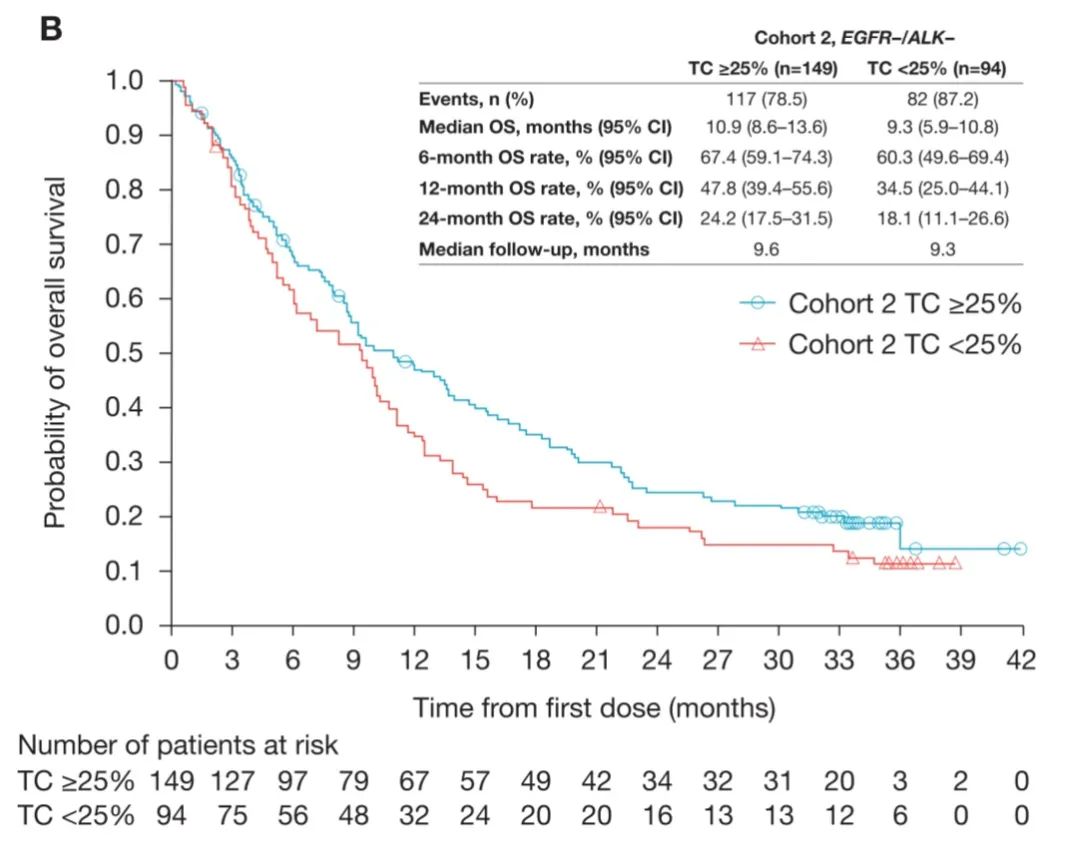
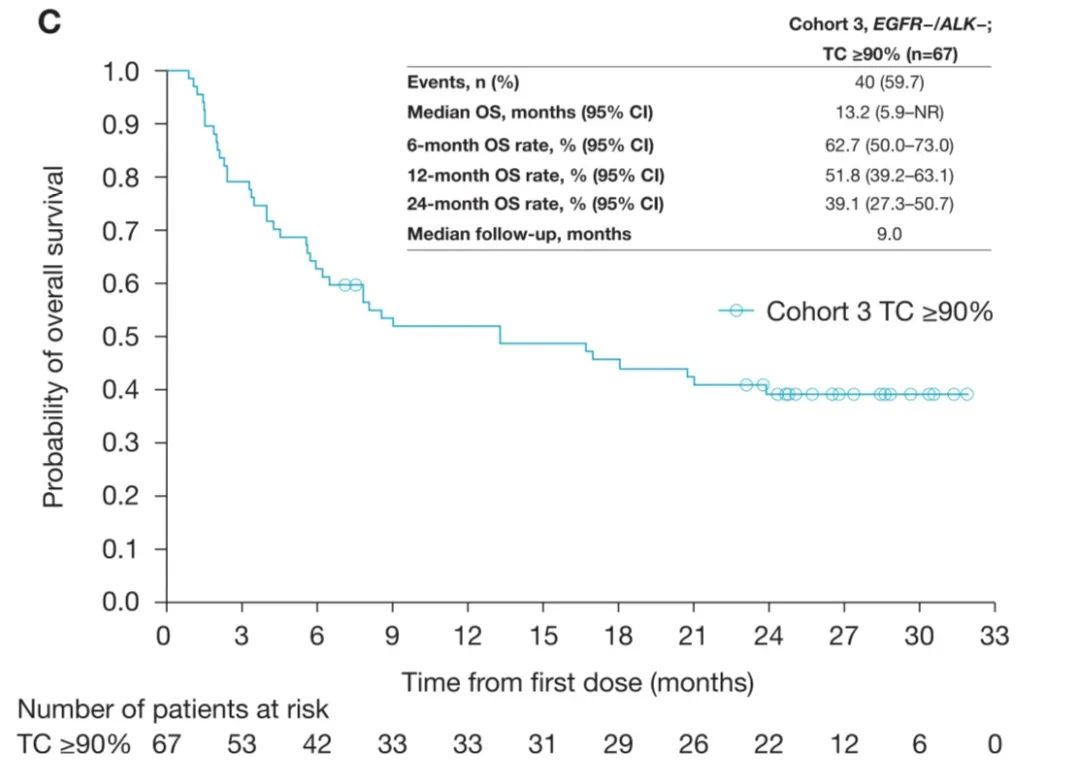
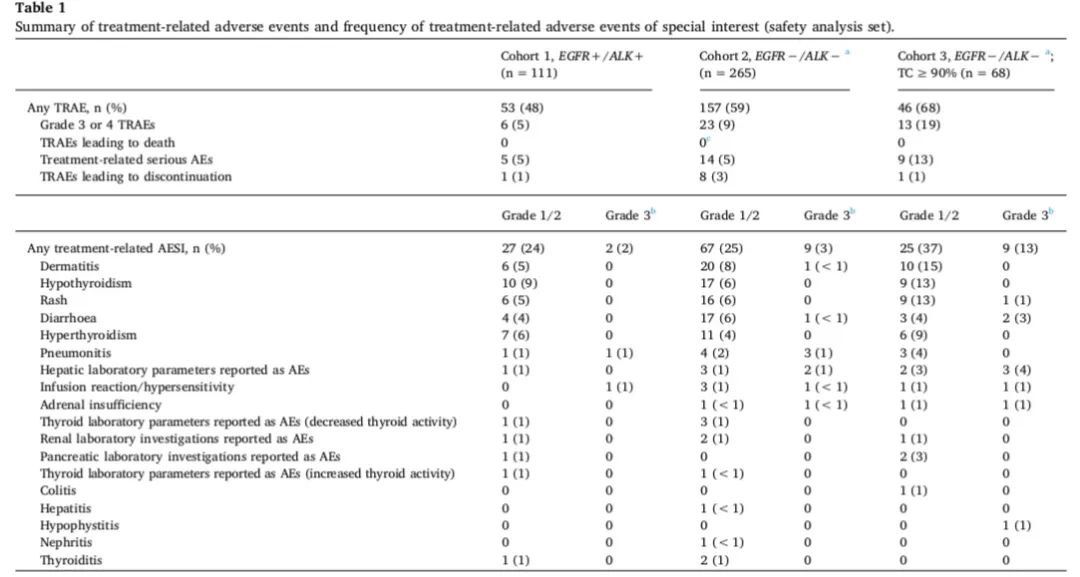
5. ATLANTIC研究:无论是否携带EGFR/ALK突变,免疫治疗显疗效
小细胞肺癌
一线治疗
6. CASPIAN研究:Ⅲ期,I药+化疗 VS 化疗,生存获益
临床上,大约1/3的NSCLC患者在确诊时的分期为Ⅲ期、局部晚期疾病。对体力状况良好,不可手术切除的Ⅲ期NSCLC患者而言,标准治疗方法是以铂类为基础的双药化疗联合同步放疗(化放疗)。然而,接受化放疗的患者中位无进展生存期较短(大约为8个月),并且只有15%的患者达到5年生存期。多年来,对此类患者的治疗并未取得重大进展。[2015年免疫药物出现后,再次激发了肺癌专家们的希望,他们发现,放疗可以通过促进抗原的扩增和被识别以及诱导CD8+T细胞浸润等机理增加宿主抗肿瘤免疫反应。同时利用免疫长效低毒的药物特性,就此设计出同步放化疗完成后序贯PDL1单抗免疫巩固的新型治疗模式!掀起了全球针对III期不可手术肺癌的随机对照III期PACIFIC研究。PACIFIC研究是首个评估免疫检查点抑制剂用于不可切除的Ⅲ期NSCLC患者疗效的随机对照Ⅲ期临床研究。]
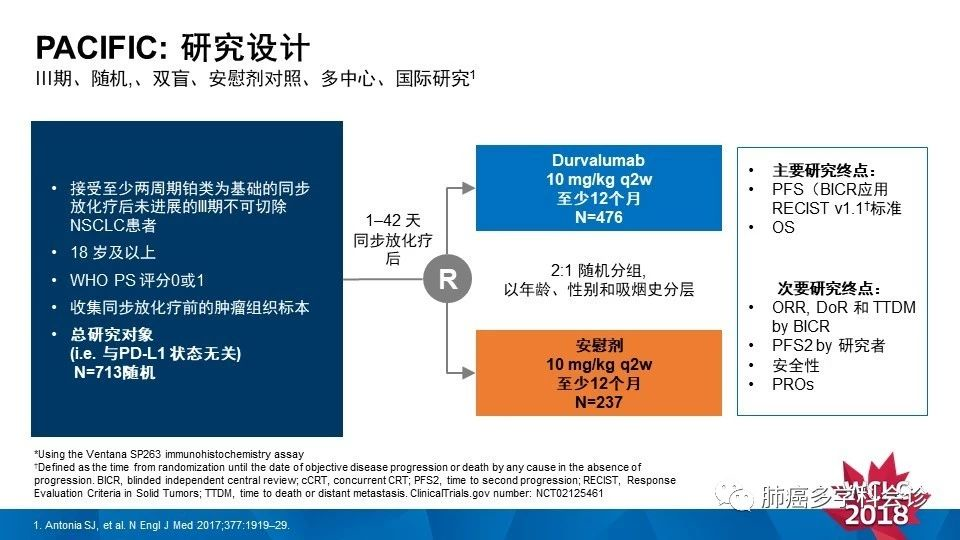
研究设计

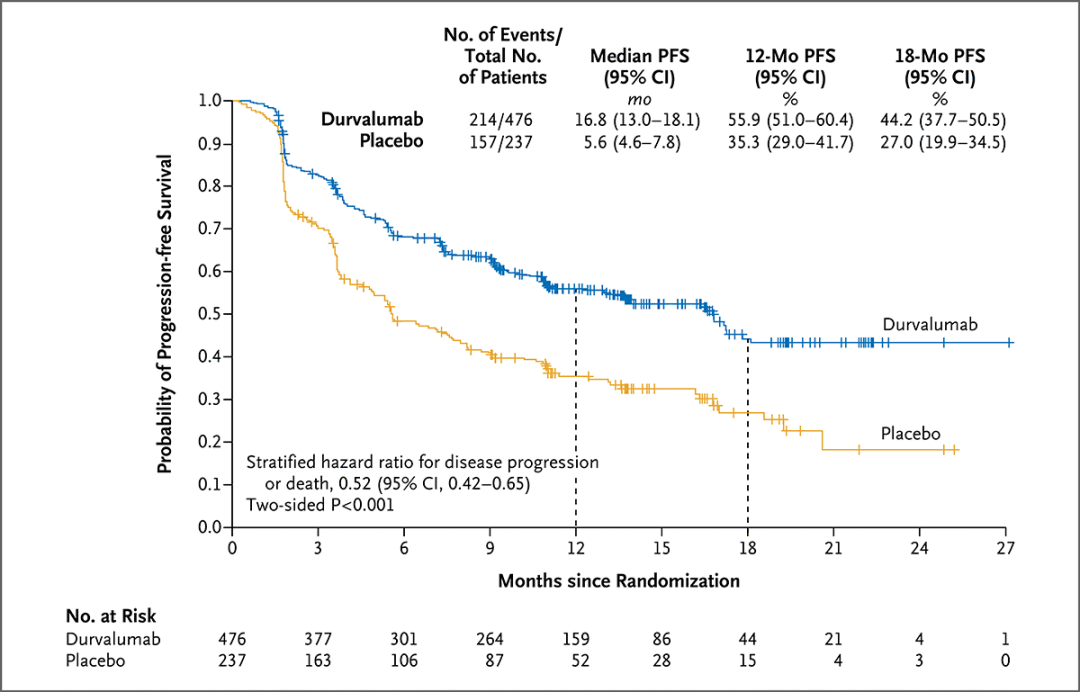
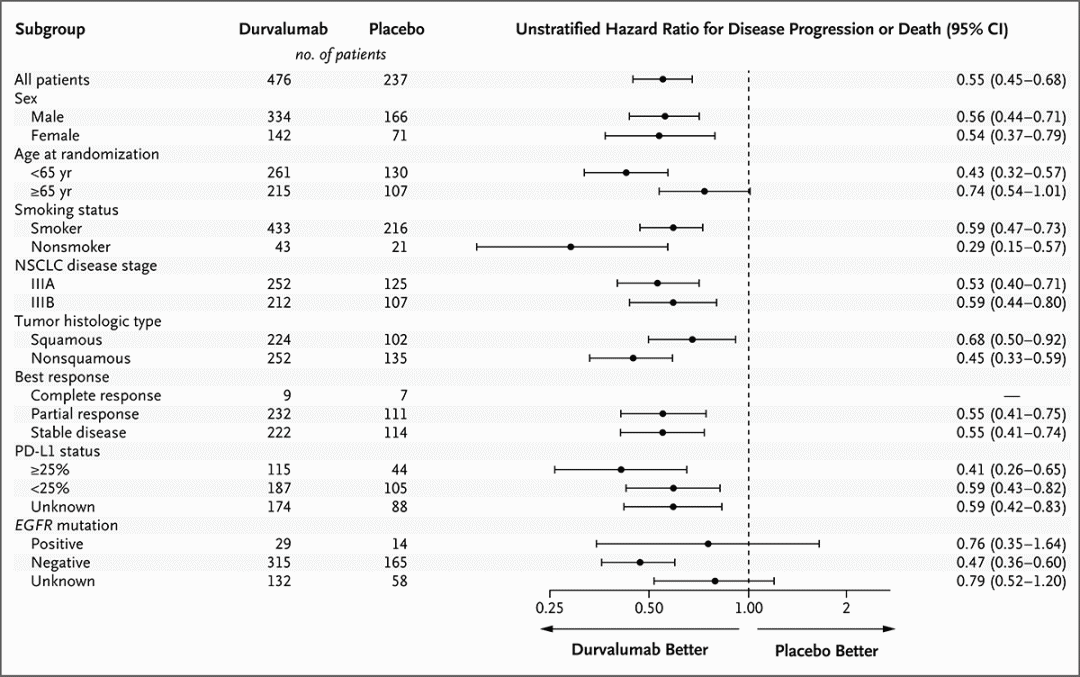
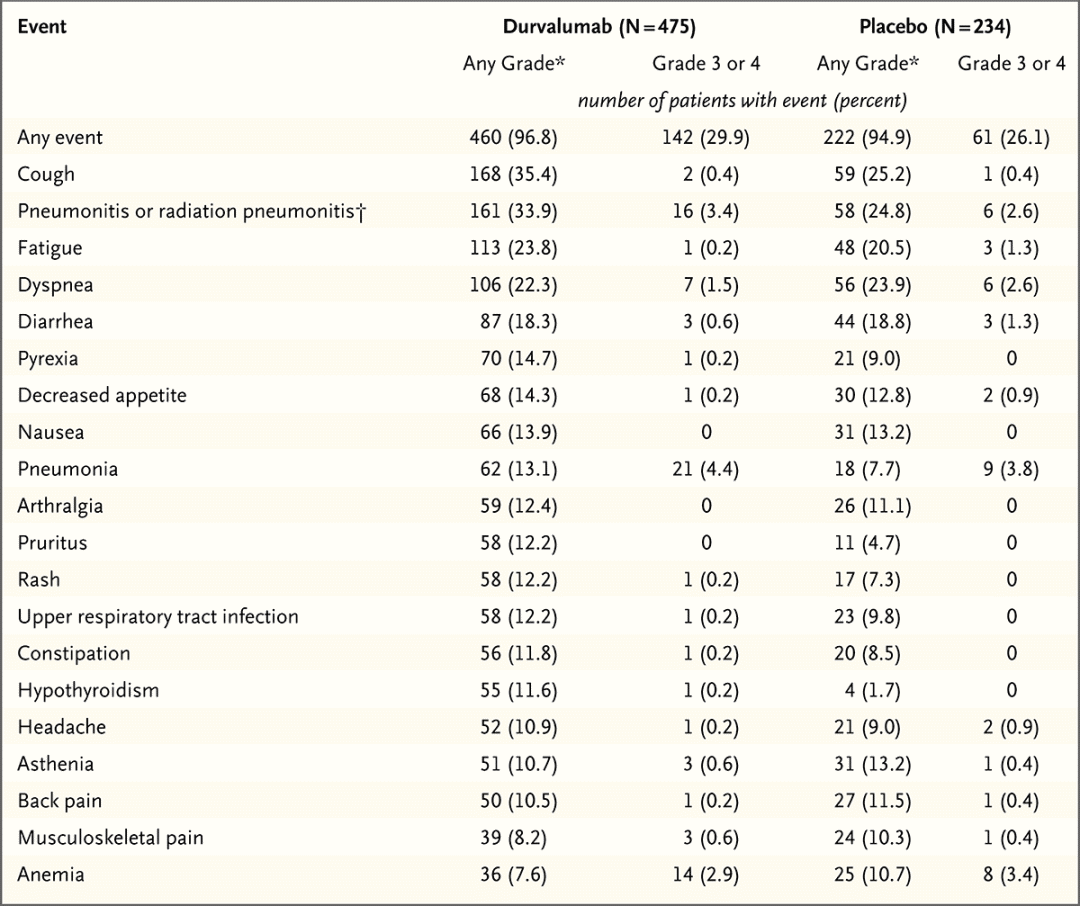


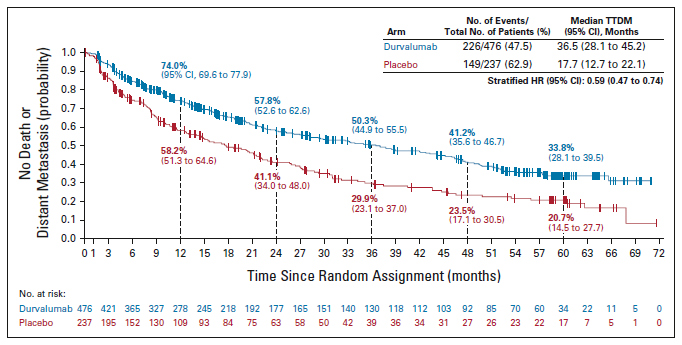
2021年ASCO大会进一步公布5年随访结果,并发表于《JCO》。结果显示:截至2021年1月11日(中位随访时间为34.2个月;范围为0.2-74.7个月),同步放化疗后度伐利尤单抗巩固治疗 vs. 安慰剂,中位OS 47.5月 vs. 29.1月(HR=0.72,95%CI 0.59-0.89),5年OS率42.9% vs. 33.4%。中位PFS 16.9月 vs 5.6月 (HR=0.55,95%CI 0.45-0.68),5年PFS率33.1% vs. 19.0%。PACIFIC5年随访数据的更新,证明了PACIFIC方案具有很好的OS以及PFS益处。[4-5]
机遇与挑战并存,希望与荣耀同在丨不可切除局部晚期/转移性NSCLC的起始治疗策略
POSEIDON研究:在III期POSEIDON研究中,与单独化疗相比,一线度伐利尤单抗+化疗显著改善了mNSCLC患者的PFS,OS改善具有积极趋势但未达到统计学显著性。与化疗相比,一线tremelimumab+度伐利尤单抗+化疗显示PFS和OS出现统计学显著和有临床意义的改善。本研究描述了tremelimumab+度伐利尤单抗+化疗和度伐利尤单抗+化疗与单独化疗相比的患者报告结局分析。EGFR/ALK野生型mNSCLC患者(n=1013)随机(1:1:1)分配至一线tremelimumab75mg+度伐利尤单抗1500mg+铂类化疗q3w治疗至多4个周期后,度伐利尤单抗 q4w治疗直至疾病进展,化疗后(第16周)再给予一剂tremelimumab;度伐利尤单抗+化疗q3w治疗至多4个周期后,度伐利尤单抗q4w治疗直至疾病进展;或化疗q3w治疗至多6个周期后。使用EORTC QLQ-C30/LC13将总体健康状况/QoL、功能和症状作为次要终点进行评估。使用Cox比例风险模型的分层对数秩检验评估至恶化时间(TTD),通过Kaplan-Meier方法估计中位数,通过logistic回归评估改善率。
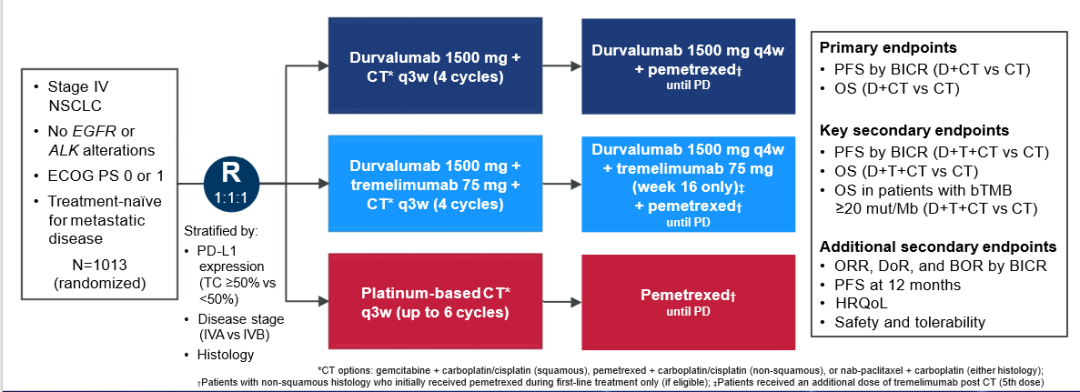
研究结果:截至2021年3月12日,分别有338、338和337例患者随机接受tremelimumab+度伐利尤单抗+化疗、度伐利尤单抗+化疗和化疗。对于tremelimumab+度伐利尤单抗+化疗、度伐利尤单抗+化疗和化疗组,C30和LC13的依从性分别为60%至88周、64周和24周。各治疗组的基线总体健康状况/QoL、功能和症状评分基本相似。HR表明,在几乎所有患者报告结局中,tremelimumab+度伐利尤单抗+化疗和度伐利尤单抗+化疗的TTD均长于化疗,包括预先规定的关注症状/领域(度伐利尤单抗+化疗与化疗相比,食欲减退[C30]除外)。tremelimumab+度伐利尤单抗+化疗和度伐利尤单抗+化疗组的患者报告结局(包括预先规定的症状/关注领域)改善率高于单独化疗组。

在化疗基础上加用度伐利尤单抗(+/-T)可改善mNSCLC患者的疗效,同时延缓健康相关QoL的恶化。与化疗组患者相比,tremelimumab+度伐利尤单抗+ 化疗组和度伐利尤单抗+化疗组患者的TTD更长,总体健康状况/QoL、功能和症状的改善率更高。(2022ELCC会议)
MYSTIC研究[6]是一项随机、开放标签的国际多中心III期临床研究,旨在探索durvalumab单药(D,PD-L1抑制剂)或联合tremelimumab(T,CTLA-4抑制剂)与标准化疗(CT)在局部晚期或转移性且EGFR和ALK野生型非小细胞肺癌(NSCLC)一线治疗的有效性与安全性。三组患者按照1:1:1的比例分为D (20 mg/kg,q4w);D (20 mg/kg,q4w) + T (1 mg/kg q4w,应用四周期)或CT组。预设的亚组分析包括年龄、性别、种族、病理类型、吸烟状态、PD-L1表达水平,事后分析包括PS评分状态。
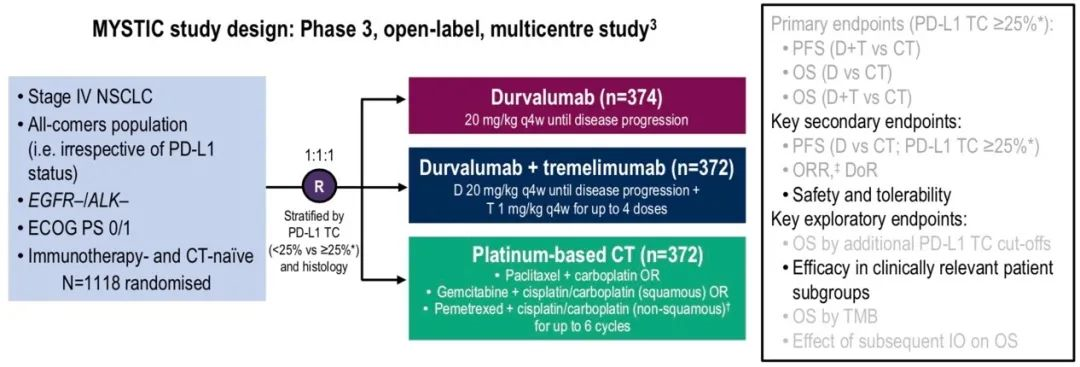
研究结果:自2015年7月21日至2016年6月8日,共入组1891例符合条件患者,其中1118例患者随机分配至3个治疗组。在PD-L1≥25%人群中,组间临床特征分布均衡。
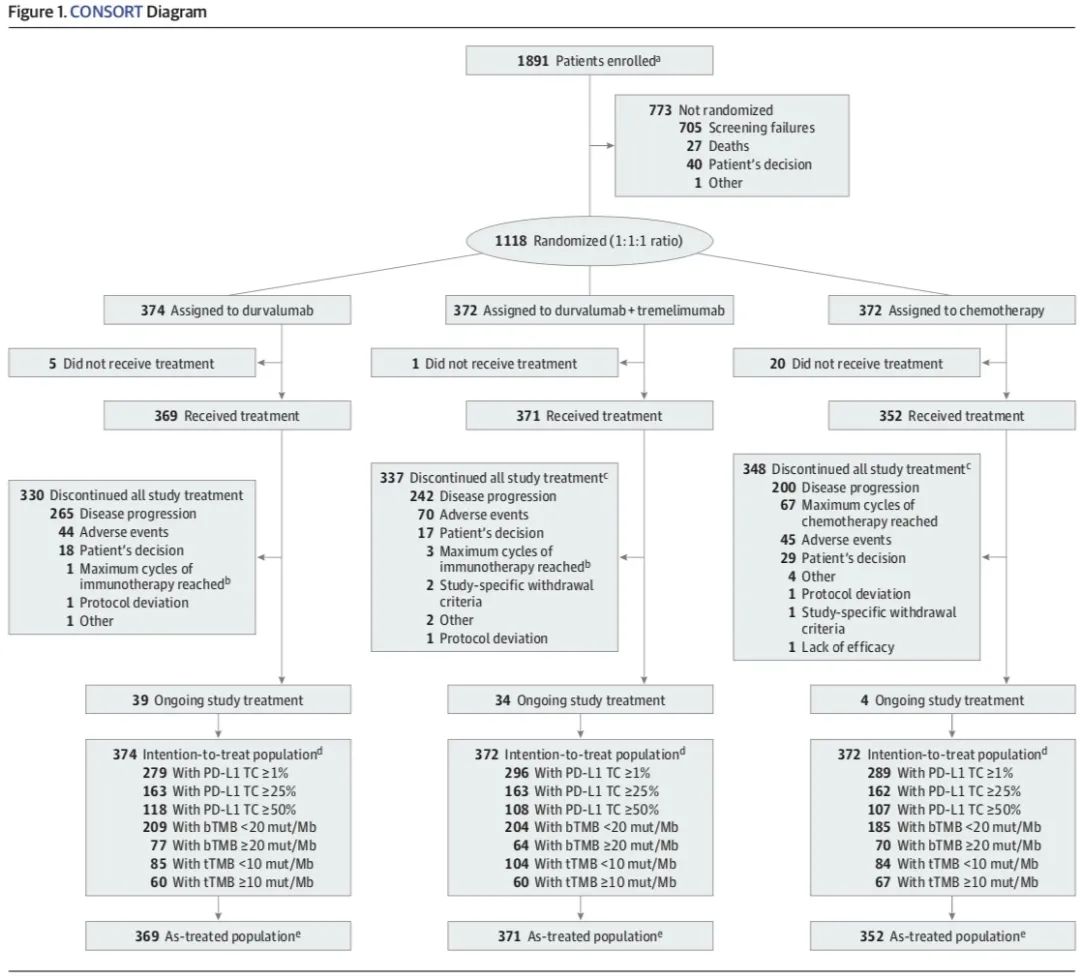

截止2018年10月,中位随访30.2个月,未看到两种免疫治疗模式分别和化疗相比能显著改善OS(16.3月 vs. 12.9月;11.9月 vs. 12.9月),但免疫治疗组2年生存率显著优于传统化疗(38.3%/35.4% vs. 22.7%)。
截止2017年1月,中位随访时间10.6月后,无论是次要终点对比度伐利尤单药和化疗(4.7月 vs. 5.4月)抑或主要终点双免疫联合对比化疗(3.9月 vs. 5.4月)均未见PFS显著改善。但两组免疫治疗模式1年PFS率均高于传统化疗(32.3%/25.8% vs. 14.3%)。
ORR在免疫单药、双免疫联合治疗、化疗组中分别为35.6%,34.4%及37.7%,化疗组中位缓解持续时间为4.4月,免疫组未达到。
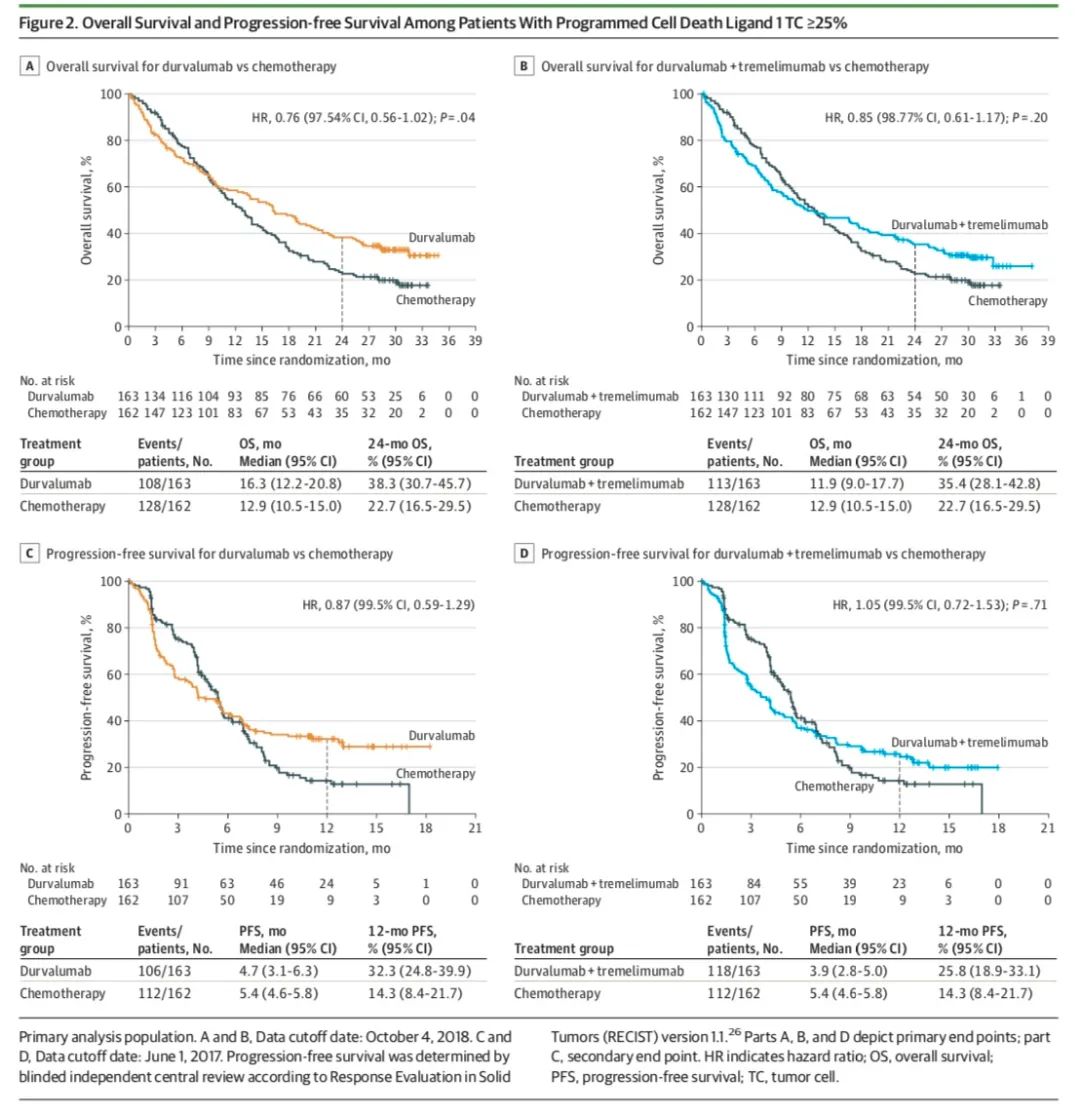
OS、PFS
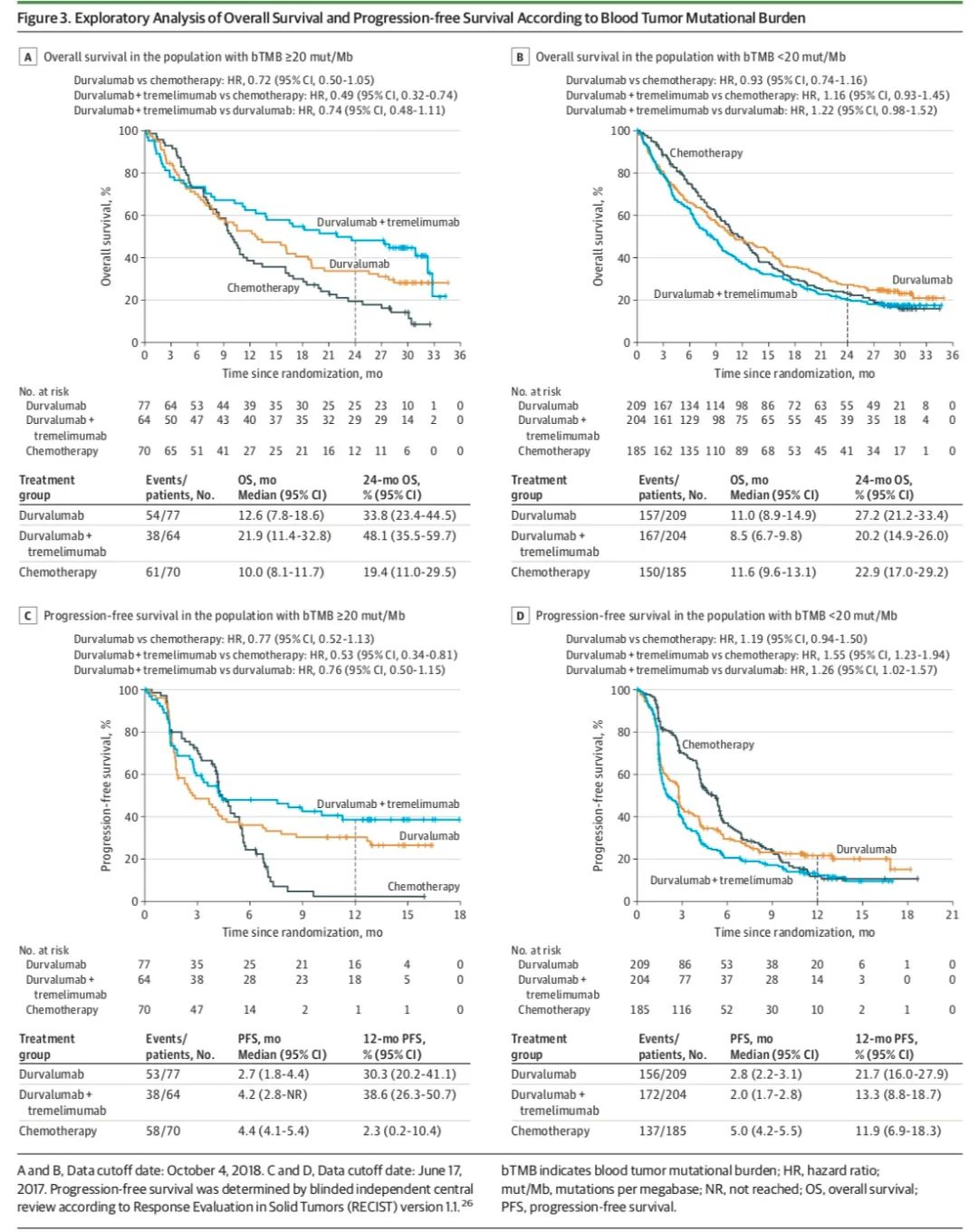
探索性分析
探索性分析部分中,有809例患者有可评估血浆TMB(bTMB),460例患者具有可评估组织TMB(tTMB)。其中针对高bTMB和PD-L1阳性表达未见明显相关性,与既往研究结果类似提示TMB可以作为独立于PD-L1表达预测生物标志物[7]。
在高bTMB(≥20mut/Mb)亚组中,度伐利尤单抗联合Tremelimumab较度伐利尤单抗和化疗显示出显著OS获益(21.9月 vs. 12.6月 vs. 10月),双药免疫联合2年OS率达到48.1%,而化疗组仅为19.4%,同样在PFS及ORR也观察到双药免疫联合较传统化疗的获益,但在低bTMB(<20mut/Mb)亚组中,双药免疫联合治疗未见OS改善。以10mut/Mb作为tTMB界值,也观察到高tTMB亚组中双药免疫联合的OS改善,但需要注意的是在高bTMB或tTMB组中均存在较低bTMB/tTMB组更高吸烟人群和鳞癌比例,后者可能是潜在临床疗效预测因素。
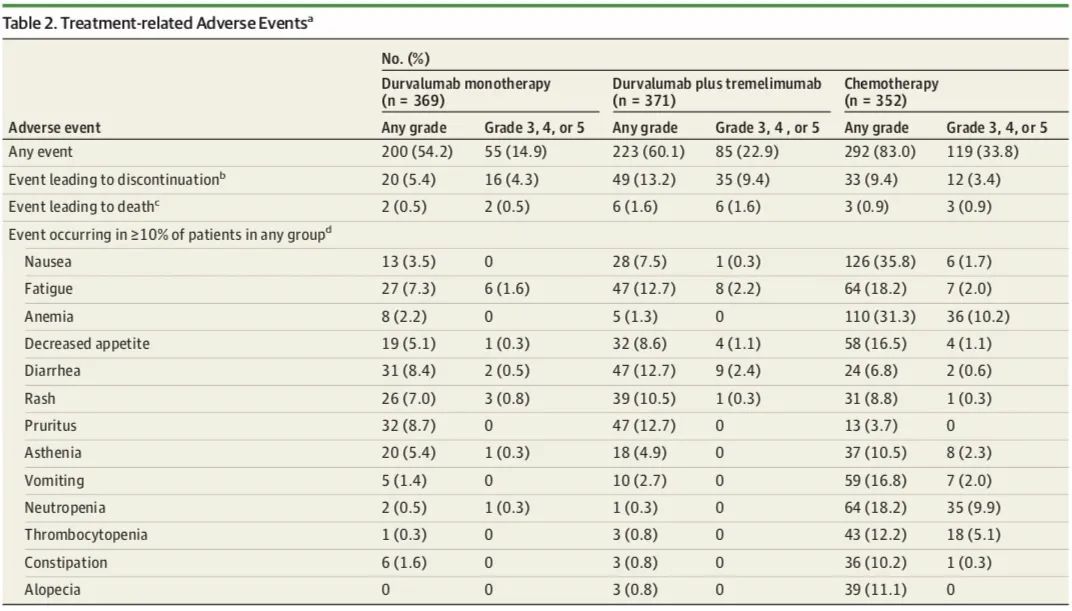
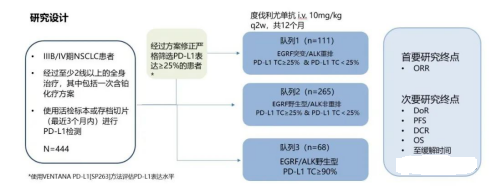
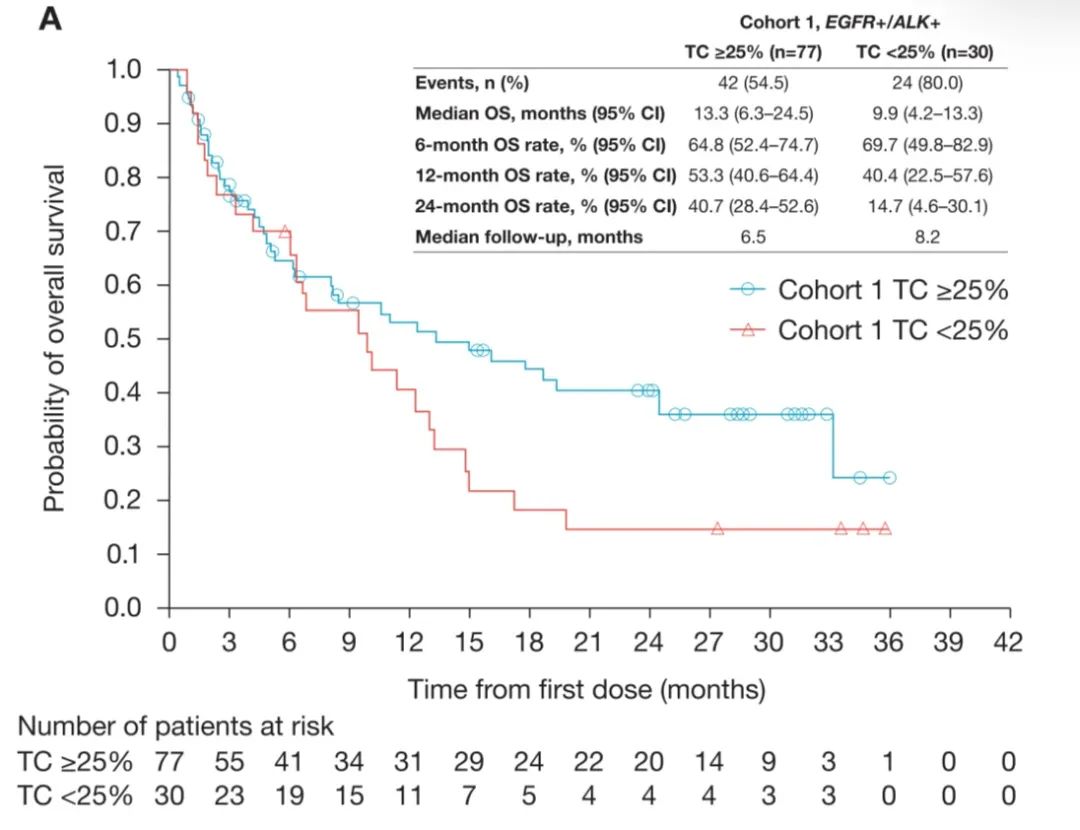
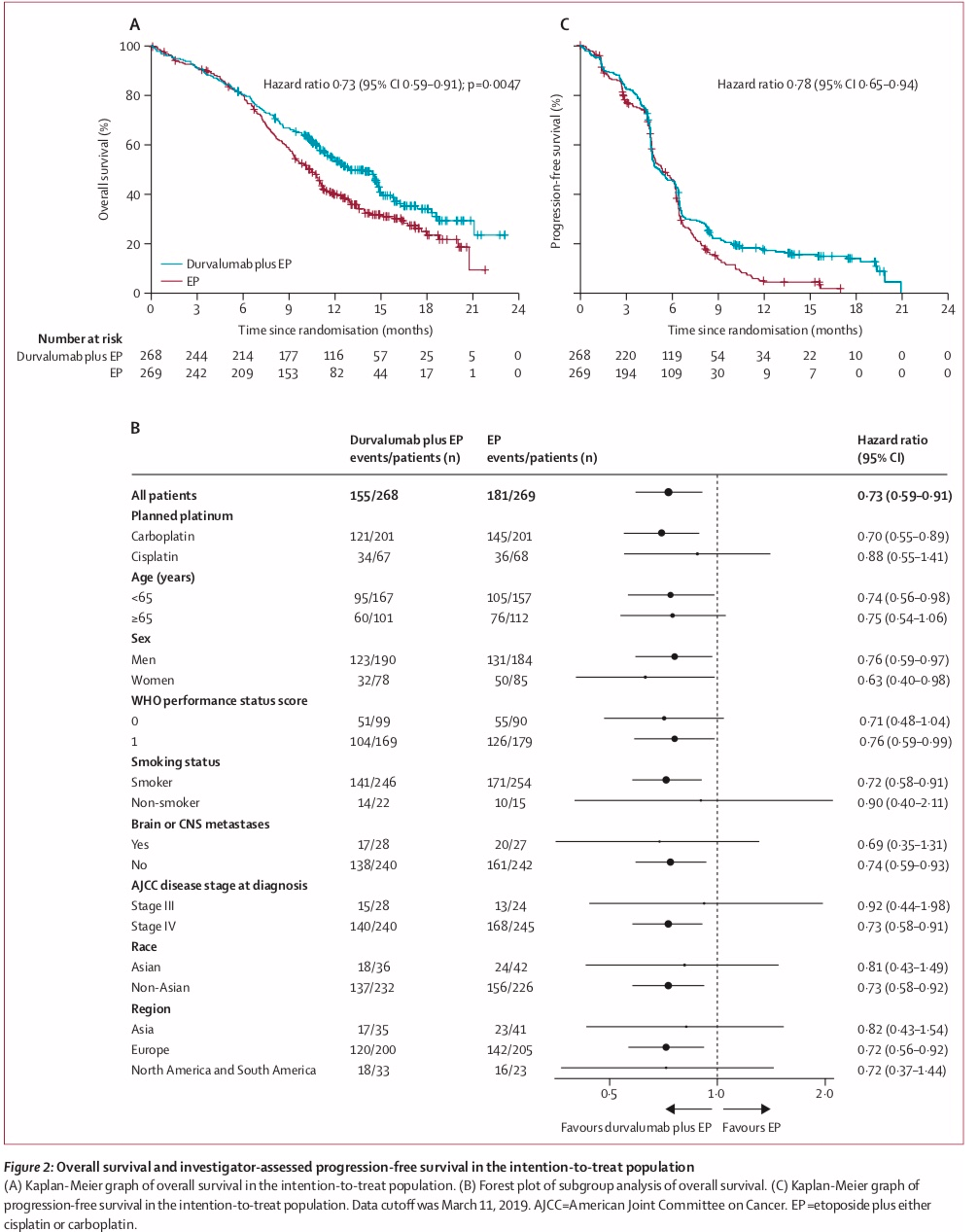
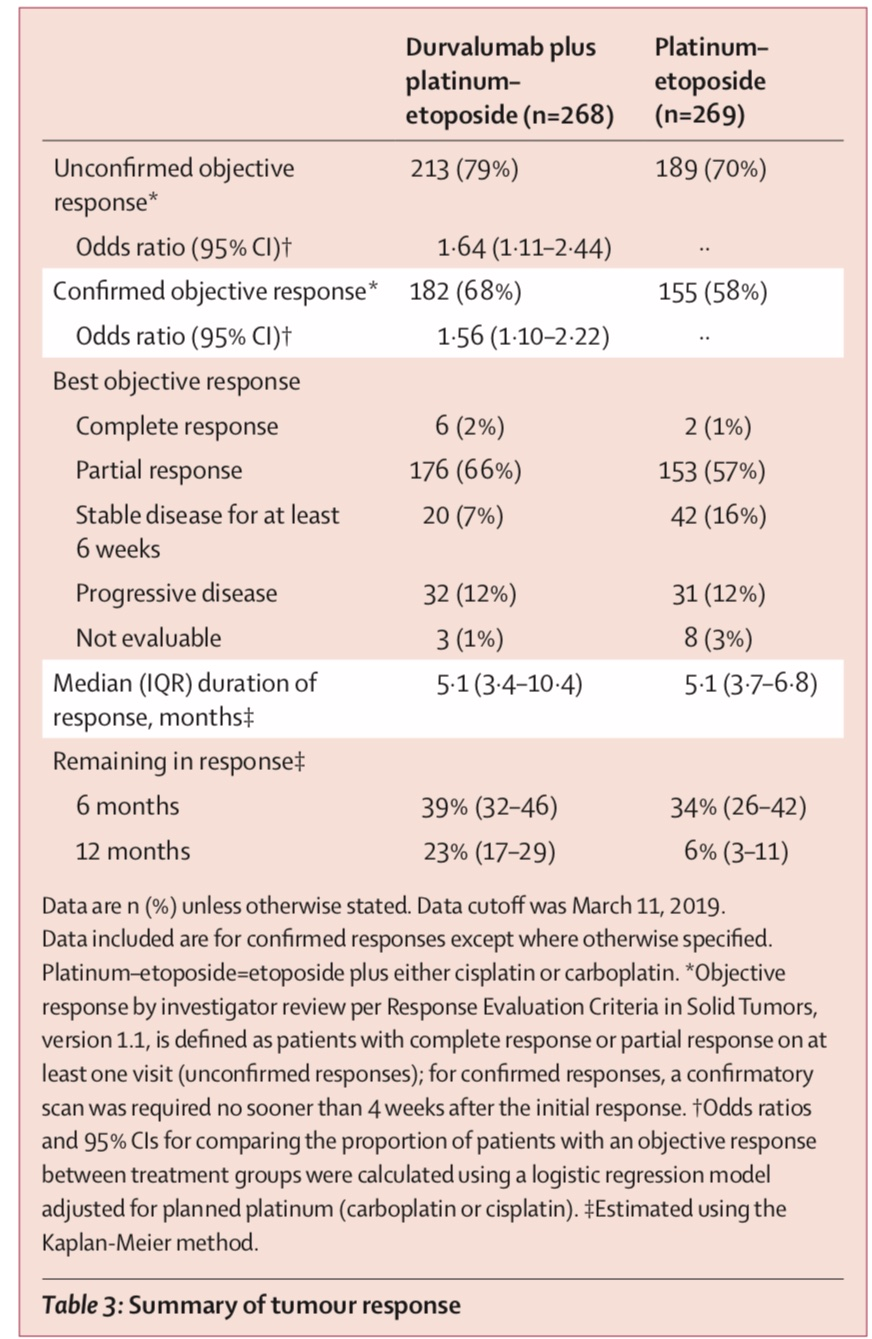
CASPIAN研究[9]:是一项Ⅲ期、随机、开放标签的全球多中心临床试验,针对广泛期SCLC患者的一线治疗,在全球22个国家的200多个中心进行。临床计划招募805例未经系统治疗的广泛期小细胞肺癌患者,分成三组:一组接受双免疫(度伐利尤单抗+CTLA-4抗体)+化疗;一组接受度伐利尤单抗+化疗;一组单独使用化疗。
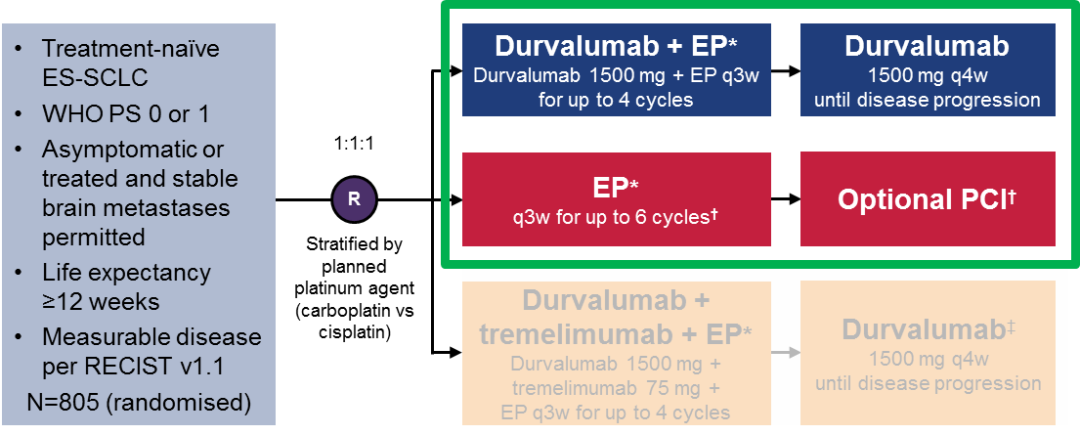
目前,只公布了度伐利尤单抗+化疗(铂-依托泊苷)组和单独化疗(铂-依托泊苷)组的数据,试验中使用固定剂量的度伐利尤单抗(1500mg),每3周给药一次,共4个周期,同时联合化疗,然后每4周给药一次,直至疾病进展。
在生存期方面:在度伐利尤单抗+化疗组联合组中,中位OS为13.0个月,而化疗单药组为10.3个月,降低死亡风险27%。另外,无论是12个月的OS率还是18个月的OS率,度伐利尤单抗联合化疗组与化疗相比同样具有显著的优势,分别为53.7%和39.8%,33.9%和24.7%。
参考文献
推荐阅读
肺癌系列文章汇总
肺癌相关指南及专家共识大汇总

微信扫一扫
关注该公众号
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言