左心疾病的右心室衰竭:从病理生理学到临床表现和预后
2022-11-04 肺动脉高压研究进展 肺动脉高压研究进展
右心衰竭(RHF)是一种临床综合征,其症状和体征是由右心结构,主要是右心室(RV)的功能障碍或超负荷引起的,导致全身静脉高压,周围水肿,最后,右心提供组织灌注的能力受损。
右心衰竭(RHF)是一种临床综合征,其症状和体征是由右心结构,主要是右心室(RV)的功能障碍或超负荷引起的,导致全身静脉高压,周围水肿,最后,右心提供组织灌注的能力受损。RHF的发病机制包括右心无力维持足够低的全身静脉压以保证最佳的静脉回流和保持肾功能。实际上,所有涉及左心的心肌疾病都可能是RHF的原因。这可能是由冠状动脉疾病、高血压、瓣膜性心脏病、心肌病和心肌炎造成的。RHF最突出的临床症状包括颈部静脉肿胀,颈部静脉压升高和踝部水肿。随着情况的恶化,液体积聚变得普遍,腿部广泛水肿,充血性肝脏肿大,最终出现腹水。诊断RHF需要有右心房和静脉压力升高的迹象,包括颈部静脉扩张,并至少有以下标准之一。(1)RV功能受损;(2)肺动脉高压;(3)周围水肿和充血性肝脏肿大。早期识别RHF并确定潜在的病因以及诱发因素,对于治疗患者并可能有效逆转临床表现和改善预后至关重要。
背景介绍:
右心衰竭(RHF)是一种临床综合征,其症状和体征继发于右心结构的功能障碍/或超负荷,导致全身静脉高压(SVH)和周围水肿,最后导致心输出量(CO)减少。RHF和右心室(RV)功能障碍(RVD)并不是同义词,因为有些患者没有症状的RVD,而且RVD并不总是引起RHF。直到最近,导致该综合征的机制还没有被完全阐明。
过去,RV很少受到关注,心脏病专家主要处理左心室的疾病,主要是因为RV对整个心脏血流动力学的贡献并不清楚。由于这个原因,RV经常被称为被遗忘的腔室,它被认为只是一个将血液传递到肺循环的被动管道。
由于RV的几何结构复杂,极难通过二维成像来描述其特征,因此RV一直被忽视。由于其特殊的形状和解剖结构,RV的容积不能用通常用于LV的方法测量。同样,RV的收缩方式也不同,其特点是普遍的纵向缩短,而径向收缩功能则不明显(图1)。
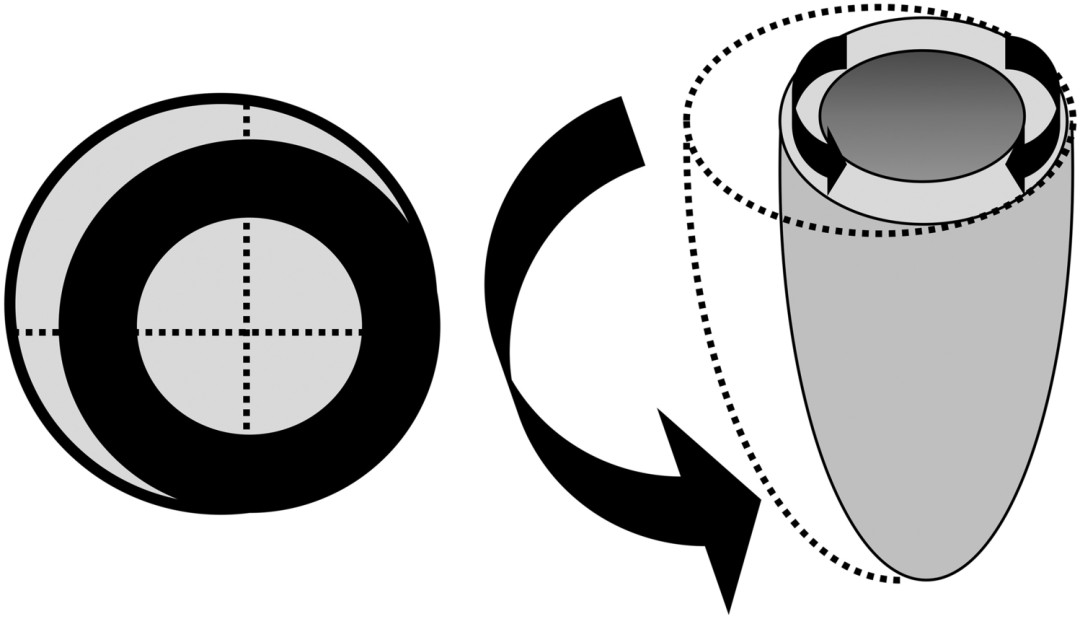
图1,右心室壁纤维缩短的方式。
从生理学角度看,RV应该被认为是一个高容量低压力泵,它的每博输出量(SV)与左心室相同,但其输出功约为25%。
RV的顺应性比LV好,能更好地处理增加的容积,但它的室壁很薄,因此在设计上很难处理急性的压力负荷。相反,它可以在压力增加最小的情况下容纳大量的血液。一项开创性的工作强调了RV和LV对实验性后负荷增加的反应(图2)。在左心室,后负荷的增加只导致SV的轻微下降;相反,同样的后负荷在左心室可以带来SV的明显下降。这些观察结果的一个临床相关的推论是,与容积过载相比,RV并不适合对抗压力过载。
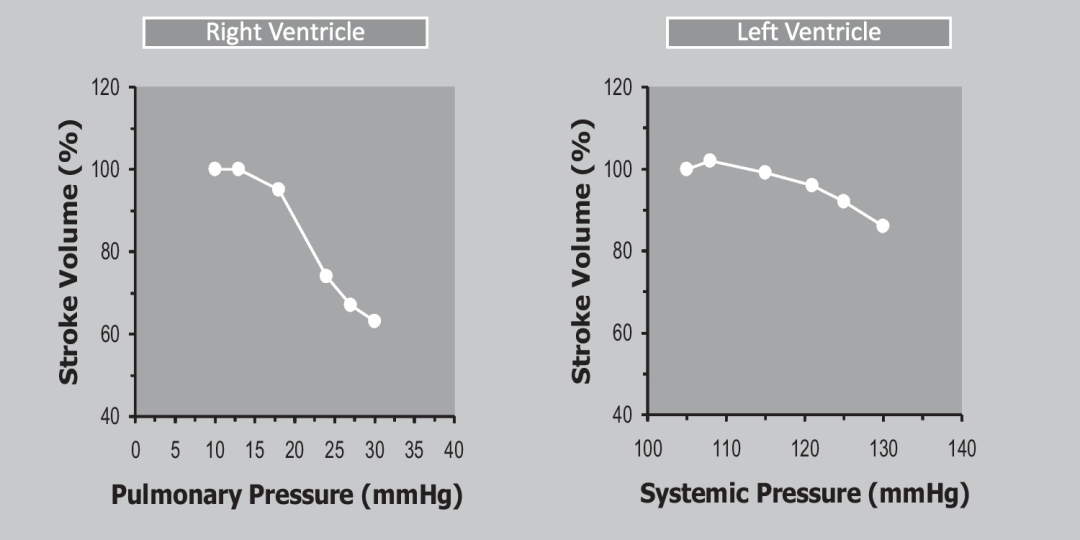
图2,右心室和左心室对增加后负荷和容积过载的反应比较。
RV抵消后负荷的能力在很大程度上取决于RV和肺循环之间令人满意的耦合,即所谓的RV肺动脉耦合,这导致了右心向肺血管的有效能量转移。RV和LV之间的密切关系,即所谓的心室相互依存关系,是由一个心室通过室间隔传递给另一个心室的力量造成的,它进一步调节了RV的行为。通过两个心室的同步收缩和松弛,实现了高效的CO和充盈。
抵消负荷的能力并不是心室之间的唯一区别。RV的任务不仅仅是以一定的势能将血液泵入循环,而且还要降低右心房(RA)的压力,将非常膨胀的静脉系统的压力维持在可能的较低水平,明显低于血浆渗透压,使血液从静脉排出。这些信息使我们能够理解RHF的起源是由于右心无力维持足够低的全身静脉压以保证最佳的静脉回流(稳定状态下与CO相等),或者只有在静脉压异常升高的情况下才能做到这一点,并解释了为什么SVH的发生是右侧HF发病的先决条件和该综合征的主要临床特征之一。
右心室衰竭的病因学和流行病学
RHF是由于RV不能支持循环中的血流和容纳静脉回流而不增加RA充盈压而引起的。RV衰竭的发病机制可能是急性或慢性的。
急性RHF最常见的原因是肺栓塞和急性心肌梗死,主要是(但不完全是)继发于右冠状动脉闭塞。比较少见的是心脏手术或植入左心室辅助装置(LVAD)后发生的急性RHF。
慢性RHF最常与左侧HF相关。心肌疾病直接影响RV的频率要低得多,如心律失常性心肌病。心肌炎可损害20%左右的患者的RV,他们通常也有左心室炎症。据报道,在Tako tsubo综合征中,有类似比例的受试者有RV受累的迹象。RHF可能是由慢性阻塞性肺病或其他慢性肺部疾病继发的慢性肺心病引起的。在COVID-19患者中也有描述,由于多次肺栓塞,可能还有直接的心肌损伤,导致RV过载和功能障碍。相反,目前还不清楚COVID-19是否也以缺氧性肺血管收缩增加RV后负荷为特征。由于房间隔缺损和原发性三尖瓣疾病(如类癌综合征或右侧心内膜炎)导致的慢性容量过载是成年发病的RHF的其他罕见病因。最后,肺动脉高压(PAH)是RHF的一个重要原因,因为它体现了基本的病理生理学原理,并且可以用特定的药物治疗。
右心衰竭的病理生理学
在PAH或RV容量过载或原始功能障碍的情况下,RV力学和功能都会发生改变。PAH引起的RV收缩功能障碍和后负荷不匹配都可能是RVD的原因。PAH的定义是收缩期肺动脉压力(sPAP)和平均PAP(mPAP)在休息时分别超过35和20毫米汞柱,或在运动时mPAP超过35毫米汞柱。正常的肺循环是一个低阻力系统,有相当的储备:因此,在PAH发展之前,有效血管床的大小必须发生实质性的减少。
RV肥大是最初的适应性反应,允许降低室壁应力和维持SV。腔室扩张随之而来,由于三尖瓣环的扩张,常常伴有三尖瓣反流。然而,由于RV不能像处理容积过载那样处理压力过载,RVD进展,三尖瓣反流恶化,SVH加重,静脉充血增加。后负荷增加成为RVD和肺源性和心源性衰竭的主要机制,无论是在急性还是慢性情况下。其他机制,如心肌缺血、神经激素激活和不利的RV-LV相互作用,可能对RV应对后负荷增加的能力产生负面影响。然而,当舒张末期容积上升时,尽管功能受到相当大的抑制,但衰竭的RV仍可射出正常或接近正常的SV。
在严重的情况下,右心扩张,室间隔向左隆起,增加左心充盈压(LHFP),损害左心充盈,导致左心HF,CO下降。当肺部血流动力学异常长期存在时,肺血管阻力(PVR)上升,这可能导致CO下降。
RVD可能引起RV充盈受损和全身静脉压升高,但SVH可能来自RV功能受损以外的其他机制,包括不适当的神经荷尔蒙激活,随后细胞外液量大量扩张,以及胸腔和呼吸系统改变引起的RA充盈异常。其他机制可能有助于RHF的发展,如继发于慢性阻塞性肺病、间质性肺病、胸腔笼畸形或神经肌肉疾病的严重呼吸障碍与通气不足。它们会阻碍血液从静脉血管排入肺循环,阻止RA和全身静脉压力的生理性下降。相反,即使在RV严重失调的情况下,也可以通过高效的呼吸泵吸入血液来维持正常的静脉回流 。
RA和全身静脉压力的升高是急性和慢性RHF中肾功能受损的主要决定因素。SVH可能是肾静脉压力上升的原因,可能会使肾功能恶化。肌酐水平的上升可能促使临床医生错误地减少环形利尿剂的治疗。然而,这种行为可能是有害的,因为它可能阻止SVH的减少,并进一步加重肾功能损害。血管加压素、肾素-血管紧张素系统和交感神经系统的激活可能会诱发血管收缩与钠和水潴留,导致肾脏灌注减少。在HF和左心室射血分数(LVEF)降低的患者中,已经证实了RVD、肾功能受损和持续充血之间的密切关系。最后,液体积聚和静脉充血可能是导致肾功能障碍和急性HF的促炎症刺激因素。
左心病的右心室衰竭
所有涉及左心的心肌疾病都可能是导致RHF的原因,这可能是由冠状动脉疾病、高血压、瓣膜性心脏病、心肌病和心肌炎造成的。继发于左心功能障碍的RV衰竭的机制包括:(1)影响LV和RV的同一病因;(2)由于LHFP增加而导致PAH的发生。
在大多数病人中,RV衰竭的发生是由于肺充血和PAH的发展,反映了LHFP升高的后向传递。左侧HF引起的慢性RHF最常见的原因是由毛细血管后PAH引起的RV后负荷逐渐增加。毛细血管后PAH的特点是平均PAP≥25 mmHg,LHFP升高:肺毛细血管楔压(PCWP)≥15 mmHg,LV舒张末期压力≥18 mmHg。大多数HF患者有毛细血管后PAH,其特点是PVR低。
传统上,HF根据LVEF的测量被划分为不同的实体。RVD的患病率根据用于识别RVD的标准而不同。在LVEF降低的HF患者中经常发现RV损伤。在一项对保留LVEF的HF研究的荟萃分析中,根据三尖瓣环面收缩期偏移(TAPSE)<16mm、三尖瓣环面收缩期速度(RV S')<9.5cm/s或分数面积变化(FAC)<35%的定义,分别有28%、21%或18%的患者存在RVD 。在Olmsted县HF和保留LVEF的受试者队列中,35%的患者TAPSE值低于规定的正常下限(16mm),21%的患者在半定量评估时有轻度或中度的RVD。
左心病的PAH也可能取决于肺循环内的血管变化,包括肺血管重塑、内皮功能障碍和与缺氧有关的血管收缩,这就转化为PVR的升高,即合并毛细血管前和毛细血管后PAH。这些患者表现出比例失调或混合型PAH,其特点是经肺梯度增加和舒张期肺梯度(舒张期肺梯度=肺动脉舒张压-PCWP)。无论发病机制如何,RVD和衰竭的发生率随着左心病的发展而增加。然而,由于适当的治疗干预,RV功能可以恢复。在HF和LVEF<50%的患者中,已经观察到随访时RVD的逆转,这些患者在基线时表现为RV功能受损。通常与左心房颤动有关的心房颤动可能进一步导致RVD和肺动脉解耦,这是因为左心房脉动负荷增加或由于心动周期长度不规则导致CO降低。
在左心病导致的HF患者中,由于液体从毛细血管转移到肺泡空间的障碍,继发于肺部充血的症状和体征最初占主导地位,包括肺部啰音、正呼吸和阵发性夜间呼吸困难。然而,随着时间的推移,LHFP的进一步增加和PAH的加重导致RV过载,最终导致RHF。
最后,左心室构型、负荷和功能的变化可通过收缩期和舒张期心室的相互依赖影响RV性能,由共享的室间隔介导,有可能导致RVD。室间、室内和RV不同步的存在可能进一步加重RVD,特别是在毛细血管前PAH的情况下。在PAH中,右心室收缩时间延长,当左心室已经放松时,右心室就会射出,从而造成室间不同步。此外,RV收缩和心肌节段放松的时间变得不均匀,部分原因是RV内壁应力的不均匀分布。PAH的生物力学超负荷决定了RV壁应力上升,也与影响能量代谢和应激反应途径的循环生物标志物水平的改变有关。后者可能诱发RV对升高的机械应力的适应机制。
体征和症状
尽管在诊断工具和生物标志物方面取得了进展,临床检查(即病史和体检)仍然是管理HF患者的核心。呼吸短促、疲劳、呼吸急促和周围水肿是最典型的主诉,但它们没有什么特异性,因为它们往往与RHF无关。
过去的医生们都知道由于液体积聚过多而引起的RHF的表现。当时,水肿,包括身体组织中液体的广泛扩张,被认为是心脏疾病的最显著的标志。
三尖瓣反流,通常在右胸骨旁线上有明显的收缩期杂音,是一个常见的发现,但在没有PAH的情况下,通常不会引起临床症状。里维罗-卡瓦略征是三尖瓣反流患者的一种罕见的临床症状,包括全收缩期杂音,吸气时声音变大。在PAH的情况下,三尖瓣反流可能加剧右心房的临床表现。
RHF的体征和症状基本上是由于SVH,以及由于心脏不能给全身静脉系统减压而导致的组织液积聚。RHF患者可能会出现一些临床症状,包括颈部静脉肿胀,颈静脉压(JVP)升高,肝颈部反流阳性和踝部水肿。随着情况的恶化,液体积聚成为普遍现象,腿部广泛水肿,充血性肝脏肿大,最终出现腹水。
治疗的原则
治疗的目标包括减少RV后负荷,优化RV前负荷,并可能增加RV收缩力(图3)。在急性和慢性RHF中,有效的治疗管理策略涉及识别和有效治疗RHF的具体原因和诱发因素。根据RHF的具体原因,如肺动脉高压、肺栓塞、感染、心律失常等,进行针对性的治疗是至关重要的。通过使用常用于治疗左侧HF的药物治疗继发于LV功能障碍和衰竭的肺充血,可以获得RV功能的改善和RV超负荷的减轻。
图3,优化右心室前负荷、后负荷和收缩力的策略。
临床经验告诉我们,对于急性RHF和低输出量的患者,可暂时采用增加RV收缩力的措施,如多巴胺、米力农和左旋门冬酰胺,或机械支持。使用血管扩张剂,如静脉注射前列环素,以减少RV后负荷,只限于少数情况。显然,这些方法大多需要静脉给药,因此不能长期有效。
液体管理对于治疗RV衰竭和静脉充血迹象的患者无疑是至关重要的。一个常见的误解是,大多数RHF患者是前负荷依赖性的,应通过补充容量来确保RV充盈压升高,从而获得最佳的CO;相反,绝大多数RHF是由静脉充血导致的RV容量过载引起的,或与之相关,或加剧。体积过大往往会增加RV壁的压力,增加三尖瓣反流的严重程度,恶化RV-LV的相互作用,并可能降低CO。全身静脉充血在心肾综合征的发病机制中起着关键作用。
利尿剂是治疗充血的主要疗法。RHF患者的利尿会导致静脉充血的减少,从而改善肾功能,缓解缺氧和脾脏器官细胞的酸中毒。患者往往需要限制液体和盐分,并使用大剂量的环形利尿剂(即呋塞米),主要是因为同时存在神经激素激活、利尿剂抵抗和与内脏水肿有关的口服药物吸收障碍。在服用环形利尿剂的病人中,仰卧位而不是直立位可能会获得更大的利尿效果和体重减轻。由于近端和远端肾小管对钠的重吸收增加,慢性环形利尿剂治疗可能出现利尿作用减弱,有时被称为制动现象。由于肾小球对钠重吸收的顺序阻断,通常通过环形利尿剂与噻嗪类和/或乙酰唑胺的联合治疗来清除多余的液体。美托拉宗可与呋塞米联合治疗严重的RHF和难治性水肿。电解质失衡常常由这种关联引起,补充钾和/或服用保钾剂可能是有益的。尽管肾小球滤过率低,但美托拉宗会产生利尿反应。托拉塞米有时优于呋塞米,因为其口服生物利用度更好。醛固酮拮抗剂可能有助于从钾的损失中维持钾的平衡。最后,体外超滤是治疗RHF急性失代偿期患者容量过载的一种替代疗法。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言