北京大学汪贻广教授《自然·通讯》:特异性靶向肿瘤相关巨噬细胞溶酶体,重编程M2型巨噬细胞
2023-09-26 BioMed科技 BioMed科技 发表于上海
北京大学汪贻广教授团队设计了一个能区分不同免疫细胞酸性溶酶体环境(pHL)的pH门控纳米颗粒(PGNs)库,用来特异性靶向和重编程肿瘤微环境中M2样巨噬细胞。
肿瘤微环境具有严重的免疫抑制作用,阻碍了免疫治疗。作为肿瘤微环境中最丰富的免疫细胞,肿瘤相关巨噬细胞 (TAM) 主要表现出促肿瘤 M2 样表型,在肿瘤进展、转移、免疫逃避和免疫治疗耐药中发挥着至关重要的作用。研究表明TAM主要通过以下途径抑制细胞毒性T细胞功能:(i)产生抑制性细胞因子(如IL-10);(ii)干预抗原呈递;(iii)抑制免疫刺激性群体(如树突状细胞、DC)的和招募免疫抑制群体(如调节性T细胞)。当前,多种抗 TAM 策略已陆续开展中。然而,特异性操纵 TAMs 以促进抗肿瘤免疫反应,同时保护健康组织中的巨噬细胞仍然是一个重大挑战。
成熟的树突状细胞(DCS)可以通过增加细胞的pH值和降低溶酶体酶水平生成合适的抗原表达肽,发挥抗原呈递作用。在TAMs中,M2样表型的巨噬细胞会上调溶酶体功能,引起抗原降解及免疫沉默。相反,促炎性M1样巨噬细胞能下调溶酶体功能,并且具有抗原交叉呈递的潜力。M1通过该抗原交叉呈递有效激活CD8+T细胞清除肿瘤。如何调节 M2样TAMs的溶酶体功能将其促肿瘤表型转变为杀肿瘤M1样表型,从而微调其蛋白水解作用,将抗原有效呈递给细胞毒性T淋巴细胞呢?
基于此,北京大学汪贻广教授团队设计了一个能区分不同免疫细胞酸性溶酶体环境(pHL)的pH门控纳米颗粒(PGNs)库,用来特异性靶向和重编程肿瘤微环境中M2样巨噬细胞。PGN库由11个纳米颗粒组成,pH响应从4.5到5.5,涵盖溶酶体不同细胞类型的pH值范围。通过PGN4.9纳米粒子成功筛选出能特异性靶向M2型巨噬细胞的溶酶体酸性信号(pHL~ 4.4)。此外,研究者设计了一种具有 AND 门控能力的 PGN 4.9 纳米佐剂,将高溶酶体酸度和组织蛋白酶活性两种串联信号,有效释放 Toll 样受体7/8(TLR7/8) 激动剂(咪唑喹啉,IMDQ ),选择性地将M2样表型重编程为M1样表型。PGN4.9纳米佐剂在肿瘤细胞中可有效调节 M2 样 TAM 的溶酶体酸化和蛋白水解,增强抗原交叉呈递并激活 CD8 +T细胞功能,增强癌症免疫治疗。相反,PGN4.9纳米佐剂在其他细胞类型中保持惰性,有效避免了急性全身毒性。PGN 4.9 纳米佐剂联合化疗或检查点抑制剂可诱导肿瘤退消退和延长肿瘤小鼠存活期。该工作为如何特异性调节 TAM 的溶酶体功能以实现有效的癌症免疫治疗提供了新的见解。
该研究以题为《pH-gated nanoparticles selectively regulate lysosomal function of tumour-associated macrophages for cancer immunotherapy》的论文发表在《Nature Communications》期刊上

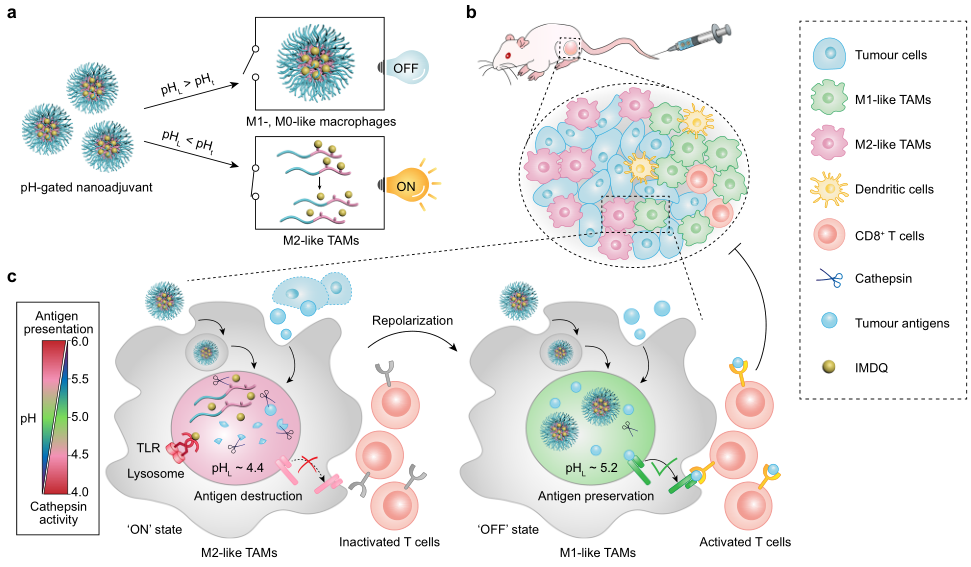
图1. PGN4.9纳米佐剂的设计和调节M2型作用机制。
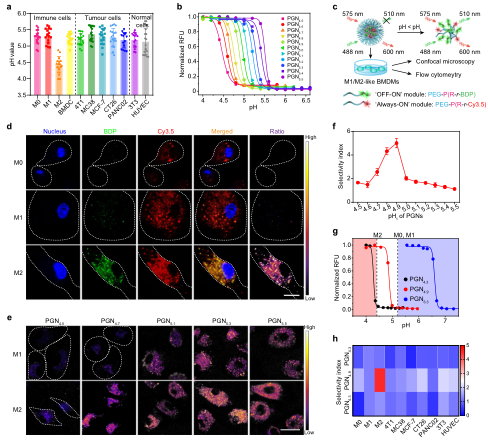
图2. PGNs库的设计与表征。
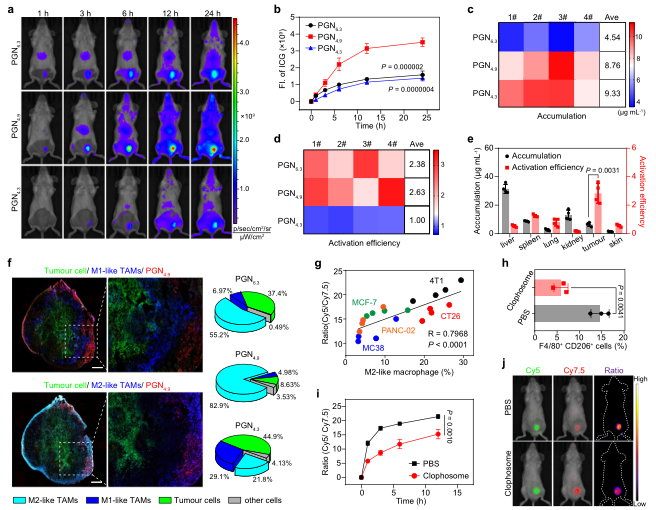
图3. PGN4.9体内选择性靶向M2型巨噬细胞。
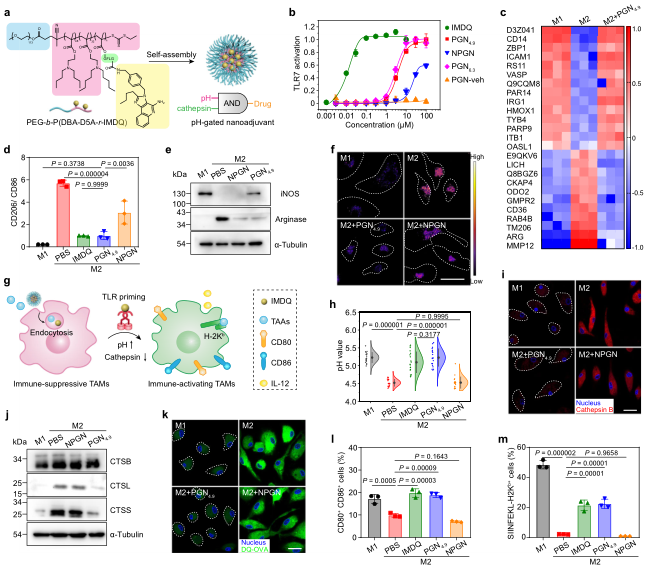
图4. PGN4.9纳米佐剂重编程M2样巨噬细胞,增强体外抗原交叉呈递。
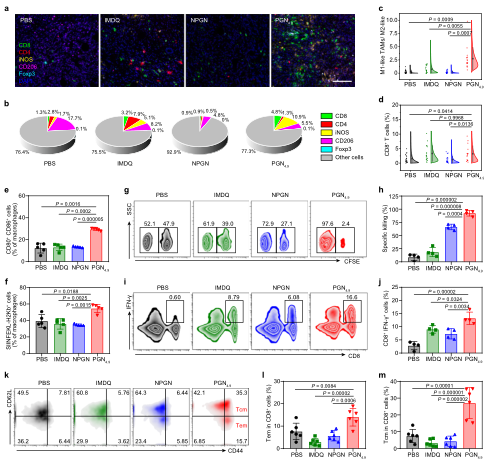
图5. PGN4.9纳米佐剂改善免疫抑制性微环境。

图6. PGN4.9纳米佐剂在不同肿瘤模型中的治疗效果。
TAMS在不同癌症类型中具有不同的功能。当前抗TAMs药物主要基于三种策略:(i)抑制TAMs的招募,(i)靶向T A M的耗竭以及(iii)M2样巨噬细胞重编程。然而,抑制TAMS招募和存活不能维持持续抗肿瘤效应,而巨噬细胞重编程是一个更有效的策略,不但可以改善免疫抑制功能,而且可以增强抗原交叉表达。
适应性免疫应答需要有效的抗原交叉呈递。这个过程需要专业抗原呈递细胞溶酶体的适当调节,而高活性的溶酶体蛋容易导致抗原的降解。对于TAMs而言,它们的溶酶体降解能力取决于其表型的溶酶体酸性,M1样巨噬细胞有一个最佳的溶酶体活性,能触发抗原交叉呈递激活CD8+细胞功能。因此,靶向M2型TAMs对M1型表型的极化,对逆转免疫抑制性肿瘤微环境、增强抗原交叉呈递,最终实现抗癌症免疫具有很大的意义。
免疫激动剂(如R848和CPG)经自由扩散分布于全身,容易造成严重的系统免疫毒性。已开发了多种纳米颗粒来递送免疫激动剂来实现M2样TAMs的极化。然而,许多此类策略是基于组织靶向机制,这种机制也能激活肝、脾、肺和皮肤等非恶性器官中的M0和M1样巨噬细胞,从而引起生物安全方面的担忧。因此,特异性调节M2样TAM的纳米佐剂技术为癌症免疫疗法提供了安全有效的保障。
基于M2样TAMs(pHL~4.4)与M0和M1样巨噬细胞(pHL~5.2)之间的溶酶体pH差,利用pH响应纳米技术是实现M2样TAMs靶向调节的一种很有前途的方法。在本文中,研究者成功设计和筛选了特异性靶向M2型TAMs的 PGN 纳米佐剂。它具有以下几个特点:首先,PGN 纳米佐剂pH响应灵敏度高(ΔpH ON/OFF ~ 0.2-0.3),对于M2型TAMs溶酶体的pH门控激活十分重要;其次,pHt的可调性使其能成功筛选PGN4.9纳米辅助剂,用于特定靶向M2样TAMs;最后,通过酶介导的药物释放,能成功实现免疫治疗。
原文链接:
https://doi.org/10.1038/s41467-023-41592-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








感谢分享
35