专家共识:临床试验统计分析计划及统计分析报告的考虑
中国临床试验生物统计学组(CCTS)成员(按姓名拼音排序):陈峰、陈平雁、陈启光、贺佳、黄钦、金丕焕、李康、李宁、李卫、李晓松、凌莉、刘玉秀、苏炳华、孙高、王武保、王彤、魏朝晖、夏结来、姚晨、易东统计分析计划(statistical analysis plan,SAP)是对临床试验的统计学考虑及拟对数据进行统计分析的清晰描述。统计分析计划可以是独立的文
中国卫生统计信息 - 统计分析,试验 - 2016-01-12
药物临床试验期间安全性信息汇总分析和报告指导原则(试行)2023
根据现行《药品注册管理办法》《药物临床试验质量管理规范》和《药物警戒质量管理规范》,为推进临床试验期间安全信息汇总分析与风险评估工作,在国家药品监
国家药品监督管理局药品审评中心 - 药物临床试验,安全性信息汇总分析 - 2023-03-25
国家食药监总局连发3个文件规范临床试验数据管理
昨日,针对此前临床试验中存在的诸多问题以及由此对药品研发和审评造成的影响,国家食品药品监督管理总局连续发布了《临床试验数据管理工作技术指南》、《药物临床试验数据管理与统计分析的计划和报告指导原则》和《临床试验的电子数据采集技术指导原则》,以确保临床试验数据的真实、准确、完整和可靠,并强化药物临床研究的自律性和规范性,从源头上保证药品技术审评的质量。临床试验数据管理工作技术指南.docx药物临床试验
国家食药监 - 临床试验数据 - 2016-08-01
重磅!疫苗“一致性评价”来了
今日(12月24日),为进一步规范和提高疫苗临床研发水平,加强疫苗质量安全监管,国家药监局印发《预防用疫苗临床可比性研究技术指导原则》(以下简称指导原则)。
医谷 - 疫苗,一致性评价 - 2019-12-24
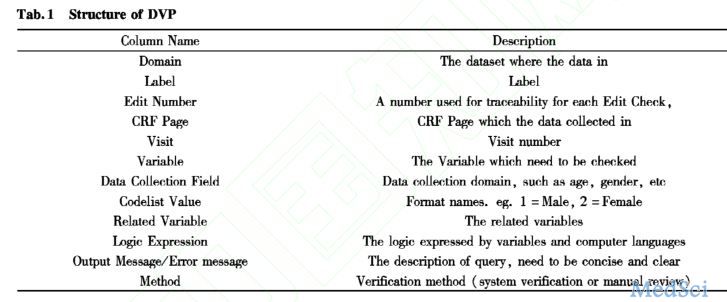
临床试验逻辑核查的分类及应用
作者:周蓓,于浩(南京医科大学公共卫生学院,南京 211166,江苏)来源:中国临床药理学与治疗学 2019-06-27摘要:临床试验数据的清理是临床试验过程中非常重要的环节,完整、清洁的数据才能用于统计分析本文旨在讨论临床试验数据清理过程中数据核查计划的撰写及逻辑核查的分类等,并进一步讨论近年来临床试验数字化趋势对数据的采集及清理可能带来的影响。关键词:临床试验;数据清理;病例报告表设计;
中国临床药理学与治疗学 - 逻辑核查 - 2019-12-26
药物临床试验数据管理与统计分析的计划和报告指导原则
虽然我国《药物临床试验质量管理规范》(Good Clinical Practice,GCP)中对药物临床试验数据管理与统计分析进行了原则要求,且国家食品药品监督管理总局已发布的有关药物临床试验及其统计学的相应技术指南也涉及数据管理和统计分析工作的主要环节,但针对数据管理计划和报告、统计分析计划和报告却没有详细的技术规范和指导性建议。因此,本技术指导原则对此进行了较为详细的介绍和阐述,并提出具体要求
国家食药监总局 - 药物临床试验数据管理与统计分析,计划和报告 - 2016-08-01
药物临床试验数据管理与统计分析计划指导原则(征求意见稿)
为进一步明确药物临床试验中数据管理和统计分析计划相关技术要求,我中心起草了《药物临床试验数据管理与统计分析计划指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议。
CDE - 数据管理,统计分析计划 - 2021-09-03
CCTS 专家共识:临床试验统计分析计划及统计分析报告的考虑 2015
统计分析计划( statistical analysis plan,SAP) 是对 临床试验的统计学考虑及拟对数据进行统计分析的清 晰描述。统计分析计划可以是独立的文件,其内容涵 盖试验中所涉及的所有统计学考虑,且具有技术性和 可操作性,包括了设计的类型、比较的类型、随机化与 盲法、主要指标和次要指标的定义与测量、检验假设、 数据集的定义、疗效及安全性评价和统计分析的详细 计划。
CCTS,统计 - 2015-06-17
FDA指导原则:使用饮食管理的先天性代谢错误:在药物产品开发的临床试验中优化和标准化饮食的注意事项:行业指南
本指南描述了食品和药物管理局 (FDA) 关于如何在临床试验中优化和标准化饮食管理的当前建议,以开发治疗先天性代谢障碍 (IEM) 的药物,其中饮食管理是患者代谢的关键组成部分。 控制。 在进入临床试
FDA - 2021-10-22
2016 药物临床试验安全评价•广东共识
为了明确临床试验过程中药物安全性评价相关概念、原则和方法,增加研究的可操作性,以期提高药物临床试验安全信`急质量并规范评价方法,本会药物临床试验专业委员会编写了《安全评价·广东共识》,现予以印发,供各医疗单位参考
广东省药学会网站 - 药物临床试验,安全评价 - 2016-10-09
2016 药物临床试验受试者招募·广东共识
为确保受试者权益,对临床试验过程中招募对象的选择、招募方式、招募材料、发布方式等予以明确; 为伦理委员会审查,药物临床试验机构监管提供参考,使申办者、研究者在受试者招募过程中更加公平、合理、规范。
今日药学.2016,26(5):289-290. - 药物临床试验 - 2016-09-21
我国临床试验生物统计学指导原则与国际ICH E9比较研究
Harmonised Tripartite Guideline Statistical Principles ClinicalTrails E9》(以下简称“ICH E9”)是在人用药品注册技术要求国际协调会议的赞助下制定,目的从统计学原理和方法出发,向申办者和专家提供建议,以便有助于为申请新药入市而作的临床 试验的分析和结论得到公认。现主要用于欧盟日本及美国管理当局的
中国卫生统计 - 生物统计,ICH,E9 - 2014-08-09
新药临床试验设计中的基础问题解读
1新药临床试验管理规范1.1受试者权益安全性保障(即伦理性) 1.临床试验必须获得国家药品监督管理局的批准 2.为确保受试者的权益,并为之提供公众保证。必须经伦理委员会批准 3.中国GCP规定参加临床试验的研究单位必须是国家药品临床研究基地 4.中国GCP规定,负责临床试验的研究者(investigator)必须具备的条件
MedSci原创 - 新药,临床试验,设计 - 2012-12-25
为您找到相关结果约500个