CRO公司临床研究监查盲区在哪里?
制定完善的《监查计划》,是保证临床研究质量的关键。但是,即使是有丰富临床研究管理经验的国际性CRO公司,在制定《监查计划》的时候,也难免有所疏漏。
医药经济报 - CRO,临床研究,医药外包服务 - 2019-09-24
宁夏药监局公布监查计划:重点查药店特殊药品
3月12、13日,宁夏回族自治区药监局分别印发了《2019年全区药品生产、特殊管理药品监督检查计划》(以下简称《检查计划》),《宁夏回族自治区药品监督管理局药品批发企业零售连锁总部监督检查制度(试行)》(以下简称《检查制度》)的通知。
药店经理人 - 宁夏,药监局,监查计划 - 2019-03-14
CDE和注册司专家发文:基于风险的监查(RBM)应用和挑战
药品化妆品注册管理司,北京 100038) 来源:中国新药与临床杂志 2018年6月 第37卷第6期 摘要:本文结合国际人用药品注册技术要求协调会(ICH)及美国食品和药物管理局(FDA)关于基于风险的监查
中国新药与临床杂志 - CDE,风险的监查 - 2018-08-16
CDE发布《药物临床试验中心化监查统计指导原则(征求意见稿)》公开征求意见通知
9月16日,国家药监局药审中心(CDE)发布《药物临床试验中心化监查统计指导原则(征求意见稿)》并公开征求意见通知。
CDE - 国家药品监督管理局药品审评中心 - 2021-09-17
CFDI最新分享了核查中发现的常见问题总结,探讨了新形势下申办方的应履职责
从药物临床试验数据核查看申办者的职责履行情况 作者:高荣王安娜唐静方翔王佳楠 国家药品监督管理局食品药品查验中心 来源:中国新药杂志 2019 年第 28 卷第 8 期摘要:申办者作为药物临床试验的发起组织者、经费提供者和试验监查者
网络 - 药物临床试验,药物临床试验质量管理规范,数据核查,申办者,职责 - 2019-06-09
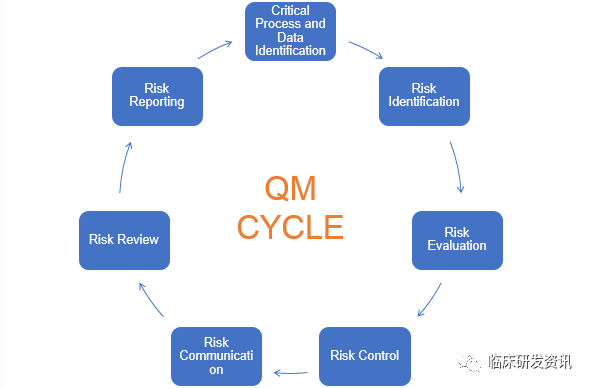
临床试验中的风险识别及风险管理
临床试验中不好的一面--风险,临床试验中处处都有坑。对待未知的事物,我们都会感觉莫名的恐惧和消极,但是对待任何未知事物人们的处理流程都是相似的,先认识,理解,再在这个认知的基础上去想办法应对,并加以利
MedSci原创 - 风险管理,临床试验 - 2020-03-29
临床研究中临床监查员(CRA)监查的职责与要求
监查员(Monitor,也称"临床研究助理"即 CRA)是申办者与研究者之间的主要联系环节。 织梦好,好织梦 监查员的资格: 监查员应有适当的医学、药学或相关专业学历,并经过必要的训练(药品研发、临床试验、GCP、SOPs等),熟悉药品管理有关法规,熟悉有关试验药物的临 床前和临床方面的信息以及临床试验方案及其相关的文件一名监查员的最合适的资格将取决于试验的类型和研究的产
MedSci原创 - 监查 - 2013-11-30
临床研究监查:原始资料从“核查”到“审核”
原始资料核查(SDV)一直都是保证临床研究质量的重要手段,也是监查员在临床研究监查过程中花费时间和精力最多的地方。但是,随着申办方和研究者临床研究经验的不断积累、各种临床研究新工具的不断出现,百分之百的原始资料核查已经不能满足临床研究监查工作高质量与高效率并举的要求。 随着美国FDA基于风险的临床研究监查指导原则的推出,原始资料审核(SDF,Source document Revi
网络 - 研究监查 - 2019-12-26
解读美国FDA关于临床研究监查的新指导原则
有着6年临床医师经验,曾先后担任新加坡ICON临床研究有限公司临床研究副总监,加拿大ICON临床研究有限公司和加拿大PAREXEL 国际公司等公司的高级CRA,对临床研究监查有16年丰富经验
中国处方药 - 临床研究,监查 - 2013-11-30
李宾:临床试验中中心化监查可发现90%问题
CRA(临床监查员)忙于各种程序,都无暇做监查。 如何解决这一难题?李宾介绍,2011年8月,FDA出台了一份有关临床研究监查的新
MedSci原创 - 中心化,监查 - 2013-11-30
对美国FDA关于临床试验监查的新指导原则的解读
在2011年末,FDA推出了关于临床试验监查的新指导原则(A Risk-Based Approach to Monitoring)的草案。因为这个指导原则对临床试验监查的看法同现行的模式完全不同,让人产生了临床试验将来是否还需要监查 的想法。在2013年8月,FDA正式颁布了该指导原则。也就意味
Tigermed - FDA,监查 - 2014-09-25
FDA:新药临床研究需要基于研究风险的监查模式(Risk-based Monitoring)
2011年8月,FDA出台了一份有关临床研究监查的指导原则草案(Guidance for Industry Oversight of Clinical Investigations——A Risk-Based该指导原则草案强调了集中化监查(Centralized Monitoring)的重要性。在此之前,FDA
MedSci原创 - 风险的监查 - 2013-12-07
临床研究:具有中国特色的主要研究者(PI)
主要研究者的英文是Principal Investigator,缩写为PI。根据ICH-GCP的定义,Principal Investigator 同Investigator实际上是一回事。如果一个药物临床研究机构(国外称为Site)只有一个研究者,就称为Investigator,如果一个机构有多位研究者,那么主要负责的研究者就称为PI,其他称为Sub-investigator(辅助研究者),
MedSci原创 - 临床研究,研究者 - 2014-05-19
临床试验有关SOP汇总
临床试验方案修改SOP1. 申办者(包括药厂、CRO等)向中心药物临床试验办公室提出修改申请,填写“药物临床试验修改申请表”。2. 提供资料,包括:药物临床试验前研究资料,含试验药物的化学、药学、毒理学、药理学和临床的(包括以前的和正在进行的试验)资料和数据、研究者手册、试验药品药检报告、申办者资质证明、SFDA药物临床试验批文、试验方案和知情同意书(可以是初稿)。3. 药物临床试验办公室根据
MedSci原创 - 临床试验,SOP - 2014-03-28
为您找到相关结果约151个