EMA支持批准两种丙肝药物Epclusa和Zepatier
欧洲药品管理局 (EMA)支持批准Epclusa(sofosbuvir/velpatasvir,400mg/100mg) 用于全基因型丙肝、 Zepatier(grazoprevir/elbasvir,
MedSci原创 - EMA,Zepatier,丙肝 - 2016-05-31
20价肺炎球菌疫苗,即将获得EMA的批准
所有侵袭性肺炎球菌疾病例的一半以上是由20vPnC涵盖的20种血清型引起的,其中包括7种血清型(8、10A、11A、12F、15B、22F和33F)。
MedSci原创 - 20vPnC,20价肺炎球菌疫苗 - 2021-02-26
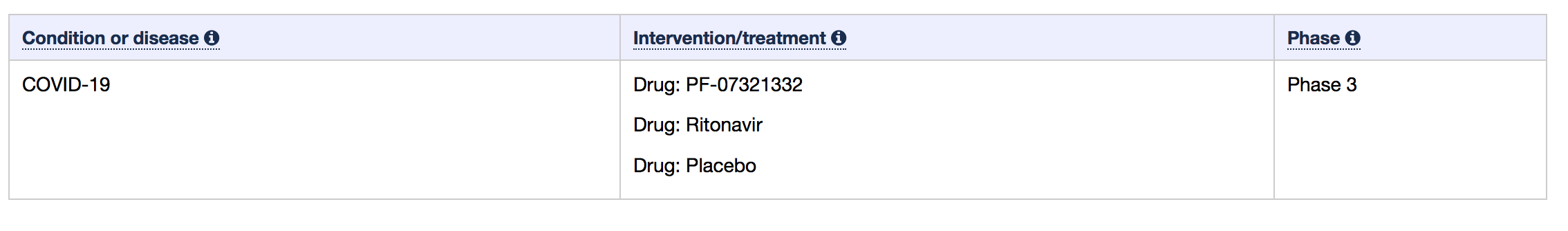
EMA建议对辉瑞的Paxlovid进行有条件授权
辉瑞上个月报告的试验结果显示,与安慰剂相比,Paxlovid 在症状出现后三天内服用可将住院或死亡风险降低 89%,在五天内服用可降低 88%。
MedSci原创 - Covid-19,Paxlovid - 2022-02-03
FDA:百特药物ADVATE欧洲SmPC更新获EMA批准
百特(Baxter)22日宣布,欧洲药品管理局(EMA)已批准了药物ADVATE(重组全长FVIII因子)的产品特性概要(SmPC)更新,纳入了IV期预防性研究的数据,使临床医师和患者能够更好地选择个性化的治疗方案
生物谷 - 新药,FDA - 2013-07-24
EMA确认AbbVie的MS药物Zinbryta的风险超过益处
欧洲药品管理局(EMA)近日披露,它对Biogen和AbbVie的Zinbryta(daclizumab)的审查证实,多发性硬化症(MS)药物Zinbryta会对脑部、肝脏和其他器官造成严重和可能致命的免疫反应
MedSci原创 - Zinbryta,退市,益处风险比 - 2018-05-20
EMA就使用regdanvimab治疗COVID-19,持谨慎意见
EMA人用药品委员会(CHMP)已完成对单克隆抗体regdanvimab(也称为CT-P59)治疗COVID-19的审查。
MedSci原创 - Covid-19,COVID-19肺炎,regdanvimab - 2021-03-27
EMA:III期试验成功—Medicines耗资$2.4亿收购ProFibrix
Medicines公司今天公布了生物制剂Fibrocaps的关键性III期临床试验FINISH-3的数据,该项试验在美国和西欧的65个站点开展,涉及719例患者,在4个不同的手术适应症脊柱外科、肝切除、软组织剥离、血管手术中,均达到了所有主要和次要止血疗效终点。 Fibrocaps是荷兰生物技术公司ProFibrix开发的一种生物制剂,这是一种干粉外用配方的纤维蛋白原和凝血酶,开发用于手术过
生物谷 - 新药,EMA - 2013-08-07
EMA接受辉瑞新药BZA/CE上市许可申请的审查
欧洲药品管理局(EMA)表示,已接受对辉瑞(Pfizer)药物BZA/CE(bazedoxifene/conjugated estrogens辉瑞预计在2013年得到EMA的
生物谷 - 新药,FDA - 2012-07-24
EMA接受审查阿斯利康新药naloxegol上市许可申请
阿斯利康(AstraZeneca)9月27日宣布,欧洲药品管理局(EMA)已接受审查实验性药物naloxegol上市许可申请(MAA)。
生物谷 - 新药,FDA - 2013-09-30
蓝鸟生物生产规范获EMA批准 基因疗法Zynteglo准备上市!
近日,蓝鸟生物(bluebird)宣布,欧洲药品管理局(EMA)已批准其基因疗法Zynteglo(含βA-T87Q球蛋白编码基因的自体CD34+细胞)的精细商业药品制造规范。
新浪医药新闻 - 蓝鸟生物,基因疗法 - 2019-10-25
EMA建议:限制育龄期女性使用丙戊酸盐
欧洲药品管理局(EMA)药物安全和风险评估委员会建议,加强对丙戊酸盐的使用管理,限制育龄期女性使用丙戊酸盐。 这是由于,孕期丙戊酸盐暴露会导致胎儿畸形和发育问题。
丁香园 - 丙戊酸钠,EMA,女性,育龄女性,药物 - 2014-10-22
贝伐珠单抗新适应证有望获EMA批准
9月20日,欧洲药品管理局(EMA)人用药品委员会(CHMP)宣布对正在申请的贝伐珠单抗新适应证持积极肯定的意见,新适应证为,贝伐珠单抗与卡铂和吉西他滨联用适用于首次复发的铂敏感性上皮性卵巢癌、输卵管癌和原发性腹膜癌患者
中国医学论坛报 - 贝伐珠单抗,靶向药物 - 2012-10-26
EMA:托哌酮受限 仅卒中后痉挛用
2012年6月22日,欧洲药品管理局(EMA)发布信息,推荐限制托哌酮的使用,仅限用于卒中后痉挛的口服治疗。
医学论坛网 - 托哌酮,肌肉松弛剂,卒中后痉挛 - 2012-07-06
EMA支持首个B型脑膜炎球菌疫苗上市
11月15日,欧洲药品管理局(EMA)推荐批准首个B型脑膜炎球菌疫苗(Bexsero)上市。该疫苗将获准用于年龄在2个月以上的人群。 EMA将要求欧委会批准Bexsero疫苗用于2个月以上人群。 由于美国B型脑膜炎发病率低于欧
医学论坛网 - B型脑膜炎球菌,疫苗 - 2012-11-27
EMA公布GMP违规:印度和中国违规药企数居首
为了增加透明度,欧洲药品管理局(EMA)已公布了EudraGMDP数据库,数据库整理了不符合GMP的工厂。EMA在一份声明中表示,这项新措施已作为提高透明度和业务开发而采取。目前,该数据库包括2007年以来80多个违规报告。按照该报告,2013年有34例设施未能
生物谷 - 印度,中国,药企数,EMA - 2014-01-23
为您找到相关结果约500个