2018年FDA批准的临床试验进展的新药汇总
新药和生物制品的提供常常意味着为患者提供新的治疗方案,从而促进公众的健康保健,而FDA的药物评价和研究中心(FDA’s Center for Drug Evaluation and Research,CDER)在帮助推进新药开发方面发挥关键作用。每年,CDER都批准许多新药和生物制品,其中一些产品是创新的新产品,以前从未在临床实践中使用,而一些产品是与先前批准的产品相同或相关,这些药品将进
MedSci原创 - 新药,FDA,2018 - 2018-12-19
一文读懂国内外药品试验数据保护制度
2017年5月,CFDA发布《关于鼓励药品医疗器械创新保护创新者权益的相关政策(征求意见稿)》,明确提出完善药品试验数据保护制度,对于数据保护,我们到底了解多少?
医药经济报 - 药品试验,数据保护 - 2017-10-06
临床方案中主要疗效指标及试验时间的考虑要素
众所周知,新药临床试验的主要目标,是寻找风 险效益比可以接受、用法与用量安全有效的药物;同时,确定可能由该药受益的特定对象及使用适应症。因此在临床试验方案设计时,对照药的选择、剂量探索的设 计、主要疗效指标的选择、试验时间的确定等因素,都是重要的基本考虑点。这些因素将决定临床试验是否能为药品注册提供有效的证据,其中任何因素的设计错 误,都可能导致试验结果无法对产品能否上市作出判断,从而造
中国临床药理学杂志 - 研究设计,时间 - 2017-06-29
2018年中国肿瘤临床试验蓝皮书
前言 本蓝皮书纳入统计的肿瘤试验全部来源于“药物临床试验登记与信息公示平台”(http://www.chinadrugtrials.org.cn/eap/main),时间以登记网站上“首次公示信息日期”作为统计时间节点,有些试验可能早就结束,但首次公示信息日期是2018年,也纳入统计;有些试验招募的是健康受试者,则不在统计范围以内。
临床试验招募信息 - 肿瘤,临床试验 - 2019-02-03
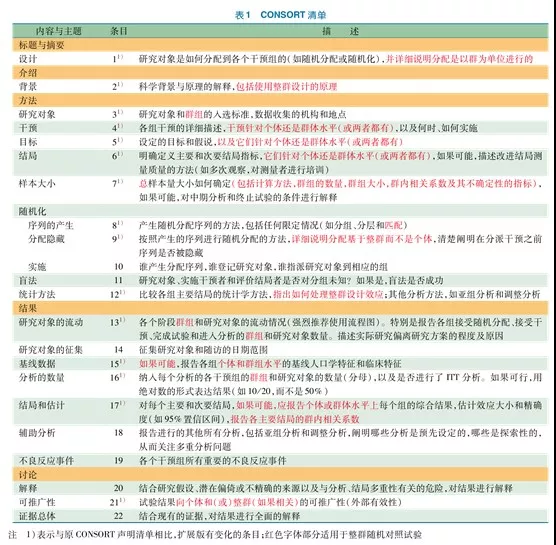
【讲堂】临床试验报告的统一标准(CONSORT)
一随机对照试验及其报告现状随机对照试验(RCT)通常是评估干预效果的最佳研究设计,但低质量的临床试验可能会错误地估计疗效。自2000年以来,每年都有25000篇随机或对照试验的文章被发表,但庞大的数量并不意味着决策者很容易找到可信的证据进行临床和保健决策,中国发表的随机对照试验文章质量亦令人堪忧。
复旦循证护理中心 - 临床试验报告 - 2018-12-13
BMJ:随机对照试验中基于性别的亚组差异
统计学显著性的性别-处理相互作用的频率只是比预期的稍有增加,而性别-处理相互作用的后续证实或临床相关性证据较少。
MedSci原创 - 性别-处理相互作用 - 2016-11-24
临床试验中的期中分析相关统计要求
中期分析中一个最重要的统计问题,就是所谓的“Multiple Looks”的问题,其实Multiple Looks也是多重性问题之一。
小胖说统计 - 临床试验 - 2018-11-04
药品临床试验数据将受“第三方稽查”
药品临床试验是检验药品安全有效的重要关口,临床试验数据的真实性关乎性命,尤其重要。一些新药从研发到药品上市往往需要投入巨资,如果不把握好临床试验的重要关口,临床数据失真,往往导致上市后药效差,大大减低药品销售量,甚至退市。怎么才能提高临床试验质量?这都关系到哪些环节?临床试验数据不被国际认可新药上市要经过研发、药物临床试验、审批多个环节。药物临床试验是检验药品
bioon - 药品临床试验,第三方稽查 - 2013-10-24
临床试验中的意向性分析(ITT)原则介绍
近年来,术语Intention-To-Treat(ITT),在国外药品临床试验有关的期刊上出现的频率很高,受到广泛重视,得到许多实际应用。ICH-E9[1]对该原则的各种表述和不同用法进行了协调。
中国新药杂志 - ITT,临床试验 - 2013-06-09
高质量的医疗器械临床试验,有据可依
昨日,国家心血管病中心医学统计部主办的医疗器械临床试验法规、设计、质控及评价专题研讨会如期举行。国家心血管病中心党委书记李惠君在致辞中表示,医疗器械临床试验在临床治疗领域和卫生政策制定方面都发挥着重要
中国循环杂志 - 医疗器械临床试验 - 2017-08-11
药物临床试验中有效性指标的分类标准
典型的生物标记物通过试验( 如血脂中的低密度脂蛋白等) 或者仪器( 如血压计) 来测量取得的。多数生物标
MedSci原创 - 临床试验,有效性 - 2017-07-17
为您找到相关结果约500个