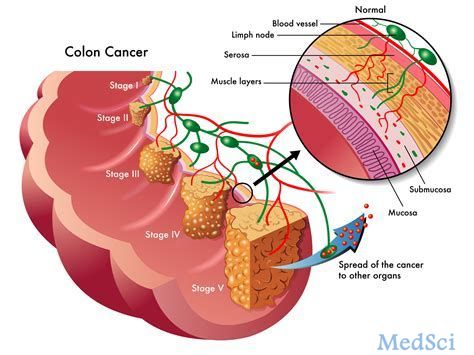
Lancet Oncol:帕唑帕尼加每周紫杉醇用于晚期卵巢癌的II期临床研究
背景:血管生成抑制用于卵巢癌治疗是一种有价值的治疗策略。帕唑帕尼对卵巢癌具有抗血管生成活性。我们评估针对于耐药或铂类难治的晚期卵巢癌患者,紫杉醇治疗时增加帕唑帕尼对疗效的影响。方法:这是在意大利11家医院进行的,开放标签的、随机的II阶段临床试验。患者包括铂类耐药或铂类难治的晚期卵巢癌先前接受大于二线化疗的患者,东部合作肿瘤组性能状态0 - 1,无残留的外周神经毒性。
MedSci原创 - 帕唑帕尼,紫杉醇,卵巢癌 - 2015-05-06
ESMO世界胃肠癌大会:murlentamab的II期临床研究结果
GamaMabs是一家临床阶段生物技术公司,专注于开发抗AMHRII的抗体药物,近日宣布,将在ESMO世界胃肠癌大会上公布murlentamab治疗转移性结直肠癌(mCRC)II期临床数据。
MedSci原创 - murlentamab,ESMO - 2019-07-07
辉瑞新冠口服药Paxlovid用于暴露后预防的II/III期临床失败
当地时间4月29日,辉瑞对外公布了一项研究其口服新冠药Paxlovid用于暴露后预防的II/III期临床(EPIC-PEP)研究情况,
网络 - 新冠病毒,Paxlovid - 2022-05-01
斑蝥素治疗常见疣的II期临床研究取得积极成绩
Verrica是一家皮肤病学医疗公司,致力于为皮肤病患者提供先进疗法,近日公布了其II期临床研究COVE-1的正面结果,以评估VP-102治疗常见疣的临床有效性。
MedSci原创 - 斑蝥素,疣,II期临床研究,VP-102 - 2019-06-27
II期临床研究FUZE评估Debio 1347治疗晚期实体瘤的疗效
Debiopharm International SA是瑞士的全球生物制药公司Debiopharm集团的一部分,近日宣布已启动FUZE研究,这是一项II期临床研究,旨在评估Debio 1347治疗携带FGFR融合的实体瘤(NCT03834220)。
网络 - Debio,1347,晚期实体瘤,FUZE研究 - 2019-02-18
Blood:Obinutuzumab、依鲁替尼和venetoclax联合靶向疗法用于慢性淋巴细胞白血病的1b期研究结果
现已证实包含抗CD20单克隆抗体obinutuzumab、Bruton酪氨酸激酶抑制剂依鲁替尼和Bcl2抑制剂venetoclax的靶向疗法用于慢性淋巴细胞白血病(CLL)患者具有显著的临床疗效,表明基于互补机制的联合疗法是理想的但是,将venetoclax与其他活性药物联合使用会增加肿瘤溶解综合征的风险,阻碍了该种联合方案的临床推广。Kerry A. Rogers等研究人员为将这种风险降至最低
MedSci原创 - 慢性淋巴细胞白血病,抗CD20单克隆抗体,依鲁替尼,Bcl抑制剂 - 2018-08-17
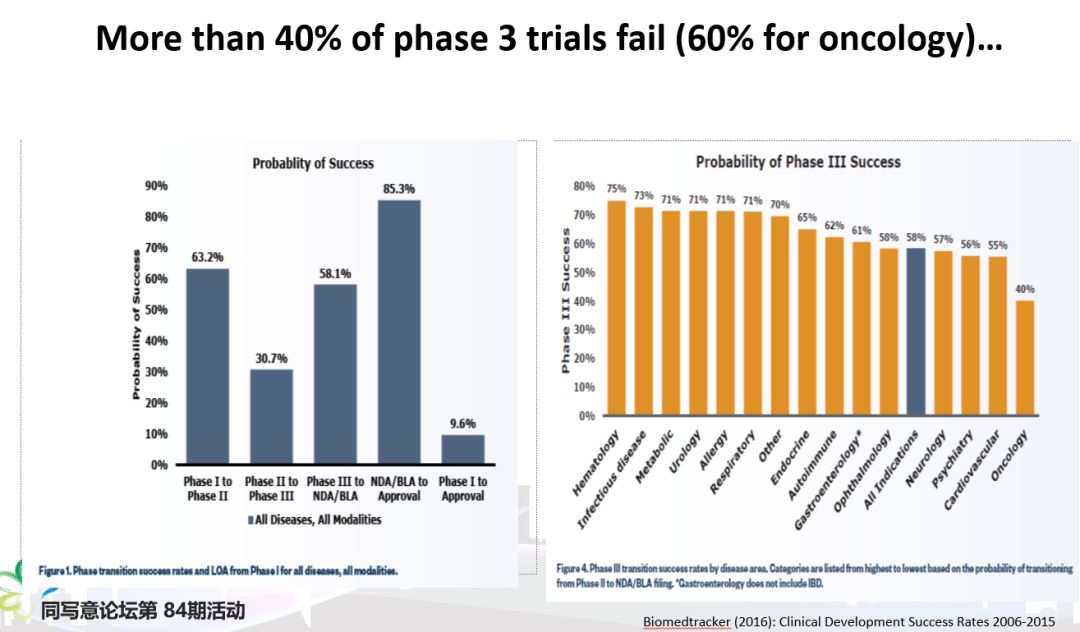
II期j临床试验成功而III期临床失败的案例教训
对比中国和美国医药的投资回报率,中国在20%以上,美国只有3%,目前中国的风险没有美国高。原因是美国创新药多,失败率高;而国内企业的临床试验,一方面是大多数还处于较早期的I期、II期临床阶段,进入III期较少,另一方面这些品类很多都是me-too或me-better,这类产品的临床成功率要高得多01临床试验是一个成功率很低的活动 新药临床试验是一个成功率很低的活动,药物从I期临床试
同写意 - 临床试验 - 2019-01-05
FOL-005的II期临床研究已接近尾声
制药公司Follicum今天宣布,在正在进行的IIa期临床研究中,FOL-005治疗脱发的所有患者均已完成治疗,该研究在200多例名男性患者中检查了不同剂量的候选药物FOL-005的安全性和治疗效果。
MedSci原创 - 脱发,FOL-005 - 2021-01-29
JR-141用于黏多糖贮积症II型全球3期临床试验取得进展
HS是评估CNS症状治疗有效性的生物标志物。临床研究还表明,pabinafusp alfa对CNS症状控制有积极作用。
罕见病信息网 - 黏多糖贮积症 - 2022-04-03
Idera公司着手银屑病用药IMO-3100II期临床研究
Idera医药公司将开始进行IMO-3100 II期临床研究,这是一种治疗自身免疫疾病(尤其是中重度斑块状银屑病)的铎受体(TLR)抑制剂。IMO-3100IMO-3100是一种免疫调节剂能够抑制TLR7和TLR9的活性,调节前炎性调节剂的分泌。 设置随机双盲安慰剂控制研究是为了评估IMO-3100单一治疗的药效和安全性。研究中,将对45名中重度斑块状银屑病患者随机接受IMO-3100或
中国医药123网 - 新药,FDA - 2012-04-25
药品II期临床研究方案格式
第一部分 药品Ⅱ期临床试验方案体例格式 一、方案指南: 试验概览 1. 题目封页 2. 申办者研究者签字页 3. 试验方案目录 4. 试验研究流程图 二、方案正文: 试验方案题目 1.
MedSci原创 - II期,药品,方案 - 2013-04-16
Lancet:临床II期试验表明LCZ696可用于难治性心力衰竭治疗(PARAMOUNT研究)
诺华公布的PARAMOUNT临床II期研究结果表明,针对射血分数保留型心力衰竭 (HF-PEF) 疾病患者,临床试验药物LCZ696可以显著降低与其发病率和死亡率相关的一种关键性预测因子,该药从而成为该领域的首个治疗药物。在欧洲和美国,有多达两千万人受到这种难治性疾病的困扰。诺华公布的数据发表于在德国慕尼黑召开的ESC2012年度大会(欧洲心脏病学会)上,并同
MedSci原创 - PARAMOUNT,LCZ696,心力衰竭 - 2012-08-28
ASCO 2018:同步放化疗联合pembrolizumab巩固治疗用于不可切除III期NSCLC的II期研究
同步放化疗联合pembrolizumab巩固治疗用于不可切除III期NSCLC的II期研究:Hoosier癌症研究网络LUN 14-179试验摘要编号:8500 时间:6月4日8:00 AM~11:00AM 专场:肺癌 形式:口头报告 背景:同步放化疗(CRT)是不可切除III期NSCLC的标准治疗方案。最近PACIFIC III 期临床研究显示,与安慰剂
MedSci原创 - NSCLC,Pembrolizumab - 2018-06-01
ASCO 2014:贝伐单抗加化疗用于直肠癌术前治疗的II期临床试验
对于局部晚期直肠癌(LARC),在高质量的全直肠系膜切除术(TME )中允许省略术前放化疗(PCRT),局部复发的情况不很常见。疾病转移的风险可部分通过磁共振成像(MRI)获得预测。然而术前放化疗并不能惠及所有的LARC患者,且与长期的患病率相关。 化疗( Cty )可减少局部复发的机会,但术后辅助化疗的依从性差,因此CRT后化疗的疗效已受到质疑。
dxy - 直肠癌,贝伐单抗 - 2014-05-23
MediciNova公司将开展MN-221急性哮喘临床II期研究
MediciNova公司完成MN-221II期研究的招募工作,将评估MN-221用于治疗急性哮喘加重的安全性和药效。 II期研究共招募176名哮喘患者,将设置随机、双盲对照。安慰剂控制研究的药效初级终末点是1秒用力呼气容积(FEV1)。次级终末点研究将评估住院率降低及多种临床价值。 公司计划于今年第二季度公布此次研究结果。 Medic
cyy123 - 新药,FDA - 2012-04-16
为您找到相关结果约500个