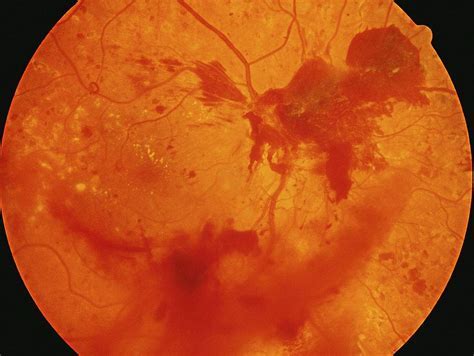
关于公开征求《糖尿病视网膜病变相关中药新药临床研发技术指导原则(征求意见稿)》意见的通知
经中心内部讨论并组织学术界专家研讨,已形成征求意见稿。现在中心网站予以公示,以广泛听取各界意见和建议。
国家药品监督管理局药品审评中心 - 糖尿病视网膜病变 - 2023-07-18
《中药新药用于胃食管反流病的临床疗效评价技术指导原则(试行)》
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,探索符合中医药特点的疗效评价标准,在国家药品监督管理局的部署下,药审中心组织制定了《中药新药用于慢性胃炎的临床疗效评价技术指导原则
国家药品监督管理局药品审评中心 - 胃食管反流病,中药新药 - 2022-12-27
成人2型糖尿病药物临床研发技术指导原则
为鼓励2型糖尿病药物临床研发,进一步规范临床研究设计和相关技术要求,在国家药品监督管理局的部署下,药审中心组织制定了《成人2型糖尿病药物临床研发技术指导原则》。
国家药品监督管理局药品审评中心 - 成人2型糖尿病,药物临床研发技术 - 2023-02-28
基于人用经验的中药复方制剂新药临床研发指导原则(试行)
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,在国家药品监督管理局的部署下,药审中心组织制定了《基于人用经验的中药复方制剂新药临床研发指导原则(试行)》。根据《国家药监局综合司
国家药品监督管理局药品审评中心 - 中药复方制剂,人用经验 - 2022-04-30
中药新药用于慢性胃炎的临床疗效评价技术指导原则(试行)
在国家药品监督管理局的部署下,药审中心组织制定了《中药新药用于慢性胃炎的临床疗效评价技术指导原则(试行)》。
国家药品监督管理局药品审评中心 - 慢性胃炎,中药新药 - 2022-12-27
与恶性肿瘤治疗相关中药新药复方制剂临床研发技术指导原则(试行)
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”注册审评证据体系研发符合中医
国家药品监督管理局药品审评中心 - 恶性肿瘤治疗,中药新药复方制剂 - 2023-04-18
国家药监局药审中心关于发布《糖尿病视网膜病变相关中药新药临床研发技术指导原则(试行)》的通告(2023年第55号)
本指导原则旨在丰富完善中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”中药注册审评证据体系研发符合中医药治疗优势和特点的糖尿病视网膜病变相关中药新药。
国家药品监督管理局药品审评中心 - 糖尿病视网膜病变 - 2023-11-14
中药新药用于胃食管反流病的临床疗效评价指导原则(征求意见稿)
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”注册审评证据体系研发符合中医药治疗优势和特点的、用于慢性胃炎、胃食管反
CDE - 胃食管反流病 - 2022-05-06
中药新药用于慢性胃炎的临床疗效评价指导原则(征求意见稿)
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”注册审评证据体系研发符合中医药治疗优势和特点的、用于慢性胃炎、胃食管反流病的中药新
CDE - 慢性胃炎 - 2022-05-06
为您找到相关结果约500个