FDA扩大了辉瑞/安斯泰来的Xtandi的适应症用以治疗非转移性前列腺癌
辉瑞和安斯泰来于2018年7月13日宣布,FDA已批准Xtandi的适应症外推,以治疗非转移性去势抵抗性前列腺癌(CRPC)。辉瑞/安斯泰来指出,该决定使得每日一次的雄激素受体抑制剂Xtandi成为美国批准的非转移性和转移性CRPC的第一种口服型治疗药物
MedSci原创 - Xtandi,辉瑞,安斯泰来 - 2018-07-16
前列腺癌治疗的最新进展:ORIC-101联合XTANDI的Ib期临床试验正式开始
临床前研究表明,新型糖皮质激素受体(GR)拮抗剂ORIC-101可能会抑制转移性前列腺癌患者对XTANDI(enzalutamide)的潜在耐药。
MedSci原创 - ORIC-101,前列腺癌,Xtandi,Enzalutamide - 2020-01-28
晚期前列腺癌药物Galeterone三期临床失败
这个临床试验比较Galeterone与阿斯特拉/Medivation的雄激素受体拮抗剂Xtandi对转移前列腺癌患者无进展生存期的改善,结果Galeterone未能显示能超过Xtandi,试验因此被终止
美中药源 - 晚期前列腺癌,Galeterone,三期临床失败 - 2016-07-27
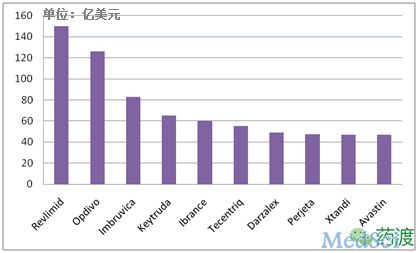
2022年最畅销的抗肿瘤药物TOP10
即使肿瘤免疫治疗药物上升,在2022年畅销的10种药物中大多数仍然是单克隆抗体药物,但是它们的状况却不容乐观,未来几年内将面临生物类似药的竞争。
药渡头条 - 抗肿瘤药物 - 2017-06-09
FDA批准阿斯利康/默克的PARP抑制剂Lynparza,治疗前列腺癌
Lynparza将疾病进展或死亡的风险降低了66%。
MedSci原创 - 前列腺癌,PARP抑制剂Lynparza - 2020-05-22
强生的雄激素受体拮抗剂Erleada,获得欧洲药品管理局批准治疗去势敏感型前列腺癌
强生公司(Johnson&Johnson)宣布其选择性雄激素受体(AR)拮抗剂Erleada(apalutamide),获得欧洲药品管理局批准,将适应症扩展用于治疗转移性去势敏感性前列腺癌(mCSPC),此次批准使该药物的适用人群再增加了100000例欧洲患者。
MedSci原创 - 强生,雄激素受体拮抗剂,Erleada,欧洲药品管理局,去势敏感型前列腺癌 - 2020-02-02
制药巨头疯抢新生物制药的逻辑:现有药品将失专利保护
全球的大型制药企业都在饿狼扑食般盯着新生的药物公司,这些药企大都在最新的生物制药、免疫疗法等领域有一两项成熟的药品,和正在第二、三试验阶段的产品管线,也被资本市场青睐。 尽管收购并购的趋势已经持续了十余年,如巨头辉瑞从2000年开始并购华纳兰伯特和法玛西亚,之后又并购惠氏,成为全球范围内数一数二的制药企业。争抢中小型制药公司的趋势却在最近一两年集中爆发,压力主要来自专利到期的威胁,和新领
经济观察报 - 制药巨头,生物制药,专利保护 - 2016-08-08
晚期前列腺癌新药研发竞争格局
前列腺癌是一种男性雄激素依赖型的肿瘤,雄激素会刺激前列腺癌细胞的生长,诱使疾病进展。转移性前列腺癌患者常用药物去势治疗(ADT),最初应答率能达80%-90%,但几乎所有患者都会在去势治疗后最终进展为转移性去势抵抗性前列腺癌(mCRPC)。
医药魔方 - 前列腺癌,药物研发,市场格局 - 2019-10-22
Medivation化身“香饽饽” 默沙东或加入竞购大军?
随着生物医药产业竞争的日趋激烈。兼并收购已经成为医药巨头扩充研发实力、获得新产品的重要途径之一。最近,据路透社报道,有消息人士表明,美国默沙东公司有一项加入竞购肿瘤药物研发公司Medivation的行列当中。而默沙东并不是唯一一个与Medivation公司传出绯闻的生物医药公司。 消息来源表示,自从本月默沙东在肿瘤免疫疗法领域最大的竞争对手施贵宝公司新药Opdivo在一项治疗非细小性细胞肺癌的
生物谷 - 默沙东 - 2016-08-22
Forbes:2016年抗癌征途上的大事记
导读:近日,Forbes网站刊出“2016年度抗癌8大里程碑事件”,回顾了过去一年我们在癌症治疗领域所作出的努力和成绩,列举了“癌症登月计划”、“21世纪治愈法案”以及艾伯维、辉瑞、Kita、BMS等制药巨头的一系列新动态。1月12日:美国副总统拜登授命领导 “癌症登月计划”图片来源: MANDEL NGAN/AFP/Getty Images2016年年初,美国总统巴拉克•奥巴马于在国情咨文中
生物探索 - 抗癌征途 - 2017-01-04
JAMA:FDA审批新药速度过快或存在安全隐患
FDA药物研究与评估中心负责人指出,医学团体和公众敦促FDA加快新药审批流程,而不是更谨慎地评估一种新药。 两位药物安全专家表示,FDA致力于加快审批预防中风、癌症和多发性硬化症新药上市,但这些新药没有经过全面的安全分析。 药物安全专家托马斯·摩尔(T
网络 - FDA,新药,安全隐患 - 2012-09-20
Clovis的Rubraca超越了多个PARP抑制剂竞争对手,在前列腺癌领域获得FDA的优先审查
FDA刚刚开始对Rubraca(rucaparib)进行为期六个月的优先审查,判决将于5月15日之前完成,用作BRCA1 / 2突变的复发或转移的去势抵抗性前列腺癌(CRPC)成人的单一疗法。BRCA1 / 2基因突变是mCRPC患者最常见的缺陷。
MedSci原创 - Clovis,rubraca,PARP抑制剂,前列腺癌,FDA优先审查 - 2020-01-17
前列腺癌药物Jevtana获英国NICE支持
近日,英国药物成本与疗效管理部门NICE在与赛诺菲经历了一番价格上的谈判后,终于同意推荐其前列腺癌药物Jevtana (cabazitaxel)。 2012年,NICE曾经拒绝批准Jevtana (cabazitaxel)在英国和威尔士地区使用,然而还是有550名前列腺癌患者通过癌症药物基金(Cancer Drugs Fund,CDF)成功获得该药物治疗,直到去年该药
不详 - 赛诺菲,前列腺癌 - 2016-04-26
NICE最终指南推荐恩杂鲁胺用于前列腺癌
恩杂鲁胺也被称作Xtandi,由安斯泰来制药生产。 在之前的草案建议中,NICE并未推荐恩杂鲁胺用于已应用阿比特龙(Abiraterone)治疗过的患者人群。
MedSci原创 - 前列腺癌,恩杂鲁胺,NICE - 2014-05-20
为您找到相关结果约47个