CFDA发布公告修订《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》
一、《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》修订的总体思路和原则是什么? 依据《条例》设定的原则和要求对《办法》进行修订。修订的总体思路与《条例》修订的总体思路保持一致,以分类管理为基础,以风险高低为依据,确定医疗器械注册与备案的具体要求。医疗器械注册是一项行政许可制度,是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其
CFDA - CFDA - 2015-02-09
国家卫健委发布乡村医生证再注册通知
刚刚,国家卫生健康委发布《关于做好乡村医生执业证书有效期满再注册工作的通知》,村医必看!刚刚,国家卫生健康委办公厅发布了《关于做好乡村医生执业证书有效期满再注册工作的通知》(下文简称《通知》),要求地方各级卫生健康行政部门对获得乡村医生执业证书满5年的村医进行执业再注册工作。
基层医师公社 - 卫健委,乡村医生,注册 - 2019-02-21
26天拿证 医疗器械注册人制度产品在上海落地
医疗器械注册人制度改革后,符合条件的医疗器械注册申请人可以单独申请注册证,然后委托给有资质和生产能力的生产企业。
新华网 - 医疗器械,注册人,制度 - 2018-02-27
CFDA征求意见:计划收回省局大部分药品注册受理权
为落实《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号),将现由省级食品药品监管部门受理、食品药品监管总局审评审批的药品注册申请,调整为食品药品监管总局集中受理。国家食品药品监督管理总局起草了《关于调整药品注册受理工作的公告(征求意见稿)》,现向社会公开征求意见。
CFDA - 药品注册,CFDA - 2017-09-16
CFDA拟放宽II、III类注册检验要求,企业可以自主检验
根据械注[2017] 165号文件,总局医疗器械注册管理司将调整医疗器械检验相关工作。这次调整总体来说对企业是利好的,也是我国医疗器械注册监管迈向国际化的一步。
CIRS医疗器械监管动态 - CFDA,自主检测 - 2017-06-29
CFDA:加速境外新药国内上市,化药注册检验调整为监督抽样
6月22日,国务院新闻办公室召开政策例行吹风会。记者了解到,近年来我国在加快境外上市新药审评审批方面做了大量工作。数据显示,近十年来,在美国、欧盟、日本上市的新药共有415个,277个已经在中国上市和正在进入申报和临床试验阶段。其中,76个已经在中国上市,201个目前处在中国的临床试验和申报阶段。 从临床审批和上市审批的总时限看,我国为390天,美国为330天,欧盟为270天,日本为330天
MedSci原创 - 新药,化药 - 2018-06-23
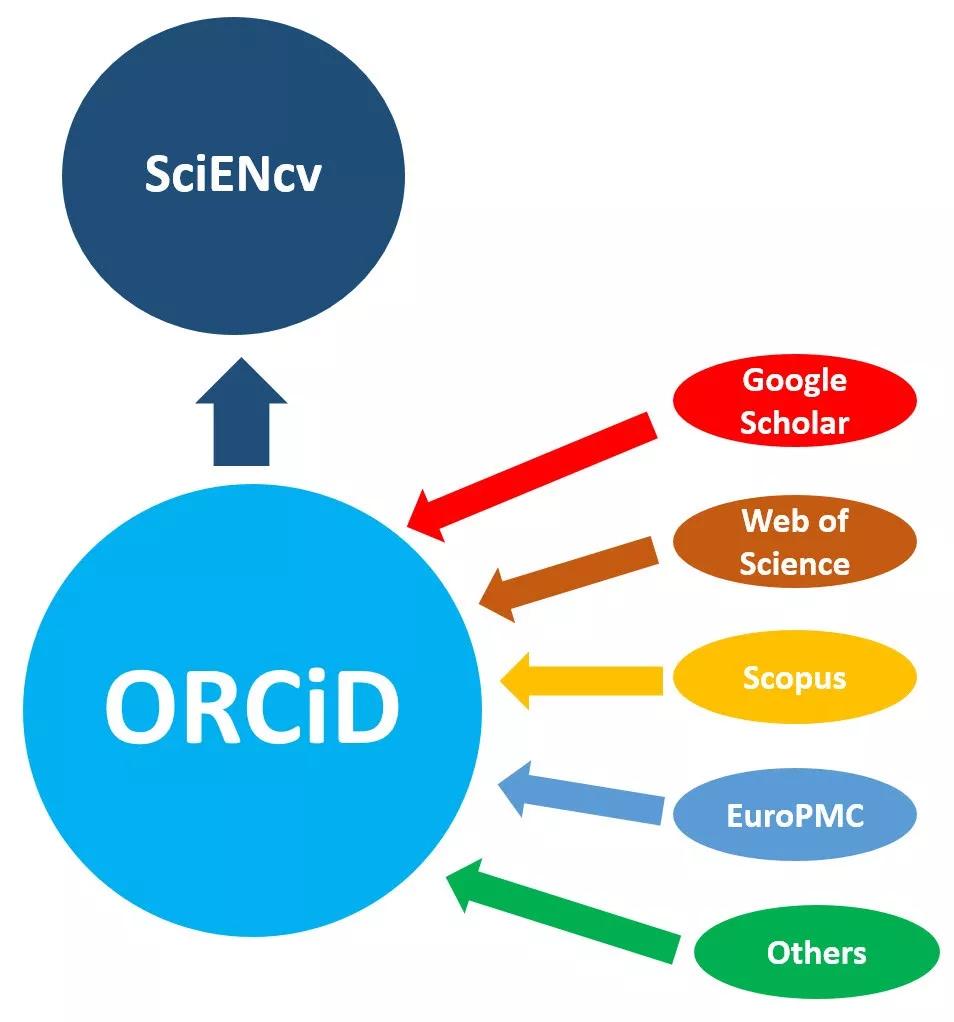
学术身份证——ORCID和ORCID iD,如何注册、获取并投稿使用?
这里就需要用到一个【学术身份证】——即ORCID,你所有的国外投稿都是需要用到这样一个系统的。
MedSci原创 - ORCID - 2020-11-02
国家卫健委发布乡村医生证再注册通知 村医必看
国家卫健委发布《关于做好乡村医生执业证书有效期满再注册工作的通知》,村医必看!国家卫健委办公厅发布了《关于做好乡村医生执业证书有效期满再注册工作的通知》(下文简称《通知》),要求地方各级卫生健康行政部门对获得乡村医生执业证书满5年的村医进行执业再注册工作。
基层医师公社 - 国家卫健委,乡村医生证,再注册 - 2019-02-21
CFDA再出重拳:6个药品注册申请不予批准!两家医院被立案调查!
总局关于7家企业6个药品注册申请不予批准的公告(2016年第92号) 根据《关于开展药物临床试验数据自查核查工作的公告》(国家食品药品监督管理总局公告2015年第117号)和《关于开展药物临床试验机构自查的公告》(国家食品药品监督管理总局、国家卫生计生委、总后勤部卫生部公告2015年第197号)要求,国家食品药品监督管理总局对部分已提交自查资料的药品注册申请进行了临床试验数据现场核查,现将有
MedSci原创 - 注册,医院 - 2016-04-29
CFDA 发布胎儿染色体非整倍体检测试剂盒注册技术审查指导原则
本指导原则旨在指导注册申请人对胎儿染色体非整倍体(T21、T18、T13)检测试剂盒(高通量测序法)注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。本指导原则是针对该类试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
CFDA - CFDA,胎儿染色体,试剂盒 - 2017-04-07
医疗器械再敲警钟!罗氏等13家被通报,2家医院被处罚
上个月,河北省临漳县妇幼保健站因使用未经注册的医疗器械而收到了1765.4万元的行政处罚,给整个医疗器械行业敲了警钟。近日,山东淄博的两家医院使用过期医疗器械被通报并被没收和罚款,CFDA通报了13家医疗器械的违规行为,这些再次给医疗器械行业一个警告!
生物探索 - 医疗器械,CFDA - 2017-02-16
进口药注册提速 国人能更快吃上新药吗?
近日,CFDA发布“进口药品注册审评审批”的相关征求意见稿,若落地将提升药品进口再注册效率,但有业内人士表示,此项改革仅涉“皮毛”......
健康点healthpoint - 进口药,注册提速 - 2018-02-23
“生物医用材料研发与组织器官修复替代”重点专项2016年度申报指南
随着生命科学、材料科学及物理、化学等学科的发展,特别是组织工程技术的发展,推动人体组织器官的修复替代进入了一个崭新的阶段。在我国人口老龄化的加速演进的新形势下,加快研发生物医用材料和组织工程技术及产品,对于培育我国战略新兴产业,转变经济发展方式,实现科技惠及民生具有重要战略意义。 为全面落实《国家中长期科学和技术发展规划纲要(2006-2020年)》的相关任务,按照国务院《关于深化中央财
科技部 - 生物医用材料,组织修复,申报指南 - 2016-03-09
大批挂证药师曝光!今年还有多少“影子药师”现形?
近日,山东省食品药品监督管理局发布《关于药品经营企业中执业药师“挂证”行为检查情况的通告(2018年第8号)》(以下简称《通知》)。《通知》指出,为强化药品经营企业监督管理,规范药品经营企业配备使用执业药师的行为,山东省局加大了对执业药师“挂证”行为的检查力度,现将检查中发现的“挂证”行为予以通告,共有72名执业药师被曝光。
21世纪药店 - 挂证药师,曝光 - 2018-01-24
为您找到相关结果约500个