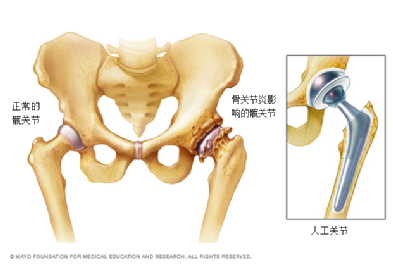
药监手中最锋利的一把刀:从狂犬病疫苗事件看飞行检查
长生生物在飞行检查中被发现,在冻干人用狂犬病疫苗生产过程中存在记录造假等严重违反药品GMP行为,引发众多连锁反应。在创新药、仿制药审评审批加速政策逐步落地的大背景下,药品的安全质量监管重心越来越从上市前向上市后转移,飞行检查的力度明显加大。2017年我国药品生产企业飞行检查57次;药品境外现场检查51个品种。仅在2017年,全国收回药品GMP证书就有157张。长生生物此次“踩雷”无疑是“飞检”趋严
健康点healthpoint - 药监,飞检 - 2018-07-18
盘点这10年CFDA为“孤儿药”做出的一系列改革
孤儿药的研究热情曾一度受“低发病率”“投资回报率”“研发难度大”、“适用患者少”等因素影响,不少制药企业也因此不愿涉足该领域。现在,随着社会认知度提高、支持政策出台、诊断及治疗手段增多,罕见病药物开发风向正在转暖。在“第十二届国际罕见病与孤儿药大会暨第六届中国罕见病高峰论坛”上,来自于国家食品药品监督管理总局药品审评中心的生物制品临床部部长高晨燕和化药临床一步高级审评员张杰从国家政策层面跟大家
生物探索 - CFDA,孤儿药,改革 - 2017-09-13
三问宫颈癌疫苗:二价四价够用吗
国内可以预约接种的二价、四价疫苗,已经退出了美国市场,不是因为安全性或疫苗效力问题,而是价格问题。目前世界卫生组织对这3种疫苗的推荐没有偏好。
人民日报 - 宫颈癌,疫苗 - 2018-01-31
国家药监局曝光“飞检”计划 201家药企将被查
6月4日,国家药品监督管理局发布《关于开展2018年国家药品跟踪检查有关事宜的通告(2018年第35号)》。国家药监局要检查201家药企国家药监局制定的《2018年药品跟踪检查计划》,涵盖201家药品生产企业。包括2017年国家抽检发现问题较多的企业38家,疫苗类生物制品生产企业40家,血液制品生产企业28家,麻醉、精神药品和药品易制毒类生产企
赛柏蓝 - 飞检计划 - 2018-06-05
CFDA明确一致性评价申报要求,通过一致性评价标识出炉
8月25日,CFDA官网发布《关于仿制药质量和疗效一致性评价工作有关事项的公告》(2017年第100号),该文件意见稿曾于6月9日挂网征求意见。
CFDA官网 - CFDA,申报要求,一致性评价,标识 - 2017-08-28
《药品注册管理办法》9年后最重大修改(附修订稿 VS 2007版)
7月25日,CFDA通过官网发布《药品注册管理办法(修订稿)》,向社会公开征求意见,时间为一个月。关于此修改稿的意见可于8月26日之前反馈给CFDA。时隔九年,与上一版2007年《药品注册管理办法》相比较,中国医药行业的情况发生了巨大的变化,药品注册管理工作的流程和范围需要进行与时俱进的重新调整:两万件药品注册申请积压待审,运动式的削峰药审无法真正改变这种积压的现状;药品僵尸文号盛行,如何从注
E药经理人 - 药品,注册管理 - 2016-07-26
国家药监局:201家药企将被查
6月4日,国家药品监督管理局发布《关于开展2018年国家药品跟踪检查有关事宜的通告(2018年第35号)》。
赛柏蓝 - 药企,飞行检查,药监局 - 2018-06-05
我国仿制药渐入国际主流市场 一致性评价成关键
近日,由国家食品药品监督管理总局和广西壮族自治区人民政府共同主办的第四届中国—东盟药品合作发展高峰论坛暨西太平洋地区草药协调论坛在南宁举办。本届论坛以“提升仿制药质量”为主题,共同探讨药品监管的国际发展之路,谋求打造中国药品监管部门与东盟以及一带一路国家的监管合作平台。作为全球重要的医药市场,中国是最大的仿制药生产国,仿制药成为拉动全球药品销售增长的主要力量。但是,目前我国仿制药发
中国网 - 仿制药,国际主流市场,一致性评价 - 2016-12-24
2018年CFDA 十大热点动向!
2018 年,我们告别了 CFDA,迎来了全新的 NMPA,药物审批速度也在逐渐加快,四家企业的试剂盒获得批准,很多事情正在发生。
转化医学网 - CFDA,NMPA - 2018-12-20
31条修改,《药品注册管理办法》再次发布征求意见稿
10月15日,中国政府法制信息网公布:国家市场监督管理总局关于《药品注册管理办法(征求意见稿)》(以下简称新版)《药品生产监督管理办法(征求意见稿)》《药品经营监督管理办法(征求意见稿)》公开征求意见的通知2019年8月26日,《药品管理法》经第十三届全国人民代表常务委员会第十二次会议审议通过,自2019年12月1日起施行。为建立科学、严格的药品监督管理制度,
医谷 - 药品注册管理办法,征求意见 - 2019-10-18
基因测序重启:狼来了还是粮来了
最近,两款来自华大基因的仪器成为中国监管部门首次批准注册的第二代基因测序诊断产品。对此,外界褒贬不一。 今年2月的一纸禁令,让中国无创基因产前检测市场突然陷入“休克”。最近,国家食品药品监督管理总局在官网上发布消息称,已批准BGISEQ-1000基因测序仪、BGISEQ-100基因测序仪和胎儿染色体非整倍体检测试剂盒、胎儿染色体非整倍体检测试剂盒医疗器械的
中国科学报 - 基因测序,临床应用 - 2014-08-14
卫计委:关于加强临床使用基因测序相关产品和技术管理的通知
各省、自治区、直辖市食品药品监督管理局、卫生计生委(卫生厅局),新疆生产建设兵团食品药品监督管理局、卫生局: 包括产前基因检测在内的基因测序相关产品和技术属于当代前沿产品和技术研究范畴,涉及伦理、隐私和人类遗传资源保护、生物安全以及医疗机构开展基因诊断服务技术管理、价格、质量监管等问题。目前,基因测序相关产品和技术已由实验室研究演变到临床使用,对此,国务院有关部门高度重视。为保证公众使用基因测序诊
医药网 - 国家食品药品监管总局办公厅,国家卫生计生委,临床,基因测序 - 2014-02-17
为您找到相关结果约500个