云顶新耀:立于医学创新之顶,放眼举世新药
自2018年港交所修改《上市规则》引入18A章,允许未盈利生物科技公司赴港上市以来,未盈利的生物医药公司就成为港股的重要焦点之一。今年虽然受新冠疫情影响,却也未打消医疗生物科技股的赴港热情。截止目前不
医药魔方 - 医学创新,举世新药,C轮融资 - 2020-11-03
2021年上半年盘点:FDA批准抗肿瘤药物汇总
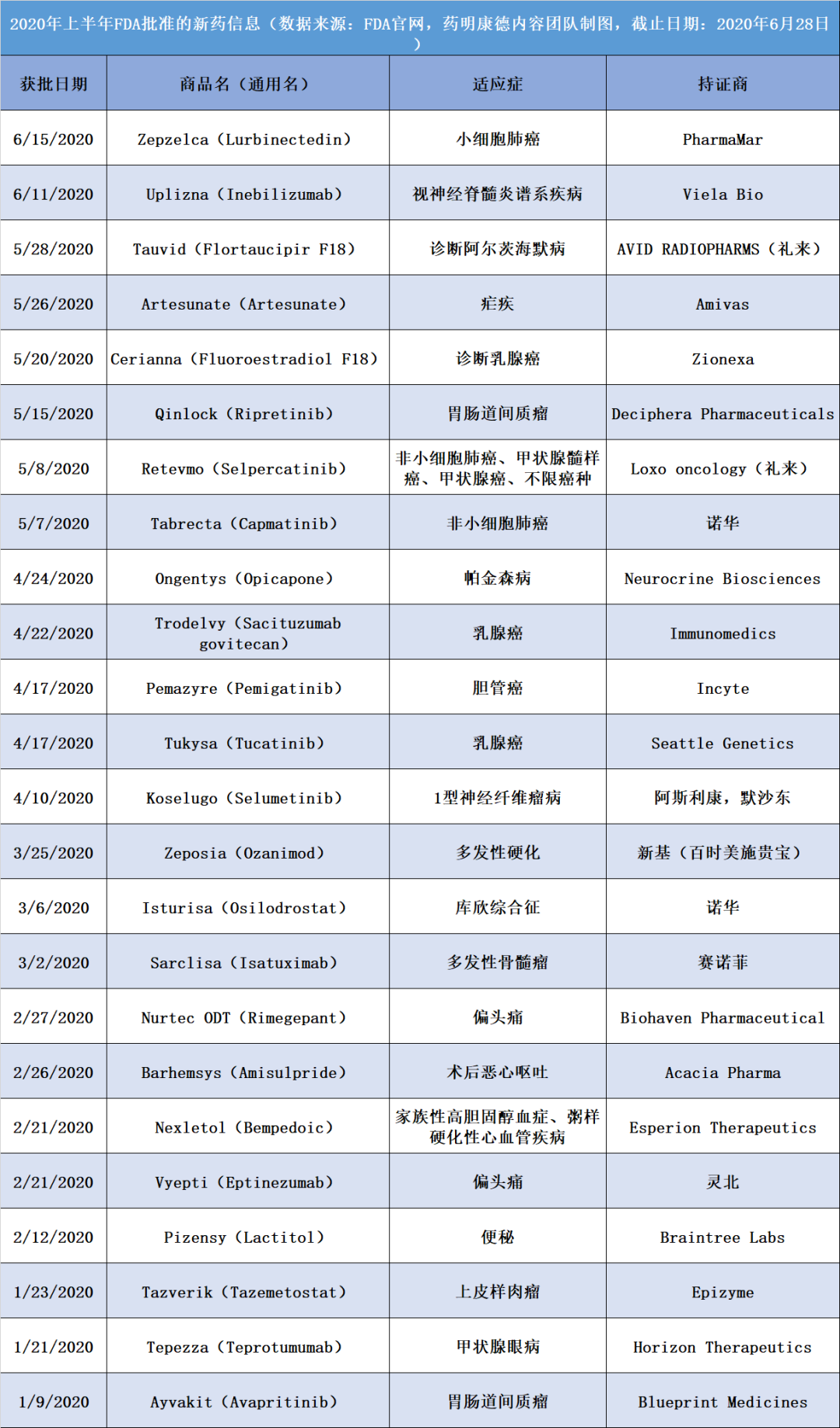
2021年上半年,FDA批准涉及22种药物的35个适应症(其中加速批准适应症14个)。FDA批准了共22款抗癌新疗法,包括靶向,免疫检查点抑制剂,过继性细胞免疫疗法等等,覆盖了几乎全部的癌症种类,值得
网络 - FDA - 2021-07-04
FDA提前4个月加速批准DS-8201治疗HER2低表达乳腺癌,超6成乳腺癌患者均能受益
当地时间2022年8月5日,美国FDA批准 Enhertu (fam-trastuzumab-deruxtecan-nxki,T-DXd,DS-8201,德喜曲妥珠单抗,)新适应症,用于治疗无法切除或
MedSci原创 - 乳腺癌,T-DXd,HER2低表达 - 2022-08-07
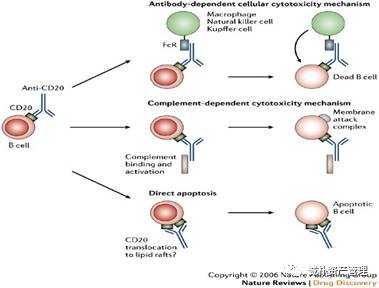
抗CD20单抗科普:从一代的利妥昔到三代的阿妥珠
大家最熟悉的抗CD20单抗是来自罗氏的利妥昔(商品名: 美罗华),自从问世以来,利妥昔和化疗药物的联用成为了治疗某些特定类型的非霍奇金淋巴瘤的标准方案,但以CD20为靶点的单抗药物远不止利妥昔,只是利
网络 - CD20单抗 - 2020-05-07
2020年最新抗体报告:36款单抗尽收眼底
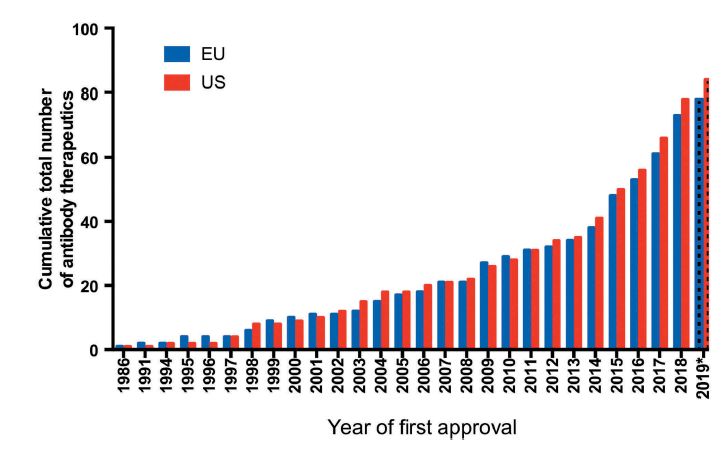
12月26日,来自美国抗体协会等机构的4位科学家在mAbs上发表了题为“Antibodies to watch in 2020”的年度报告[1]。报告汇总分析了2019年在美国和欧盟监管下获批的抗体疗法,以及截至2019年11月处于后期临床研究的候选抗体药物。 图1 1986–2019年,在美国或欧盟首次获批的抗体疗法的累积数量(图片来源:mAbs) 报告称,2010-20
医药魔方 - 单抗,抗体 - 2020-02-05
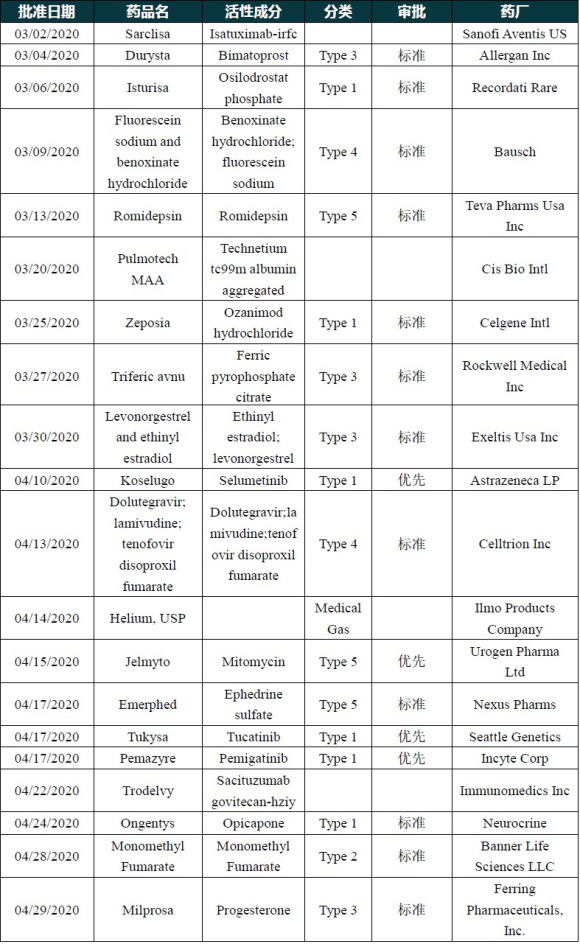
4月份,FDA和NMPA批准了哪些新药?
2020年1-4月批准了42个NDA/BLA申请新药,包括5个生物药,12个新分子实体(Type 1),7个新剂型(Type3),5个新组合(Type4),7个新配方或新制造商(Type5),2个已上
MedSci原创 - FDA,NMPA - 2020-05-07
Nat Rev Clin Oncol:探索下一代抗体偶联药物(ADC)
ADC的治疗潜力巨大,但要实现这一潜力,需要克服几个关键挑战,如耐药性、肿瘤内和瘤瘤间异质性以及TRAE的风险。新兴的ADC模式,包括双特异性和双载荷ADC,显示出解决耐药性和肿瘤异质性的潜力
小药说药 - 伊立替康,抗体偶联药物,ADC类药物,金盏花素 - 2024-01-21
ADC有效载荷的研究前沿
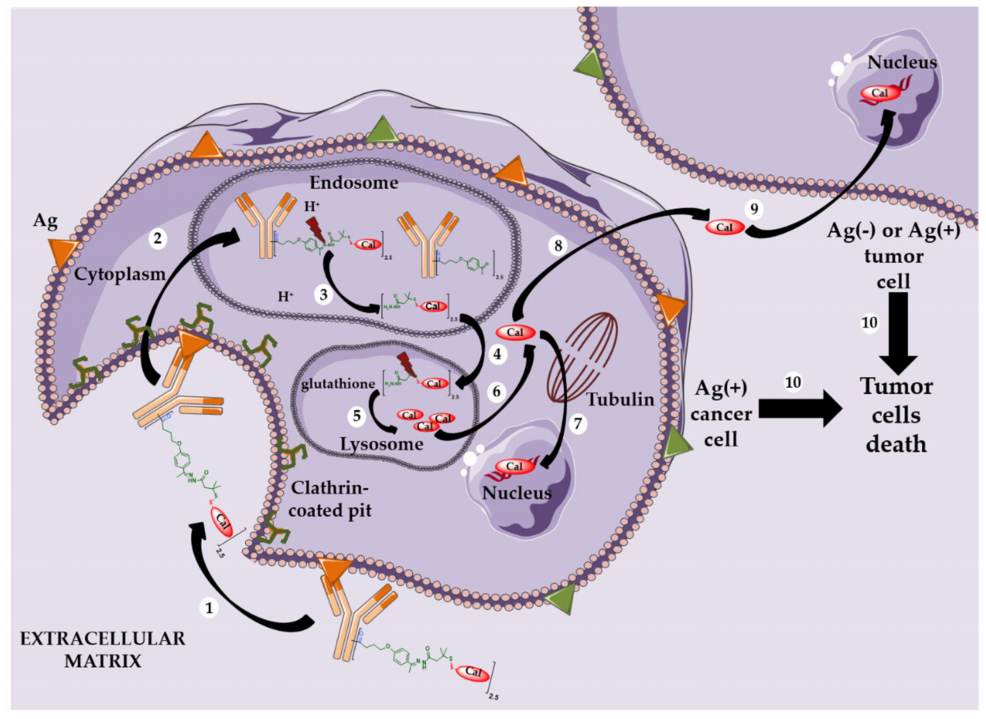
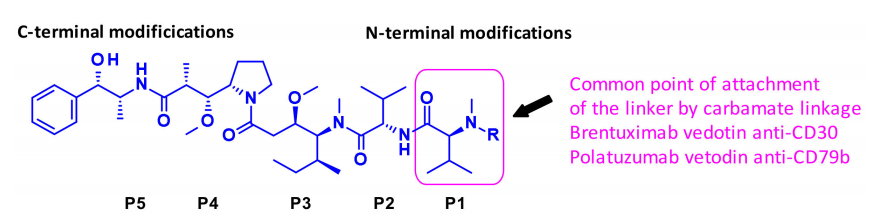
抗体偶联药物(ADC)是由靶向特异性抗原的单克隆抗体与小分子细胞毒性药物通过连接子链接而成,兼具传统小分子化疗的强大杀伤效应及抗体药物的肿瘤靶向性。
小药说药 - 微管破坏药物,美登素衍生物(DM2,DM4),微管溶素 - 2022-12-01
为您找到相关结果约27个