美国FDA受理君实生物重新提交的特瑞普利单抗治疗鼻咽癌上市申请
FDA已将特瑞普利单抗BLA的目标审评日期定为2022年12月23日。 如若获批,特瑞普利单抗将成为美国首个且唯一用于鼻咽癌治疗的肿瘤免疫药物。
网络 - 鼻咽癌,美国FDA,特瑞普利单抗 - 2022-07-07
基石药业将艾伏尼布片在大中华地区和新加坡的独家权益出售给施维雅
择捷美®联合氟尿嘧啶类和铂类化疗药物用于一线治疗不可切除的局部晚期、复发或转移性ESCC的新适应症上市申请已获NMPA批准
网络 - 2023-12-21
Sirtex Medical和China Grand Pharmaceutical宣布SIR-Spheres Y-90树脂微球获得NMPA认可
SIR-Spheres®Y-90树脂微球的新药申请(NDA)已获得中国NMPA的批准。
MedSci原创 - 肝癌,转移性结直肠癌,NMPA,SIR-Spheres Y-90树脂微球 - 2020-11-29
对比药品关联审评审批政策 明确法规趋向
2019年7月16日,国家药监局发布《关于进一步完善药品关联审评审批和监管工作有关事宜的公告》(2019年 第56号,简称"正式稿",下同),这对应的是2019年4月4日发布的国家药监局综合司再次公开征求《关于进一步完善药品关联审评审批和监管工作有关事宜的公告(征求意见稿)》(简称"征求意见稿",下同)。通过比较两者,可以明确政策法规的趋向。
CPhI制药在线 - 药品关联审批,法规政策 - 2019-07-31
安全性动态跟踪罗沙司他,科学审评加速本土可及
中国国家药品监督管理局(NMPA)先于全球其他国家批准罗沙司他用于慢性肾脏病透析患者的贫血治疗,该药在中国的首发上市,意味着我国首次成为全球首批First-in-class原创新药的国家,这在新药注册史上具有里程碑意义目前,罗沙司他已经完成全球Ⅲ期临床研究,试验评估的心血管(CV)安全性汇总分析结果,将作为该药向美国食品药品监督管理局(FDA)提交申报
医药经济报 - 罗沙司他 - 2019-07-03
天境生物半年报:将提交CD38抗体上市申请,启动“超级抗体”研发
8月31日,天境生物公布了2021年上半年业绩及公司近况。根据报告,天境生物上半年核心研发投入费用为人民币4.8亿元。与此同时,该公司产品管线也取得了13个研发关键里程碑,
天镜生物 - PD-L1 - 2021-09-02
双特异性抗体KN026与KN046联合疗法获美国FDA孤儿药资格认定,用于治疗胃癌及胃食管连接部癌
12月23日,康宁杰瑞生物制药宣布,公司自主研发的双特异性抗体KN026(抗HER2双特异性抗体)与KN046(PD-L1/CTLA-4双特异性单域抗体)联合疗法获美国食品药品监督管理局(FDA)授予
医药魔方 - 胃癌,胃食管连接部癌 - 2020-12-23
君实生物特瑞普利单抗治疗食管癌获得美国FDA孤儿药资格认定
君实生物自主研发的抗PD-1单抗药物特瑞普利单抗用于治疗食管癌(EC)获得美国食品药品监督管理局(FDA)授予的孤儿药资格认定(Orphan-drug Designation)。
网络 - 食管癌,孤儿药认定,君实生物,特瑞普利单抗注射液(拓益®) - 2021-11-16
2020肿瘤新药数据卡——恩沙替尼
2020年,国家药品监督管理局(NMPA)共批准16种肿瘤新药。基于医药魔方NextPharma数据库、NextMed数据库及公开信息,医药魔方Med特别推出“肿瘤新药数据卡”,为大家介绍国内上市肿瘤
医药魔方 - 肿瘤,恩沙替尼 - 2021-04-30
盘点 | 2019年3月全球获批新药情况
一、FDA获批上市药品动态监测 根据火石创造数据库数据显示,截至2019 年 3月FDA共批准94个药品上市,其中NDA药品为10个,BLA药品为1个,ANDA药品为83个。1.jpg 表1 FDA批准的NDA和BLA药品 在上述批准的10种NDA品种中,西尼莫德、BREXANOLONE和SOLRIAMFETOL为新分子实体(N
火石创造 - 新药 - 2019-04-10
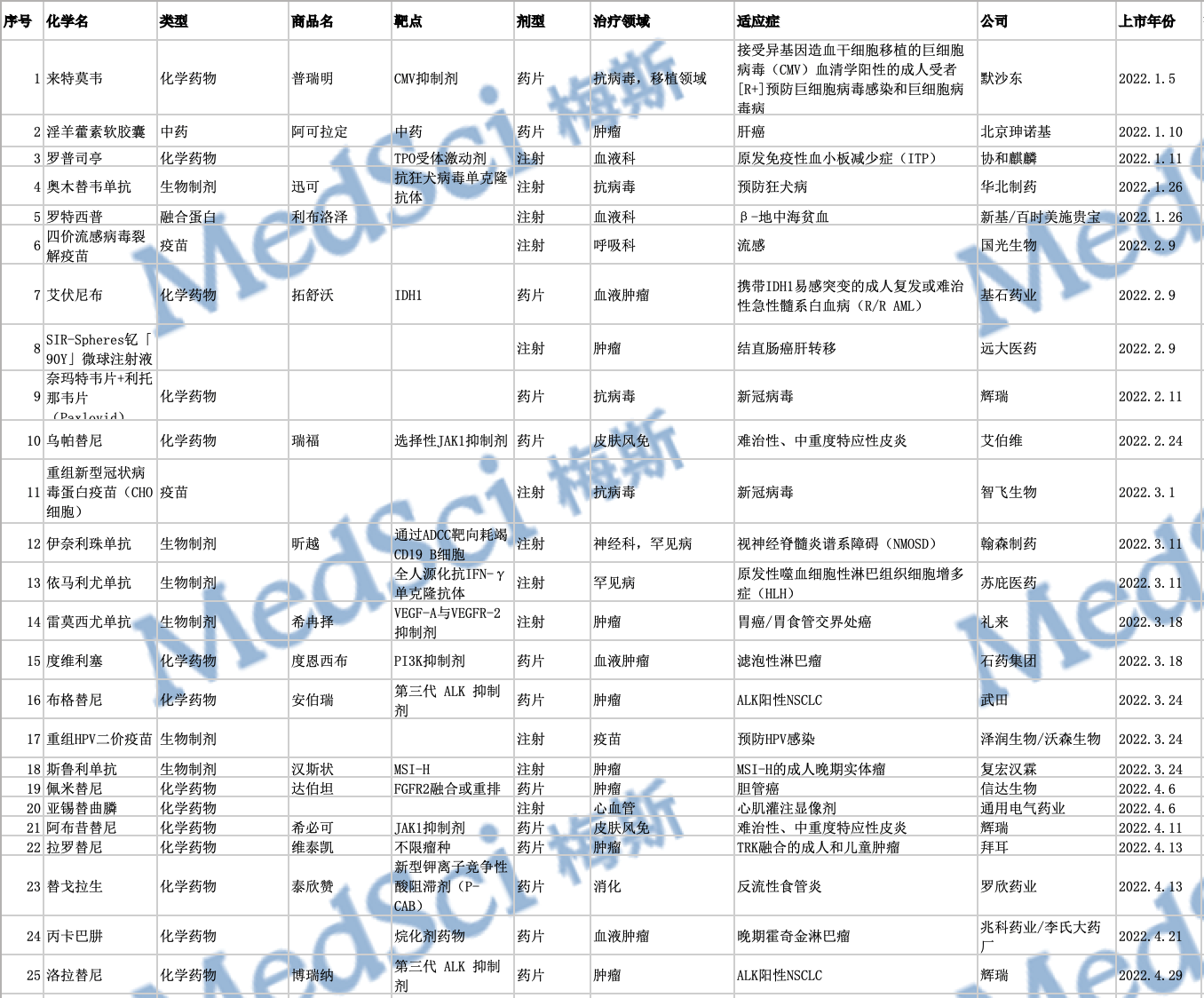
2022年中国NMPA批准上市的50款创新药物
2022年,中国药监局(NMPA)共批准了50款新药,其中进口新药有30款,国产新药有20款。从药物类型上看,包括28款化学药、13款生物药、5款疫苗以及4款中药。数量与2019年批准了51款新药,2
MedSci原创 - 创新药物,NMPA - 2023-01-13
君实生物特瑞普利单抗治疗小细胞肺癌获得美国FDA孤儿药资格认定
这是特瑞普利单抗获得的第五项孤儿药资格认定,此前特瑞普利单抗治疗黏膜黑色素瘤、鼻咽癌、软组织肉瘤及食管癌已分别获得FDA孤儿药资格认定。
网络 - 小细胞肺癌,君实生物,FDA孤儿药,特瑞普利单抗注射液(拓益®) - 2022-04-14
2014上半年FDA批准的新药
2014年已走过一半时间,仅从FDA的新药审批结果来看,医药行业吹来暖风。2014上半年FDA批准了18个新药,相比2013上半年有明显增长。由于2012年小型制药企业递交新药上市申请的数量激增,FDA的新药批准数量在2012年达到了39个的历史高点。随着2013年FDA批准的新药数量急剧下降至27个,人们也开始对全球新药研发
生物探索 - 新药,FDA - 2014-07-02
为您找到相关结果约500个