抽动障碍中药临床试验设计与评价技术指南
《抽动障碍中药临床试验设计与评价技术指南》为中华中医药学会标准化项目《儿科系列常见病中药临床试验设计与评价技术指南》之一。
药物评价研究 - 神经心理,抽动障碍,儿童抽动障碍 - 2022-01-22
小儿积滞中药临床试验设计与评价技术指南
《小儿积滞中药临床试验设计与评价技术指南》为中华中医药学会标准化项目《儿科系列常见病中药临床试验设计与评价技术指南》之一。其目的是以临床价值为导向,主要是在中医病证研究模式下,重点讨论具有病种、儿童和
药物评价研究 - 小儿积滞 - 2023-02-09
手足口病中药临床试验设计与评价技术指南
《手足口病中药临床试验设计与评价技术指南》为中华中医药学会标准化项目《儿科系列常见病中药临床试验设计与评价技术指南》之一。
药物评价研究 - 手足口病,感染病病毒组 - 2022-01-22
Ⅰ期临床试验病历记录要求与书写规范实践共识
本共识旨在为Ⅰ期临床试验病历的书写提供实践参考。人体生物利用度或生物等效性研究可参照本共识。
中国医药导刊 - I期临床试验,病历记录 - 2024-01-05
肿瘤药物临床试验合同框架与关键条款专家共识
因肿瘤药物临床试验复杂多样,使得临床试验合同条款众多,条款之间关联复杂.为了促进合同各方认真履行职责、有效维护各方权利、切实保护受试者权益,中国抗癌协会科技服务部临床试验稽查专家组与临床研究管理学专
癌症 - 肿瘤药物,抗肿瘤药物,肿瘤药物研发 - 2022-11-05
真实世界研究如何应用于临床试验
制药产业中,临床试验与药品的实际应用有着根本差别,这种差别会造成治疗和安全性漏洞,不利于药品生产商的重大投资。美国国会在官方网站上公布了《21世纪治愈法案》,法案中提出利用“真实世界证据”取代传统临床试验进行扩大适应症的批准。
国际药政通 - 真实世界研究 - 2018-04-13
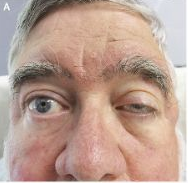
NEJM:冰敷试验与重症肌无力-案例报道
会诊医师对其左眼部位进行冰敷试验(如图B),2分钟后上睑下垂症状明显有所改善,表明试验结果为阳性(如图C)。因此,初步怀疑为重症肌无力眼肌麻痹。在本案例中,冰敷试验可作为诊
MedSci原创 - 冰敷试验,重症肌无力,吡啶斯的明 - 2016-11-13
2009 肝脏生化试验的分析与监测共识意见(草案)
中华医学会第九次全国消化系统疾病学术会议 - 2009-12-04
药物临床试验登记与信息公示管理规范(试行)
根据《国家药监局关于实施<药品注册管理办法>有关事宜的公告(2020年第46号)》,为推进相关配套规范性文件、技术指导原则起草制定工作,在国家药品监督管理局的部署下,药审中心组
CDE - 临床试验 - 2020-12-07
药物临床试验富集策略与设计指导原则(试行)
为了促进临床试验各相关方正确地认识富集策略与设计的原理与方法,并指导其规范应用以达到提高临床试验效率的目的,药审中心组织制定了《药物临床试验富集策略与设计指导原则(试行)》(见附件)。根据《国家药监局
NMPA - 临床试验 - 2021-02-09
临床试验中缺失数据的预防与处理
缺失数据在临床试验中是非常常见且不可避免的。它一般是由于受试者在试验中失访、依从性差、不良事件、缺乏疗效等原因提前退出试验而造成,也可能是因为采集标本或测量中的问题,如疫苗临床试验中因采取的血液样本过少而未能检测到有效的抗体滴度值所造成的疗效指标缺失等缺失数据不仅会降低试验的把握度,而且会给试验结果的评价带来偏倚。因此,一方面,在数据统计分析时,采用适当的统计分析方法提高试验的检验效能,减小
药学学报 - 缺失,数据 - 2017-05-12
临床试验终点事件分类、定义采集与裁定
终点事件的分类 从预后角度分类,主要考核试验药物或治疗方法改善预后的疗效,一般都是与该疾病不良预后有关的事件。根据随访时间不同,可分为远期预后终点事件和近期预后终点事件。安全性终点是所有试验必须考核的。 最近,替代终点的使用问题在学术界引起热议。替代终点与临床效益有某种联系,但并不保证绝对相关。目前临床试验中,较多使用联合终点。使用联合终点的目的是能够更全面地考察试验对整个疾
中国医学科学院阜外心血管病医院 - 终点,试验 - 2013-08-01
AHJ:注册研究和临床试验研究对比应校正基础风险指数
美国学者Steinberg等选择25个国家的3 726例ST段抬高型急性心肌梗死患者进行注册研究,并收集了人口统计学、住院治疗方案、住院发生的临床事件资料。这些医院同时参加了用依诺肝素和溶栓再灌注治疗急性心肌梗死(ExTRACT-TIMI)的随机化临床试验。结果显示,注册研究组的患者基础风险更大,未校正的住院死亡率在注册研究组比临床试验组更高。在校正了基础风险指数后,两者的死亡率接近,且注册研究组
MedSci原创 - 2013-11-18
新药临床试验方案设计的研究
新 药临床试验是药品上市前最重要的研究环节之一。新药在上市之前,需要进行I-Ⅲ期的临床试验;上市后,需进行Ⅳ期临床试验,I-Ⅳ期的临床试验是对药物的 疗效、安全性及风险效益进行科学性、真实性及可靠性的临床疗效与安全性的评价研究。I-Ⅲ期的新药临床试验的数据,需提供给国家食品药品监督管理局 (SFDA)审查,以此作为重要的依据,来决定该药上市与否。全面的、结构清晰的临床研究方案,应该包括研
中国临床药理学杂志 - 临床试验,方案 - 2014-08-09
为您找到相关结果约500个