康复训练床注册审查指导原则
为进一步规范医疗器械的管理,国家药监局器审中心组织制修订了《康复训练床注册审查指导原则》,现予发布。
国家药品监督管理局医疗器械技术审评中心 - 康复训练床 - 2024-06-05
血管内回收装置注册审查指导原则
为进一步规范药物涂层球囊扩张导管等医疗器械的管理,国家药监局器审中心组织制修订了《血管内回收装置注册审查指导原则》,现予发布。
国家药品监督管理局 - 血管 - 2024-02-04
GSK新任CEO审查其研发计划
制药公司葛兰素史克(GlaxoSmithKline)表示,为提高效率,将暂停30个临床和临床前项目,以审查其研究和开发渠道。总部位于伦敦的葛兰素史克公司表示,它还将对其罕见疾病部门进行战略审查,并"正在考虑未来对这些资产的所有权"。
MedSci原创 - GSK,研发计划 - 2017-07-26
欧盟审查MSD的Keytruda / chemo组合
欧洲的监管机构已经开始对MSD的Keytruda/pemetrexed组合进行审查,以治疗转移性非小细胞肺癌(NSCLC)患者的一线治疗。
MedSci原创 - Keytruda,/,chemo组合 - 2018-04-24
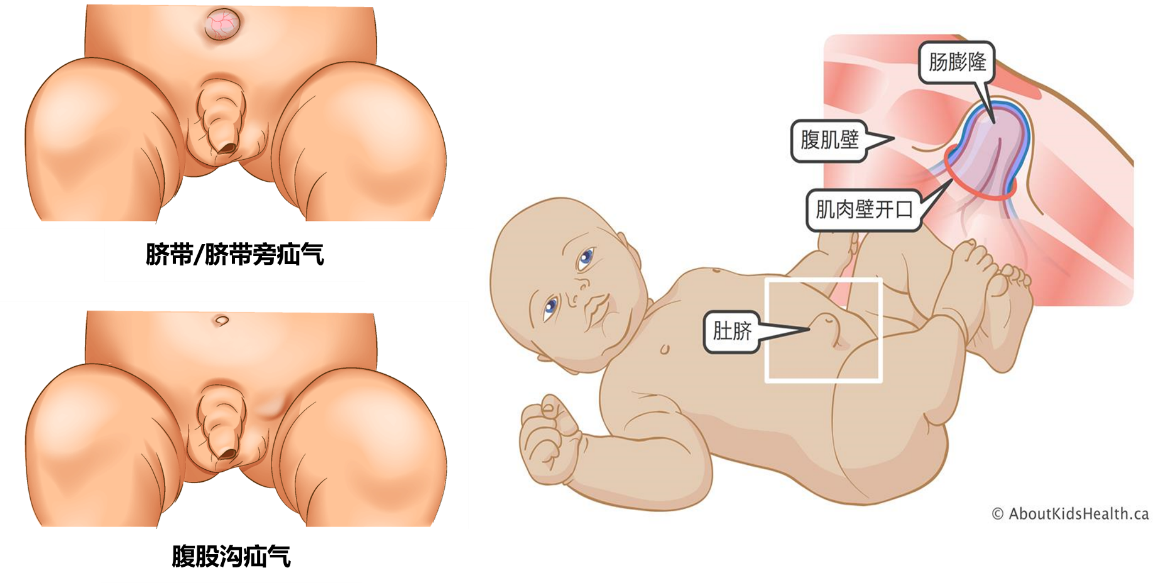
疝修补补片注册审查指导原则
为进一步规范药物涂层球囊扩张导管等医疗器械的管理,国家药监局器审中心组织制修订了《疝修补补片注册审查指导原则》,现予发布。
国家药品监督管理局 - 疝修补补片 - 2024-02-04
Shire的lanadelumab获欧盟快速审查
欧洲监管机构将对Shire的遗传性血管瘤药物lanadelumab进行加速评估。该公司正在开发lanadelumab用于预防12岁及以上病症的患者发生血管性水肿。HAE是一种罕见的遗传性疾病,会导致身体虚弱,疼痛甚至威胁生命的肿胀,全球患病率约为1/10,p000到1/50,000。Lanadelumab是一种研究性完全人源单克隆抗体,其特异性结合并抑制血浆激肽释放酶,因此可能提供新的治疗方法。该
MedSci原创 - lanadelumab,欧盟快速审查 - 2018-03-01
化学药品注册受理审查指南(试行)
根据《国家药监局关于实施<药品注册管理办法>有关事宜的公告》(2020年第46号),为推进相关配套规范性文件、技术指导原则起草制定工作,在国家药品监督管理局的部署下,药审中心组织制定了《化
CDE - 指导原则 - 2020-10-03
生物安全柜注册审查指导原则
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,根据《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号),国家药品监督管理局组织制定了生物安全柜注册审查指导原则等2项技术指
CDE - 生物安全柜 - 2022-01-24
为您找到相关结果约500个