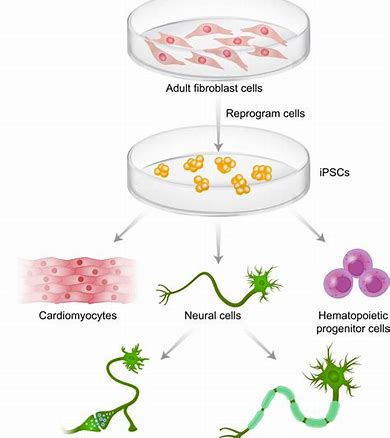
庆应义塾大学团队获得iPSCs心肌移植试验的批准
据《朝日新闻》报道,日本庆应义塾大学的研究人员已获得诱导多能干细胞(iPSCs)衍生的心肌细胞治疗扩张型心肌病的批准。
MedSci原创 - 庆应义塾大学,iPSCs,心肌移植 - 2020-02-08
EMA委员会支持批准赛诺菲的fexinidazole治疗昏睡病
赛诺菲近日宣布,欧洲药品管理局(EMA)的人用药品委员会建议批准使用fexinidazole治疗昏睡病。该公司指出,这种药物是第一种对口疮和昏睡病都有效的口服治疗药物。
MedSci原创 - fexinidazol,昏睡病,赛诺菲 - 2018-11-18
FDA批准Cosela(trilaciclib)用于减少化学疗法引起的骨髓抑制
Cosela(trilaciclib)可通过抑制细胞周期蛋白依赖性激酶4/6(CDK 4/6)来帮助保护骨髓细胞免受化学疗法的损害。
MedSci原创 - 骨髓抑制,化学疗法,Cosela(trilaciclib) - 2021-02-14
FDA 批准人工智能算法,准确检测常见骨折
近日,美国 FDA 宣布批准 Imagen 公司开发的软件 OsteoDetect 上市。OsteoDetect 是一款计算机辅助检测和诊断软件,使用人工智能算法来检测成人患者的桡骨远端骨折情况。
药明康德 - 人工智能 - 2018-05-28
FDA批准第三款新冠疫苗紧急使用授权
2月27日,美国食品和药物管理局(FDA)批准强生公司(Johnson&Johnson)生产的新冠疫苗可在美国紧急使用,适用于18岁及以上人群预防由新型冠状病毒感染引起的疾病(COVID-19)。
医谷网 - FDA,新冠疫苗,使用授权 - 2021-03-07
美或批准首个癌症基因疗法 有望治疗白血病
美国食品和药品监督管理局(FDA)的外部顾问日前对一种癌症基因疗法表示支持,即通过基因工程设计患者自身的免疫细胞来攻击和消灭癌症。
中国科学报 - 癌症,基因疗法,白血病 - 2017-07-17
批准线粒体疗法:美专家认为应始于男性胚胎
一种实验室辅助生殖技术能够让一些家庭避免患有某些遗传疾病的儿童降生,专家指出如果相关应用能够审慎地发展,可以考虑在美国推行这种疗法。这是美国国家科学院、工程院和医学院(NAS)专家组一份总结报告中公布的结论,该专家组对围绕这些争议性技术存在的伦理问题进行了评估,这种技术叫作线粒体DNA置换疗法。然而,更加具有争议的是,该专家组建议在辅助生殖过程中仅改变男性胚胎,以此限制未来后代可能存在的风险。(男
中国科学报 - 线粒体疗法,胚胎,生殖 - 2016-02-15
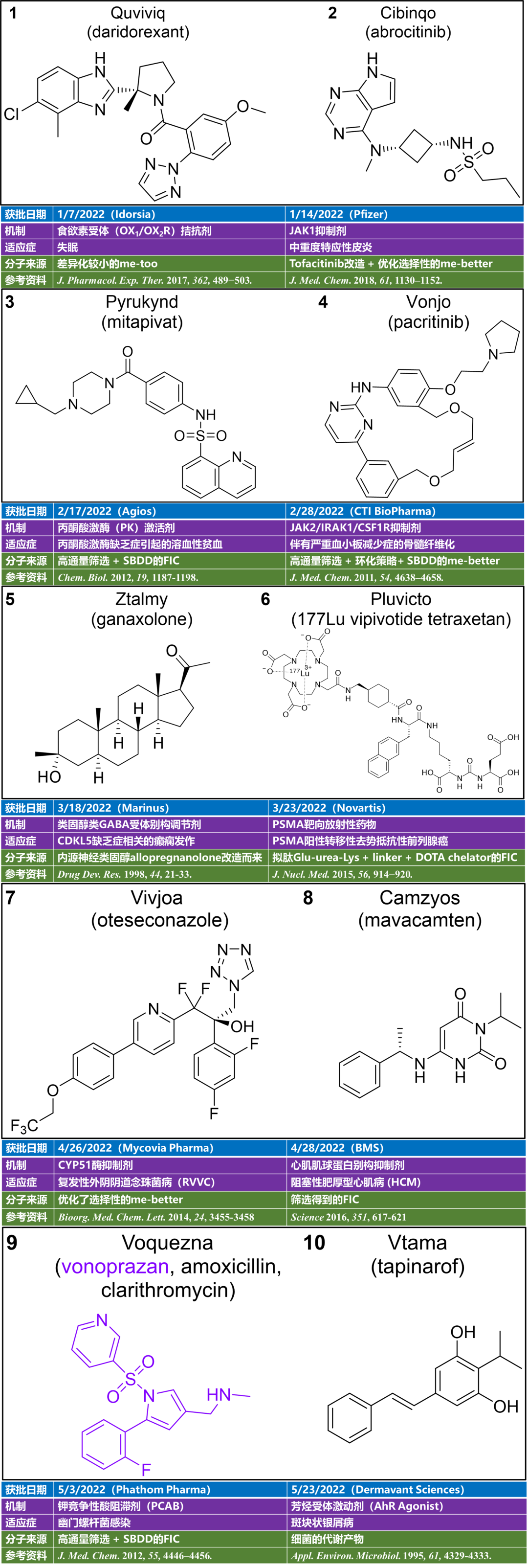
图表分析:话说2014年度FDA批准的那些药物
2014年,FDA药物评价和研究中心(CDER)审批通过了41个新药(Novel New Drugs),包括新药申报(NDAs)批准的新分子实体(NMEs)和生物制品申报(BLAs)批准的新生物药,数量是自2014年FDA批准的新药有几个特点:治疗罕见病的孤儿药的批准比往年都多;今年批准的一半以上药物为“优先审查”(Priority Review),比现有的药物有了改善;FD
创药网 - FDA,2014年度,药物 - 2015-03-31
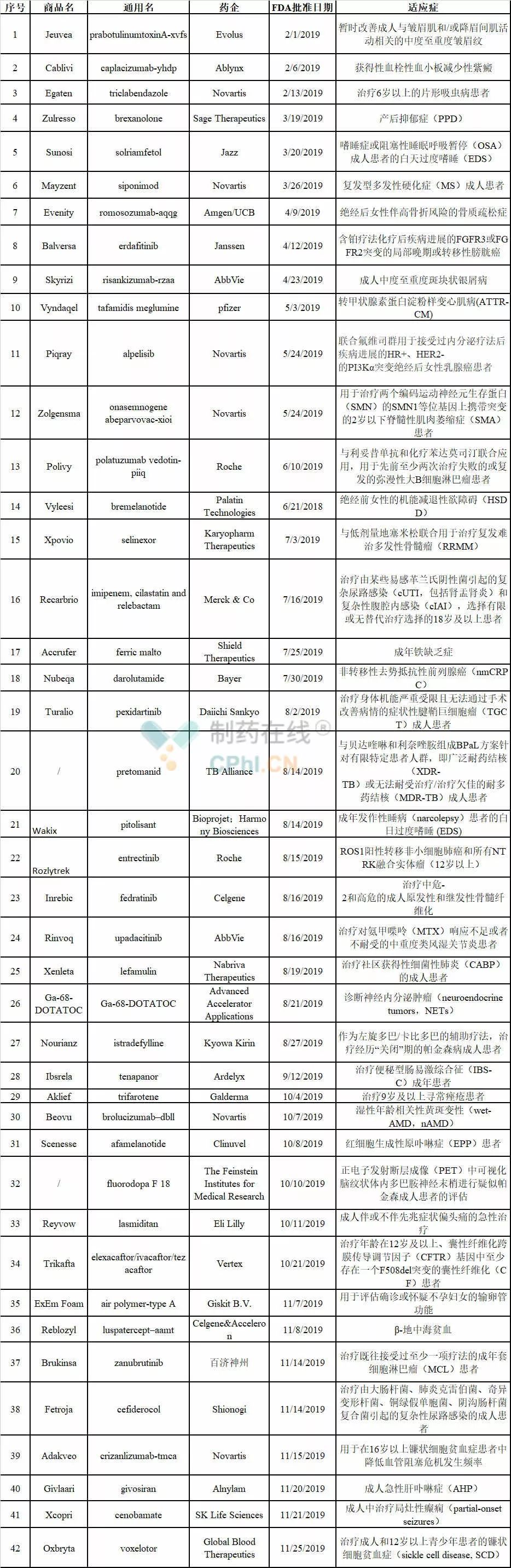
FDA 2019:批准45款新药,9款生物类似药
美国FDA的药物评估与研究中心(CDER)已经批准42款新药,9款生物类似药,3款在路上,而生物制品评估与研究中心(CBER)也批准了诺华公司的基因疗法Zolgensma和首款登革热疫苗。另外还有3款新药的PDUFA时间在12月,预计2019年将有45款新药获得FDA批准。相较于2017年和2018年,2019年会是FDA批准新药数量最低的一年,但质量不差,比如Skyrizi、Zolgensm
MedSci - FDA,新药 - 2019-12-24
百洋制药降糖新产品奈达获得FDA批准上市
近日,青岛百洋制药有限公司宣布,公司高端仿制药制剂技术取得重大突破,采用透泵控释技术的二甲双胍新药奈达®在美国获FDA审批上市,为2型糖尿病患者,尤其是肥胖和伴高胰岛素血症者带来福音。
医谷 - 百洋制药,糖尿病,二甲双胍新药 - 2019-02-26
Rozlytrek(entrectinib)治疗NTRK基因融合的实体瘤:已获欧盟批准
罗氏公司今日宣布,欧盟委员会有条件地批准了Rozlytrek(entrectinib),用于治疗12岁及以上患有NTRK基因融合的实体瘤患者。
MedSci原创 - 实体瘤,NTRK基因融合肿瘤,Rozlytrek(entrectinib) - 2020-08-03
FDA批准Carfilzomib用于治疗多发性骨髓瘤
Carfilzomib是一种静脉用药的第二代蛋白酶体抑制剂,美国食品与药品监督管理局(FDA)于7月20日宣布,批准将Carfilzomib用于治疗难治性多发性骨髓瘤患者。
EGMN - Carfilzomib,治疗,多发性骨髓瘤,FDA - 2012-07-27
FDA考虑批准“三人试管婴儿”临床试验
美国医药卫生管理当局正在考虑是否应该给一项饱受争议的辅助生育技术(assisted-reproduction technique)——线粒体置换技术(mitochondrial replacement)临床试验开绿灯,该技术能够避免携带有遗传病致病基因的女性将疾病遗传给下一代。批评者们认为,该技术也存在安全和伦理道德方面的风险。就在几天前(10月22日),美国食品与药品监督管理局(FDA)在美国马
MedSci原创 - 临床试验,FDA,试管婴儿 - 2013-11-05
失而复得,罗氏白血病药物Gazyvaro重获NICE批准
英国国家健康与临床卓越研究所 (NICE)近日撤回了对罗氏白血病药物Gazyvaro的限制,目前Gazyvaro仍处于英格兰和威尔士的NHS批准过程中,尽管如此,这对于罗氏而言无疑是一个好消息。
生物谷 - 白血病,药物 - 2014-12-04
为您找到相关结果约500个