医疗器械临床试验审批项目立卷审查要求
国家药品监督管理局组织对现行的《医疗器械临床试验审批项目立卷审查要求》文件进行了全面修订。
国家药品监督管理局官网 - 临床试验,医疗器械 - 2023-06-22
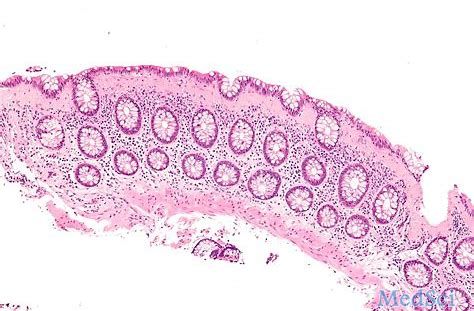
BT-11治疗溃疡性结肠炎的全球II期临床试验已正式开始
Landos是一家专注于自身免疫性疾病治疗药物发现和开发的临床阶段生物制药公司,近日宣布第一名患者已经正式入组BT-11治疗溃疡性结肠炎的全球II期临床试验,以评估BT-11在轻度和中度患者中的安全性和有效性
MedSci原创 - 溃疡性结肠炎,BT-11,钙卫蛋白 - 2019-08-21
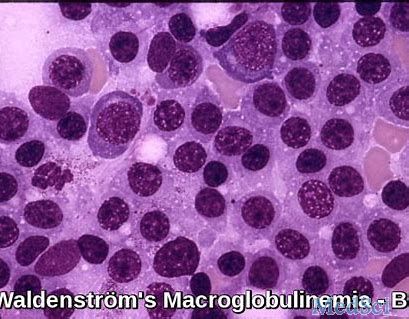
Mabruxixafor联合伊布替尼治疗华氏巨球蛋白血症:已开始Ib期临床试验
X4 Pharmaceuticals是一家临床阶段的生物制药公司,致力于开发治疗罕见疾病的新型疗法,近日宣布,已启动mavorixafor(X4P-001)联合伊布替尼(Imbruvica)治疗华氏巨球蛋白血症(WM)的Ib期临床试验。
MedSci原创 - 华氏巨球蛋白血症,伊布替尼,Mabruxixafor - 2019-12-31
欧盟加速临床试验数据公开进程 AllTrials助力
在 12 月 20 日达成的临时协议下,欧盟的研究人员将不得不公开临床试验的结果。欧盟 28 个成员国的代表与欧盟议会达成协议,这是其更广泛改革的决定性一步,将会简化和加速整个欧盟的临床试验程序。让公众更容易地获取临床试验结果的倡导是一个值得称赞的谈判结果,研究人员认为这是可以推广至全球的一个范例。20 日的协议是“一个非常重要的谈判阶段所取得的神奇结果”,英国 AllTrials 活动
生物360 - 临床试验,欧盟,公开,AllTrials - 2013-12-25
北大肿瘤医院临床试验再添新病房
北京大学肿瘤医院I期临床试验病区新病房5日下午正式启用。目前,I期临床病区有专职医生6人,研究护士团队18人,专职实验室分析人员4人。全体医护人员均接受过相关培训。这也是全国仅有的设立专职医护团队的临床试验中心。“如果没有临床研究,就没有规范治疗;如果没有临床研究,就没有医学进步。”北京大学肿瘤医院副院长沈琳说,一种新药的上市,除了在实验室里孕育外,还需要进行动物试验和临床试验。其中,临床试验特别
北京晚报 - 北大肿瘤,临床试验,新病房 - 2019-11-06
药物临床试验的一般考虑指导原则
药物临床试验的一般考虑指导原则一、概述药物临床试验的一般考虑指导原则(以下称指导原则),是目前国家食品药品监督管理总局关于研究药物在进行临床试验时的一般考虑。制定本指导原则的目的是为申请人和研究者制定药物整体研发策略及单个临床试验提供技术指导,同时也为药品技术评价提供参考。另外,已上市药品增加新适应症等进行临床试验时,可参照本指导原则。二、临床试验
CFDA - 临床试验,指导原则 - 2018-01-10
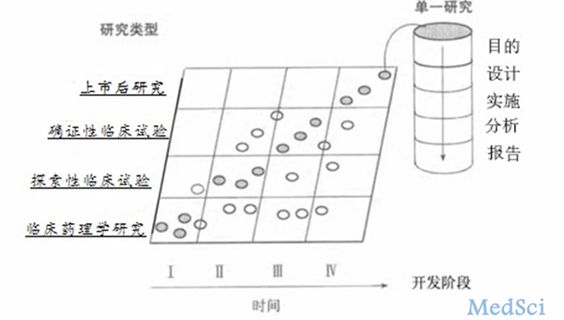
中国1类新药分布及临床试验概况分析
我国有近6700余个药物品种处于临床研究阶段,临床研究数目多、临床研究药物品种多。临床数目多,则是临床研究情况的表现,即药品临床;药物品种多,则是药物研发情况的表现,即临床药品。临床试验直观反映了药品的有效性及安全性,又侧面折射出药物研发的状态与进展。下面本文将对我国药品临床与临床药品(1类新药)做逐一分析:1、我国临床试验(CTR)情况研究-药品临床2013年9月6日,我国国家食品药品监督管理总
药渡 - 1类新药,临床研究 - 2018-11-01
芬氟拉明治疗Lennox-Gastaut综合征的III期临床试验取得积极结果
一家开发罕见疾病疗法的全球制药公司Zogenix今日报告了其研究性药物FINTEPLA®(ZX008,芬氟拉明口服液)的全球III期临床试验的最新结果,结果表明,FINTEPLA治疗Lennox-Gastaut
MedSci原创 - Lennox-Gastaut综合征,芬氟拉明,癫痫 - 2020-02-07
新药临床试验设计中的基础问题解读
1新药临床试验管理规范1.1受试者权益安全性保障(即伦理性) 1.临床试验必须获得国家药品监督管理局的批准 2.为确保受试者的权益,并为之提供公众保证。必须经伦理委员会批准 3.中国GCP规定参加临床试验的研究单位必须是国家药品临床研究基地 4.中国GCP规定,负责临床试验的研究者(investigator)必须具备的条件
MedSci原创 - 新药,临床试验,设计 - 2012-12-25
新药临床试验中遇到的100个问题(上)
在新药研发和临床试验过程中我们会遇到这样或者那样的问题,本文总结了100个我们在新药临床试验中经常遇到的问题,仅供大家参考! 1、什么是 GCP?GCP(Good Clinical Practice)中文译为“药品临床试验管理规范”,它是一种对涉及人类受试者的临床试验的设计、实施、记录及报告的国际性道德和科学质量标准。无论是由药厂发起或是由合同研究组织实施的临床试验,都应遵从此标准
佰荣泰华 - 临床试验,新药 - 2017-04-25
适应性临床试验设计相关问题的探讨
众所周知,新药的研发是一个充满变数且不断做出复杂决断的过程,这就要求试验设计应该具备可变动性,以便于在试验过程中对其进行调整。
MedSci原创 - 适应性设计,临床试验 - 2013-05-30
药物临床试验适应性设计指导原则(试行)
为规范和统一国内对适应性设计的认识,促进适应性设计的应用和理解以提高研发效率,药审中心组织制定了《药物临床试验适应性设计指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术
NMPA - 临床试验 - 2021-02-09
遗传学分析引发癌症治疗临床试验变革
布鲁塞尔——随着癌症相关遗传标志物的队伍迅速壮大,肿瘤治疗临床试验的设计正在发生根本性的转变。如今的趋势是将详细的遗传学分析纳入到临床试验中,这样一旦有了结果,研究者就可以尝试将治疗应答或失败与肿瘤遗传特性的变化联系起来。在由美国临床肿瘤学会(ASCO)、欧洲癌症研究与治疗组织(EORTC)和美国国立癌症研究所(NCI)联合举办的会议上,这一领域的权威专家指出,
爱思唯尔 - 遗传学分析,肿瘤治疗临床试验 - 2013-11-27
AllTrials组织声明:所有临床试验数据皆要公开
It’s time all clinical trial results are reported. Patients, researchers, pharmacists, doctors and regulators everywhere will benefit from publication of clinical trial results. Wherever you are in th
MedSci原创 - AllTrials,临床试验 - 2013-03-22
为您找到相关结果约500个