JAMA Surg:术后抗菌药物治疗时间与不良预后
研究认为,延长术后抗菌药物预防治疗时间与更高的AKI和艰难梭菌感染风险有关,且持续时间延长不会导致额外的SSI降低
MedSci原创 - 抗菌药物,外科,感染 - 2019-04-28
阿达格拉西布治疗携带KRASG12C突变的晚期实体瘤:疗效显著可耐受
该研究旨在评估阿达格拉西布在具有KRASG12C突变的实体瘤患者中的疗效和安全性。
MedSci原创 - 实体瘤,KRASG12C,阿达格拉西布 - 2023-06-29
BMJ:抗PD-L1药物免疫相关的不良事件!
由此可见,器官特异性免疫相关的不良事件在接受抗PD-1药物治疗较为罕见,但风险与对照治疗相比有所增加。与免疫激活有关的一般不良事件在很大程度上相似。不良事件与肌肉骨骼问题的报道不一致,可能是常见的不良事件。
MedSci原创 - 抗PD-L1药物,免疫,不良事件 - 2018-03-15
Clinical Nutrition: 胃切除术后早期口服肠内营养的耐受性及预测肠衰竭的危险因素
但是,很少研究早期口服肠内营养的耐受性。 这项研究旨在调查早期口服营养的耐受性以及影响胃切除术后肠衰竭的因素。
MedSci原创 - 肠内营养,肠衰竭 - 2020-11-15
警惕:双黄连注射剂的严重不良反应
2001年11月,国家药品不良反应监测中心(以下简称国家中心)首次通报了双黄连注射剂引起的过敏反应。通报发布后,国家中心仍陆续收到有关双黄连注射剂的严重不良
国家药品不良反应监测中心 - 双黄连,药品不良反应 - 2016-08-04
JGH Open:门失弛缓患者营养不良的影响因素
门失弛症患者营养不良的概率不高,研究也相对较少。因此,本项研究旨在探究:(i)贲门失弛缓患者中的营养不良发生率,以及(ii)气胀(PD)对营养不良的影响。
MedSci原创 - 贲门失弛缓症,营养不良 - 2020-03-15
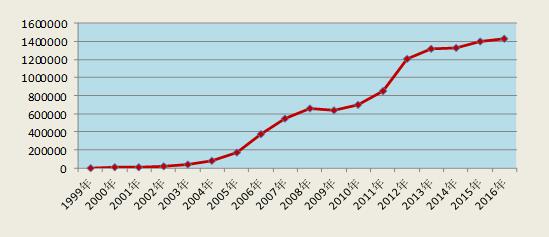
国家药品不良反应监测年度报告(2016年)
为全面反映2016年我国药品不良反应监测情况,加强药品监管,落实企业主体责任,促进临床合理用药,保障公众用药安全,依据《药品不良反应报告和监测管理办法》,国家食品药品监督管理总局(以下简称总局)组织国家药品不良反应监测中心编撰《国家药品不良反应监测年度报告(2016年)》。一、药品不良反应监测工作进展 网络建设继续深入,监测能力进一步提升。2016年,国家药品不良反应监测网络建设
MedSci原创 - 药品,不良反应 - 2017-04-28
头孢唑林注射剂的严重不良反应
2013年,国家药品不良反应病例报告数据库共收到头孢唑林注射剂严重病例报告349例。严重不良反应/事件累及系统排名前三位的依次为全身性损害、呼吸系统损害、皮肤及附件损害。一、严重病例的临床表现头孢唑
国家药品不良反应监测中心 - 头孢唑林注射剂,不良反应 - 2016-12-31
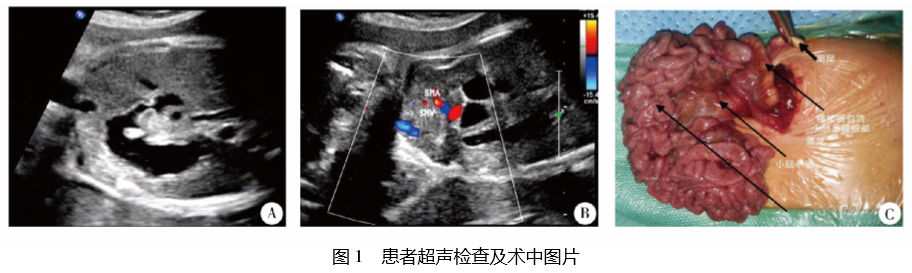
产前超声诊断肠旋转不良伴中肠扭转 1 例
孕妇, 29 岁, G1P0,孕 34 周于外院行超声检查提示:胎儿 上腹部脊柱前方偏右侧见“C 字型”肠管扩张,范围约3.6cm× 1.2cm,其背侧可见血管回声,有旋转感。孕妇唐筛未见异 常,未行无创及羊水穿刺检查,无家族病史。2018 年 7 月 31 日患者孕 37 周时于我院行产科超声检查,超声示: 单活胎, 胎儿测值符合孕周,羊水指数 15.1cm; 胎儿部分肠管迂曲扩 张,较宽处内径
现代妇产科进展 - 产前超声,肠旋转不良,中肠扭转 - 2019-11-19
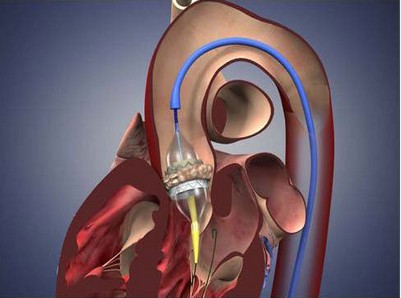
JACC:TAVR预后不良风险模型,到底有没有应用价值?
来自美国的研究人员开展了一项研究,这项研究审查了以前开发的TAVR预后不良风险模型在外部数据集的性能,并探讨了老年领域对模型性能的增量贡献。TAVR后的不良结果被定义为死亡,生活质量(QOL)较差,或QOL下降,研究人员使用堪萨斯城心肌病问卷进行调查
MedSci原创 - TAVR - 2016-10-19
胚胎发育不良性神经上皮肿瘤1例报道
胚胎发育不良性神经上皮肿瘤(DNT或DNET)是一种属于少见的神经元和神经胶质混合性肿瘤,1993年被WHO收人神经系统肿瘤新分类(WHOI级)。
中国实验诊断学 - 胚胎,发育,不良,神经上皮,肿瘤 - 2018-05-17
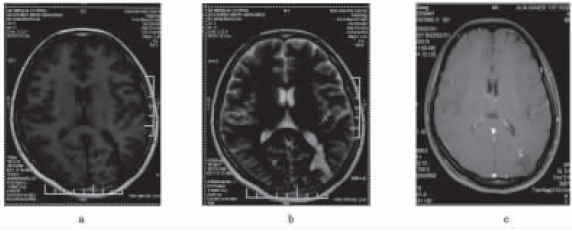
Diabetes Care:糖尿病与不良脑容积变化相关
美国学者的一项研究表明,糖尿病与脑灰质容积较小和全脑缺血性病变容积增大具有相关性。论文于2012年8月29日在线发表于《糖尿病护理》(Diabetes Care)杂志。 此项研究共纳入1366例女性受试者,并利用结构性脑磁共振成像(MRI)测定局部脑容积和缺血性病变容积。平均4.7年后对698例女性进行重复测定。对比伴和未伴糖尿病女性的横断面差异和纵向变化。 结果显示,首
医学论坛网 - 糖尿病,脑容积,缺血性病变 - 2012-09-05
CFDA:关注氟喹诺酮类药品的严重不良反应
药品不良反应信息通报制度是我国药品监督管理部门为保障公众用药安全而建立的一项制度。《药品不良反应信息通报》(以下简称《通报》)公开发布以来,对推动我国药品不良反应监测工作,保障广大人民群众用药安全起到了积极作用。本期通报品种为氟喹诺酮类药品。
DXY - 氟喹诺酮类药品 - 2013-11-22
为您找到相关结果约500个