阿达木单抗注射液生物类似药临床试验指导原则
本文为国家药品监督管理局药品审评中心发布的《阿达木单抗注射液生物类似药临床试验指导原则》。
国家药品监督管理局药品审评中心 - 临床试验 - 2024-02-12
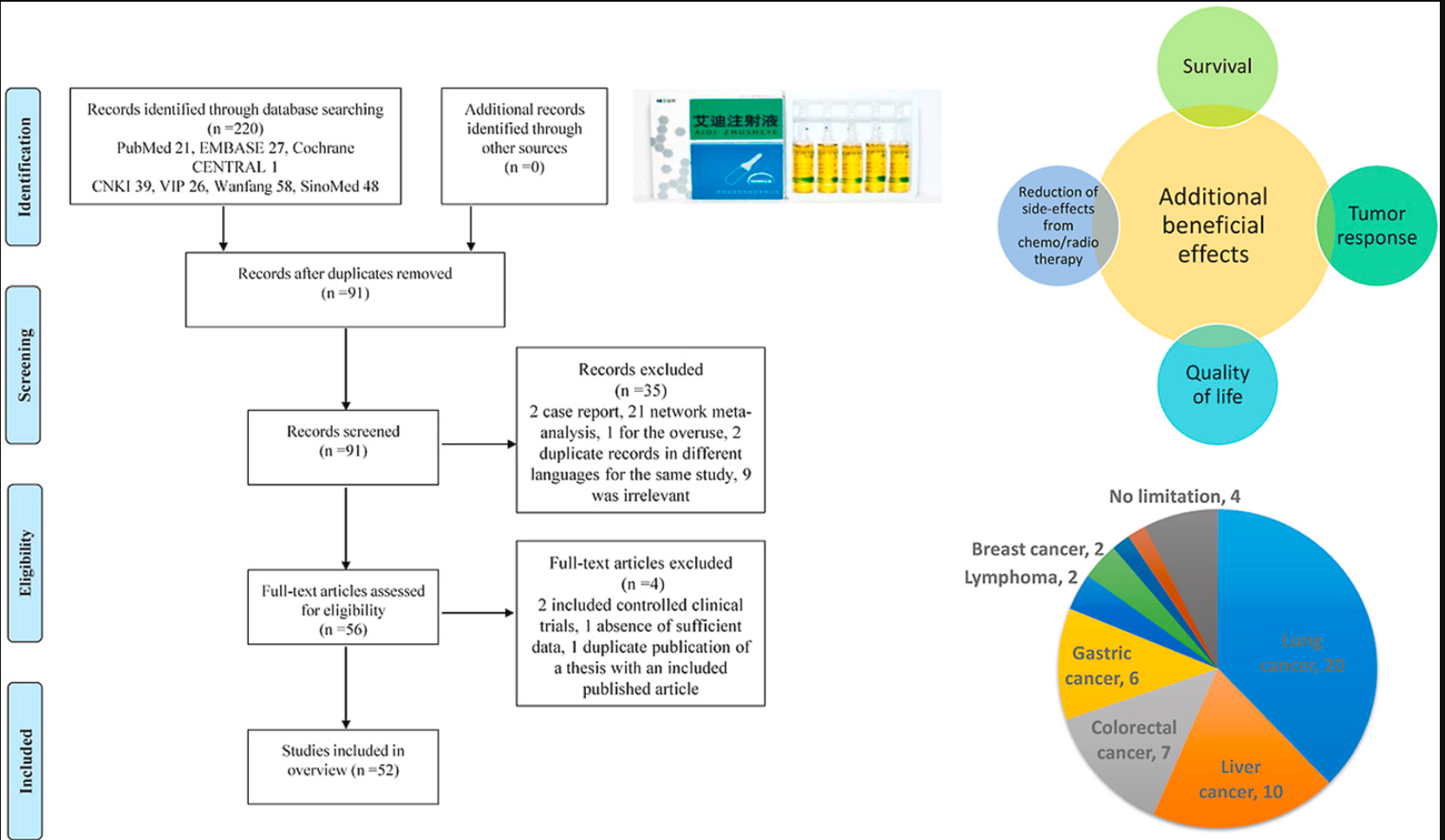
J Ethnopharmacol:中成药艾迪注射液治疗癌症的系统评价和荟萃分析
艾迪注射液是国家食品药品监督管理局批准的中草药注射剂之一,也是中国癌症治疗领域最具竞争力的产品。它由斑蝥、黄芪、人参和刺五加的提取物组成。
MedSci原创 - 中成药,系统评价,癌症护理,艾迪注射液,AMSTAR2 - 2022-03-17
苑东生物「格隆溴铵注射液」即将第2家获批
10月14日,苑东生物3类仿制药格隆溴铵注射液上市申请进入「在审批」阶段,有望于近期正式获批,成为国内继恒瑞医药之后第2家该药品获批厂家。
医药魔方 - 格隆溴铵,苑东生物 - 2020-10-15
欧盟决定保留羟乙基淀粉注射液上市许可并给出了这些建议
欧洲药品管理局(EMA)发布信息,经欧盟成员国协商采取新的措施以有效减少羟乙基淀粉(HES)注射液风险的可行性后,人用药品相互认可和分散评审程序协调组(CMDh)决定保留羟乙基淀粉(HES)注射液的上市许可
EMA网站 - 羟乙基淀粉注射液,脓毒血症 - 2018-10-17
FDA将优先授予缓控释丁丙诺啡注射液审核资格
美国食品药品监督管理局(FDA)确定了新药的《处方药使用者费用法》目标日期,即2018年1月19日。
美通社 - 丁丙诺啡注射液,FDA,审核 - 2017-09-20
用于治疗乳腺癌的帕妥珠单抗注射液获批上市
近日,国家药品监督管理局批准帕妥珠单抗注射液(英文名:Pertuzumab Injection)进口注册申请,联合曲妥珠单抗和化疗用于具有高复发风险的人表皮生长因子受体2(HER2)阳性早期乳腺癌患者的辅助治疗
国家药监局网站 - 乳腺癌,帕妥珠单抗注射液,上市 - 2018-12-17
PRS:丹参注射液可以促进人脂肪干细胞的成脂分化吗?
该研究结果表明丹参注射液对脂肪干细胞体外成脂有积极作用,但4种亲水性成分对脂肪干细胞成脂和细胞活力的影响尚不明确。
MedSci原创 - 脂肪干细胞,自体脂肪移植,自体脂肪移植隆乳,注射整容 - 2021-03-12
喜炎平注射液被叫停,国家食药总局还能做些什么?
2017年9月23日国家食品药品监督管理总局网站发文,叫停青峰药业生产的喜炎平注射液、山西振东安特生产的红花注射液。消息一出,迅速成为行业热点事件。这事儿怎么看?
医学界智库 - 喜炎平,食品药品安全 - 2017-09-26
FDA批准Gadavist注射液作为心脏磁共振(MR)成像的造影剂
拜耳公司近日宣布,美国FDA了批准Gadavist®(钆布醇)注射液用于心脏磁共振(MR)成像,以评估已知或疑似具有心肌灌注和冠状动脉疾病(CAD)的成人患者。
MedSci原创 - 心脏磁共振,Gadavist,造影剂 - 2019-07-16
国家药监局修订药品说明书:肿节风注射液禁止静脉给药!
关于修订肿节风注射液和小金制剂说明书的公告(2018年第100号)根据药品不良反应评估结果,为进一步保障公众用药安全,国家药品监督管理局决定对肿节风注射液增加警示语,对其和小金制剂(丸剂、胶囊剂、片剂)现将有关事项公告如下:一、所有肿节风注射液和小金制剂生产企业均应依据《药品注册管理办法》等有关规定,按照相应说明书修订要求(见附件1—3),
国家药监局微信公众号 - 药品,说明书,国家药监局 - 2019-01-05
68Ga-PSMA-11注射液的制备和质量控制回顾及建议
本研究有望指导核医学从业人员规范进行68Ga-PSMA-11注射液的制备和质量控制,从而提升该药物的质量与安全,并为其相关行业标准的制定提供参考。
同位素 - 68Ga-PSMA-11 - 2023-07-30
奥木替韦单抗注射液抗狂犬病临床应用专家共识
该共识规范了奥木替韦单抗的临床使用,提高了我国狂犬病暴露后预防水平,降低了感染率。
EXPERT OPINION ON DRUG SAFETY - 狂犬病,奥木替韦单抗 - 2023-07-13
盐酸多柔比星脂质体注射液仿制药研究技术指导原则
本文为国家药品监督管理局药品审评中心发布的《盐酸多柔比星脂质体注射液仿制药研究技术指导原则》。
国家药品监督管理局药品审评中心 - 多柔比星 - 2024-02-15
帕妥珠单抗注射液生物类似药临床试验指导原则
为鼓励生物类似药研发,进一步规范和指导帕妥珠单抗生物类似药的临床试验设计和终点选择,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《帕妥珠单抗注射液生物类似药临床试验指导原则》
国家药品监督管理局药品审评中心 - 帕妥珠单抗 - 2021-05-13
为您找到相关结果约500个