优先审评审批助力丙肝新药加快上市
随着我国药品审评审批制度改革的持续推进,广大丙肝患者的热切期盼成为现实——9月21日,国家食品药品监督管理总局同时批准吉利德公司(Gilead)的口服丙肝新药索磷布韦片,艾伯维公司(AbbVie)的奥比帕利片
中国医药报 - 优先评审,丙肝新药,上市 - 2017-09-25
众议院通过“21世纪治愈法案”,FDA新药评审或将进一步改革
“21世纪治愈法案”是新药开发立法的又一个里程碑,不仅进一步推动FDA对新药评审的改革,也赋予国立卫生研究院(NIH)更多的研究资源,促进基础医疗研究的发展。
美中药源 - FDA新药评审,改革 - 2015-07-13
加快境外上市新药审评审批获积极进展
党中央、国务院高度重视药品医疗器械审评审批制度改革工作,加快境外上市新药的审评审批是其中重要一环。今年4月、6月,李克强总理先后主持召开国务院常务会议,就加快进口新药上市作出系列重要部署。6月22日,在国务院新闻办召开的国务院政策例行吹风会上(以下简称吹风会),国家药品监督管理局局长焦红介绍,加快境外上市新药审评审批工作取得积极进展,简化境外上市新药审批政策效果初步显现。
中国医药报 - 境外上市新药,审评审批 - 2018-06-25
中国药品审评审批用时进一步压缩,创新药物审评审批再提速
记者6日从全国药品监管工作座谈会上获悉,我国药品审评审批用时进一步压缩,待审评的药品注册申请已由2015年高峰时的2.2万件降至3200件以内。创新药物和医疗器械审评审批进一步加快,截至今年6月底,共对29批597件药品注册申请进行优先审评审批,审核批准了39个创新医疗器械和4个优先审批医疗器械产品。国家药品监督管理局局长焦红介绍,今年以来,通过持续深化药品医疗器械审评审批制度改革,境外新药上市明
新华社 - 药品,审批,创新 - 2018-07-06
FDA优先评审再生元和赛诺菲特应性皮炎药物dupilumab
再生元($REGN)和赛诺菲($SNY)对他们治疗特应性皮炎的潜在重磅药物dupilumab使用了优先评审券。自从再生元和赛诺菲发布令人印象深刻的III期临床数据,并获得突破疗法认定之后,IL-4和IL-13抗体抑制剂的优先评审资格证实了之前的怀疑。
新浪医药新闻 - 特应性皮炎 - 2016-09-28
美国FDA批准首个干眼症新药
Shire公司宣布美国FDA已经批准其新药Xiidra滴眼剂溶液(5%浓度的lifitegrast眼用溶液)上市,每日使用两次,治疗成人干眼症患者。
生物谷 - FDA,干眼症,新药 - 2016-07-13
药品评审中心(CDE)已受理Pamiparib治疗卵巢癌的新药申请
生物技术公司百济神州今日宣布,中国药品监督管理局(NMPA)的药品评审中心(CDE)已接受百济神州PARP1和PARP2研究性抑制剂Pamiparib的新药申请(NDA)。
MedSci原创 - 卵巢癌,PARP1,Pamiparib - 2020-07-18
FDA接受阿斯利康naloxegol新药申请
阿斯利康(AstraZeneca)11月19日宣布,FDA已接受naloxegol新药申请(NDA),该药是一种实验性外周作用(peripherally-acting)μ-阿片受体拮抗剂,专门开发用于治疗阿片类药物引发的便秘
生物谷 - 新药,FDA - 2013-11-20
FDA:葛兰素史克HIV新药Tivicay获FDA批准
葛兰素史克(GSK)8月12日宣布,FDA已批准Tivicay(dolutegravir)50mg片剂。Tivicay新药申请(NDA)的提交,包括4个关键性III期临床试验(SPRING-2、SINGLE、SAILIN
生物谷 - 新药,FDA - 2013-08-15
葛均波:建议加快创新药械审评审批 | 两会谈医学创新
“在关注医学创新的过程中,我曾被两位科学家的遭遇深深触动,一是浙江大学原副校长褚健,一是清华大学教授付林。”3月6日,全国政协委员、中国科学院院士、中国医学创新联盟CMIA总发起人、博鳌医学创新研究院院长、复旦大学附属中山医院心内科主任葛均波在接受媒体采访时说,“没有法律法规做保障,创新是搞不起来的。”葛均波一直以来都是国内医学创新的推动者和践行者。作为全国政协委员,今年两会期间,葛均波多次从不同
健康界 - 药械审评 - 2018-03-07
FDA批准首个狼疮肾炎口服新药
1月22日,Aurinia制药公司宣布FDA批准Lupkynis(voclosporin,伏环孢素)上市,联合免疫抑制疗法治疗成人活动性狼疮肾炎(LN)。Lupkynis是FDA批准的首个狼疮肾炎口服
医药魔方 - 狼疮肾炎 - 2021-01-25
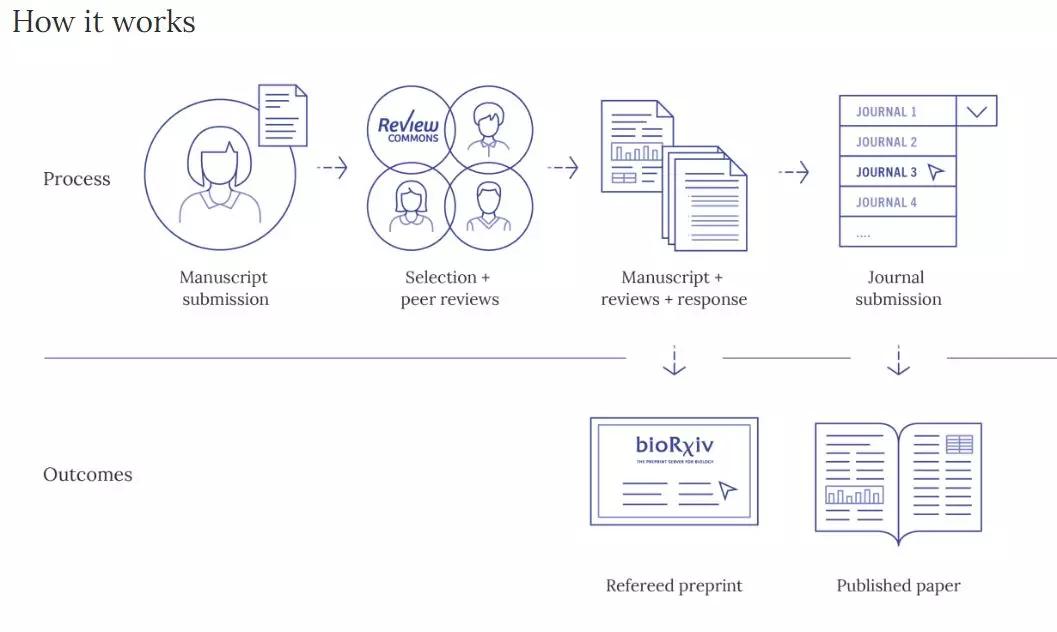
Review Commons:先于期刊同行评审之前的评审
ASAPbio和 EMBO Press于2019年12月9日推出了 Review Commons,这是一个高质量,独立于期刊的,用于对生命科学领域稿件进行同行评审,然后再提交给期刊同行评审平台。作者可以将预印本或未出版的手稿提交给Review Commons进行专家级同行评审。最终的 “ Refered Preprint”(包含稿件,审稿人报告以及作者回复审稿人意见)
网络 - 同行评审,评审 - 2020-02-13
FDA:安斯泰来新药获美国FDA批准
这款名为他克莫司的处方新药需要配合其他药物一起服用,适合于肾移植患者。公司首席科学官西夫·克斯坦恩表示说,每个患者使用的药剂都是不同,需要区别对待。
大智慧 - FDA,新药 - 2013-07-23
FDA批准治疗热带疾病新药
FDA日前批准Impavido(米替福斯)治疗热带病利什曼病(leishmaniasis),该病是苍蝇叮咬引起,由寄生虫传染给人类。Impavido获得FDA快速审批,优先审查和罕用药资格认定。
医药经济报 - 新药,FDA - 2014-04-04
为您找到相关结果约500个