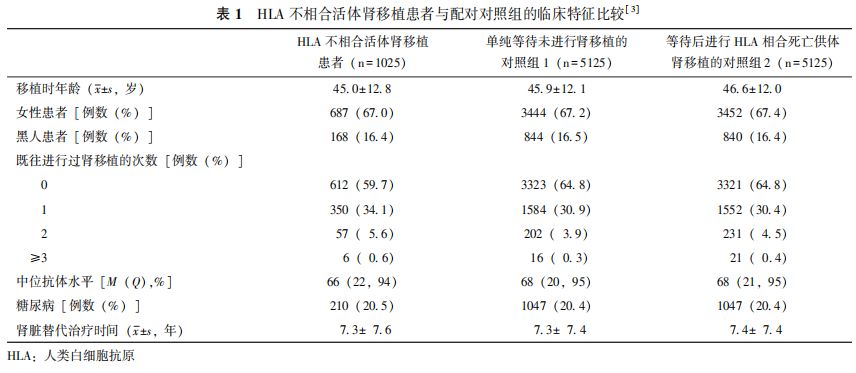
早产儿代谢性骨病的临床资料分析
在避免早产的同时,应提高对本病的综合管理,特别是注意早期监测25-羟维生素D水平,合理补充维生素D,减少远期的不良影响。
云南医药 - 早产儿,代谢性骨病 - 2022-11-29
总局明确豁免临床试验IVD试剂临床评价资料要求
继10月30日,国家食品药品监管总局发布第三批免于进行临床试验的医疗器械目录(以下简称“目录”),对37种第二类医疗器械、11种第三类医疗器械和116种体外诊断(IVD)试剂豁免进行临床试验后,日前,总局又发布《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》(以下简称《基本要求》),并于发布之日起施行。《基本要求》配合目录使用,用于指导注册申请人进行体外诊断试剂临床评价工作。这是总局
中国医药报 - 临床试验,IVD试剂 - 2017-11-10
资料整理用Excel
单位里的各类文件资料堆积如山,继续存在电脑里,随时都可能遭受病毒侵害和系统崩溃的灭顶之灾。资料的保管最理想最安全的办法是刻录到光盘里。刻录之前,我们必须对杂乱的文档进行整理。
生物谷 - 资料,料整,整理,理用,用E,Ex,xc,ce - 2012-04-16
免于进行临床试验的体外诊断试剂临床评价资料基本要求发布
为进一步做好体外诊断试剂注册管理,规范免于进行临床试验的体外诊断试剂临床评价工作,根据《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号),8日国家食品药品监督管理总局发布了《免于进行临床试验的体外诊断试剂临床评价资料基本要求
新浪医药新闻 - 体外诊断试剂,免于进行临床试验 - 2017-11-09
牙膏备案资料管理规定
为贯彻落实《牙膏监督管理办法》,规范牙膏备案工作,国家药监局制定了《牙膏备案资料管理规定》,现予发布,自2023年12月1日起施行。
国家药品监督管理局官网 - 牙膏 - 2023-11-23
临床急需境外新药标准复核检验用资料及样品有哪些要求?
6月25日,国家药品监督管理局发布《关于发布临床急需境外新药标准复核检验用资料及样品要求的通告(2019年第35号)》(以下简称通知)。
国家药品监督管理局 - 临床急需,境外新药 - 2019-06-27
《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》解读
国家食品药品监督管理总局组织制定并于2017年11月3日发布了《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》,自发布之日起施行。
CFDA - CFDA,体外诊断试剂,临床试验 - 2017-11-09
临床研究监查:原始资料从“核查”到“审核”
原始资料核查(SDV)一直都是保证临床研究质量的重要手段,也是监查员在临床研究监查过程中花费时间和精力最多的地方。但是,随着申办方和研究者临床研究经验的不断积累、各种临床研究新工具的不断出现,百分之百的原始资料核查已经不能满足临床研究监查工作高质量与高效率并举的要求。 随着美国FDA基于风险的临床研究监查指导原则的推出,原始资料审核(SDF,Source document Revi
网络 - 研究监查 - 2019-12-26
历史资料
1)学术会议 年 份 国家和地区数 国外参会人数 国内参会人数 发表论文数 1985 15 180 460 633 1987 25 126 508 695 1989 20 82 345 447 1991 25 102 308 531 1993 25 134 308 544 1995 23 142 244 472 1997 21 174 279 552 1999 23
会议 - 2008-06-26
抗肿瘤新药首次人体临床试验申请临床相关资料准备建议
优化临床试验审评审批制度是当前改革重点之一,临床试验方案将成为临床审评重点,内容结构完整的、高质量、可评价的临床试验方案是高效完成审评的保障。抗肿瘤新药是全球创新药研发热点,在当前创新药临床试验申请中大约占40%。然而,现阶段抗肿瘤药物首次
NMPA - 抗肿瘤,新药 - 2018-12-12
为您找到相关结果约500个