Alkermes开始验证ALKS 4230治疗晚期实体瘤的有效性
Alkermes公司近日宣布启动ARTISTRY-2试验,这是一项新的针对候选药物ALKS 4230的临床研究。
网络 - ALKS,4230,晚期实体瘤,融合蛋白 - 2019-02-28
FDA接受Alkermes重新提交ALKS 3831治疗精神分裂症的新药申请
精神分裂症是一种精神病,一种以思维、观点、情绪、语言、自我意识和行为出现扭曲为特征的精神疾患。
MedSci原创 - 精神分裂症,双相情感障碍,Alkermes,ALKS 3831 - 2020-12-30
FDA向Alkermes的实验性抗抑郁药ALKS 5461发出拒绝提交函
近日,Alkermes表示,FDA对其实验性药物ALKS 5461持否定态度,该药是一种每日给药一次治疗重度抑郁症以及对标准抗抑郁药反应不足的患者的口服疗法。根据Alkermes的说法,FDA这项决定的理由为“对所提出适应症的总体有效性证据不足”,并且在重新提交之前,Alkermes需要进一步开展ALKS 5461的临床试验。
MedSci原创 - ALKS,5461,重度抑郁症,Alkermes - 2018-04-03
Alkermes和Biogen宣布美国FDA接受了Diroximel富马酸盐治疗多发性硬化症的新药申请
Alkermes公司和Biogen公司近日宣布美国食品和药品监督管理局(FDA)已接受Diroximel富马酸盐治疗多发性硬化症(MS)的新药申请(NDA)。
网络 - Diroximel富马酸盐,FDA,多发性硬化症 - 2019-02-26
Alkermes的精神分裂症候选药物ALKS 3831将扩大向FDA的营销申请,以用于治疗I型双相情感障碍
Alkermes周一表示,在与FDA会面后,该制药商计划扩大其ALKS 3831在美国的营销申请,将ALKS 3831与非典型抗精神病药奥氮平和阿片类拮抗剂samidorphan联合治疗I型双相情感障碍和精神分裂症Alkermes预计将在第四季度提交申请文件,将包括ALKS 3831治疗精神分裂症患者的ENLIGHTEN临床结果,以及比较ALKS 3831和Eli Li
MedSci原创 - Alkermes,精神分裂症,ALKS,3831,FDA营销申请,I型双相情感障碍 - 2019-07-16
大冢及Lundbeck长效版Abilify新药申请审批遭FDA推迟
FDA已推迟了长效版(每月一次)重磅抗精神病药物Abilify的新药审批申请。大冢(Otsuka)制药及合作者Lundbeck,今天公布了FDA回复给公司的完整回应函(CRL),称FDA在最近的检查中发现为生产该药提供无菌水的第三方供应商存在缺陷。 "大冢正在与第三方供应商共同努力,尽早解决这一问题,并计划与FDA进行进一步的讨论以决定下一步骤,"大冢在今天的一份声明中说道。Abilify为年销
生物谷 - 大冢,Lundbeck,Abilify,FDA - 2012-08-01
FDA咨询委员会投票支持ALKS 3831治疗精神分裂症和双相障碍
FDA委员会认为,ALKS 3831中的沙美多芬可有效减轻奥氮平相关的体重增加,并且ALKS 3831的安全性已得到充分证明。
MedSci原创 - 精神分裂症,美国FDA,双相障碍,ALKS 3831 - 2020-10-10
FDA批准Vumerity治疗复发性MS
Biogen和Alkermes公司近日报道称,FDA已经批准了Vumerity(富马酸地洛西美酯)用于治疗复发形式的多发性硬化症(MS),包括活动性继发进行性疾病的患者。
MedSci原创 - FDA,Vumerity,复发性MS - 2019-10-31
强生提前终止精神分裂症III期研究
强生(JNJ)3月20日宣布,遵循独立数据监测委员会(IDMC)基于积极疗效数据所做出的建议,该公司已提前终止了有关精神分裂症药物—帕利哌酮棕榈酸酯3个月配方(paliperidone palmitate 3-month formulation)的一项III期研究,这是一种实验性药物,用于精神分裂症成人患者的治疗。 该国际性、随机、多中心、双盲III期临床试验,评估了帕利哌酮棕榈酸酯3个月配方相
生物谷 - 新药,FDA - 2014-03-21
新型抗精神分裂症药物中的“四大金刚”
SZ患者容易反复发作、反复住院,需要长期药物维持治疗。治疗精神分裂症药物较多,不同药物治疗效果也存在差异。
MedSci原创 - 抗精神分裂症药物,氨磺必利 - 2022-12-19
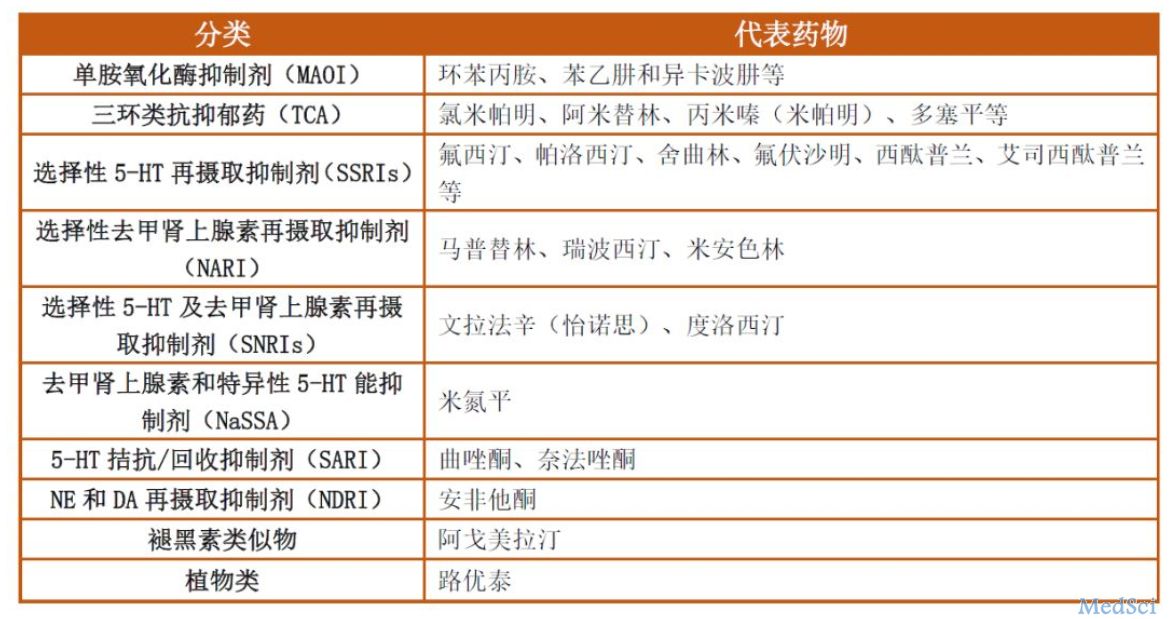
世界精神卫生日 | 抗抑郁药物的百年纵览
2018年10月10日是第25个世界精神卫生日。根据世界卫生组织统计,全世界抑郁症患者达3亿以上,而其中每年全球因抑郁症自杀死亡人数约100万,预计到2020年,抑郁症可能成为仅次于心脑血管病的人类第二大疾病。不同于心脑血管疾病多见于高龄患者,半数精神疾病始于14岁。就青少年的疾病负担而言,抑郁症是第三大原因。自杀是15-29岁人群的第二大死亡原因。为呼吁人们认识到帮助年轻人从小建立心理适应力
火石创造 - 抗抑郁药物 - 2018-10-10
10家制药企业跻身美国500强
6月7日,财富中文网与英文网全球同步发布2017年《财富》美国500强排行榜,从整体来看,今年的上榜门槛较去年稍有提升,营业收入为51.45亿美元。上榜的500家公司总收入达12.06万亿美元,相当于2016年美国GDP的65%左右。
医药观察家网 - 制药企业,500强 - 2017-06-10
2015年15大畅销新药出炉
药物开发者经常以对病人的价值为新药的高昂价格辩护,但是很少有人怀疑新药给生物制药公司提供另一种类型的价值,也就是能够通过几年有时几十年收回高昂的研发、临床试验和商业化成本而获得利润。 尽管去年新上市的药物没有一种达到成为重磅炸弹药物所需的10亿美元销售额门槛,但是排名前五中的一种新药如果其销售额再增加1亿多美元就接近这一门槛了。2015年期间投入市场的10种新药实现1000万~1亿美
生物谷 - 药物,新药,销售额,赛诺菲,艾伯维,葛兰素史克,罗氏,礼来 - 2016-03-08
Alkermes治疗MS药物进入临床一期研究
最近Alkermes公司开发的治疗多发性硬化症药物ALKS8700进入临床一期研究,公司希望这一产品在未来能够与Biogen公司治疗多发性硬化症的长效药Tecfidera抗衡。
生物谷 - 多发性硬化症,MS药物 - 2014-07-21
FDA重审3只被拒减肥药 减肥新药审批迎来拐点
2012年以来,美国FDA将对此前在2010年被拒绝的3只减肥药物进行重新审查。而至于这3只药物可否获批,医学界大多持观望的态度。医学界怀疑的并不是这些减肥药的疗效,而是它们的安全性,虽然业界也非常渴望在这一治疗领域取得重大突破。 自从上一只减肥药物获批销售以来,时间已经整整过去了13年。最后一只获得批准的减肥药是罗氏生产的赛尼可(Xenical),于1999年获得批准。 Orlistat:审
MedSci原创 - 减肥药,FDA - 2012-03-16
为您找到相关结果约24个