Circulation:减少微动脉肌化可预防自发性脑出血
2020-08-10 MedSci原创 MedSci原创
自发性深部脑出血是中风的一种毁灭性类型。小动脉壁破裂部位的平滑肌细胞变性可能足以引起出血。但深部脑出血在侵略性小血管疾病中少见,研究人员推测自发性深部脑出血可能还需要另一种细胞缺陷的参与。
自发性深部脑出血(ICH)是中风的一种毁灭性的类型,无特殊治疗方法。有人认为小动脉壁破裂部位的平滑肌细胞(SMC)变性可能足以引起出血。但深部脑出血在某些以小动脉SMC变性为特征的侵略性小血管疾病中很少见。Ratelade等人假设ICH的发生可能还需要另一种细胞缺陷的参与。
研究人员采用Col4a1+/G498V和Col4a1+/G1064D小鼠品系来研究自发性深部ICH的遗传模型,这些小鼠品系针对IV型胶原的α1链进行了突变。研究人员分析了脑视网膜微血管,进行了基因拯救实验、血管反应性分析和计算模型。并检查了散发的深部脑出血患者的死后脑组织。
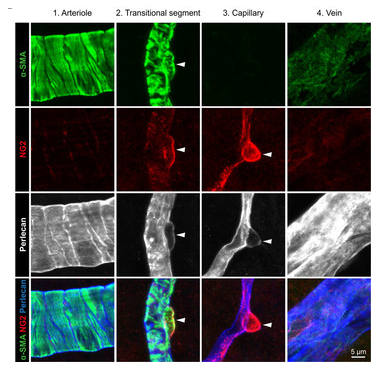
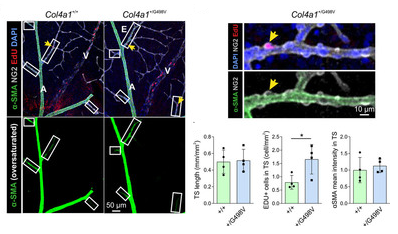
研究人员在正常的脑视网膜血管系统中确定了小动脉和毛细血管之间的一个新区段,称为过渡区段(TS),它被不同于SMC和周细胞的壁细胞覆盖。在Col4a1突变小鼠中,其TS过度肌化,壁细胞增生,表达更多的收缩蛋白,而上游小动脉表现出SMC缺失。在出生后的成熟过程中,壁细胞的增殖会有短暂的增加。在Col4a1+/G498V小鼠中,与突变的动脉不同,突变的脑微血管的SM基因和Notch3靶基因显著上调,而Notch3表达减少,进而预防ICH。
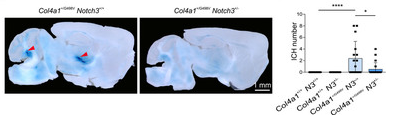
视网膜分析显示,在Col4a1+/G498V,Notch3 +/-小鼠中,TS的过度肌化减弱,但小动脉SMC的缺失没有改变。此外,视网膜TS的过度肌化增加了其收缩力和张力,并增加了上游小动脉的血管内压力。研究人员在散发的深部脑出血患者的脑组织中也发现了TS过度肌化和局灶性小动脉SMC缺失。
本研究结果显示,在Col4a1突变小鼠中,通过增加Notch3活性,TS过度肌化,通过增加上游动脉的血管内压力和促进其在SMC缺失部位发生血管破裂来参与ICH的发生。总而言之,本研究提示,这2个相互促进的血管缺损可能代表了深部ICH的一般机制。
原始出处:
Julien Ratelade,et al. Reducing Hypermuscularization of the Transitional Segment Between Arterioles and Capillaries Protects Against Spontaneous Intracerebral Hemorrhage. Circulation. 2020;141:2078–2094
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习了
92
#自发性脑出血#
37
#自发性#
27