卒中原因找不到,该抗凝还是抗血小板?
2019-05-08 Dorothy 医学界神经病学频道
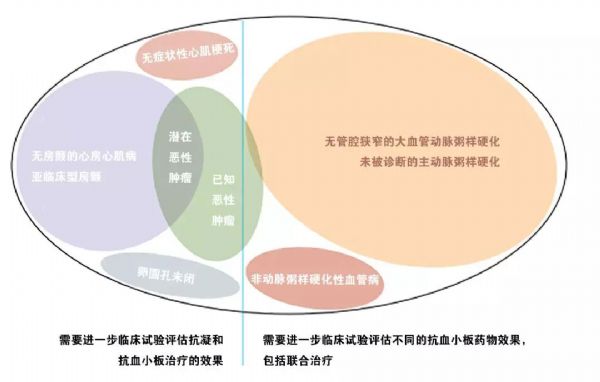
临床上,我们经常遇到一些缺血性卒中病人,没有什么常见的危险因素,血脂血压血糖都不高,不抽烟不喝酒,没有房颤,易栓症、血管炎都查了还是没毛病……那到底为什么卒中会找到他们头上?

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习谢谢分享
67
谢谢分享
81
卒中虽然是临床上常见病,溶栓,取栓等血管内治疗也很成熟,但是仍然有很多未知问题有待认知!
45