禁食用于抗癌:谣言还是科学?
2020-05-04 网络 网络
现在医学研究新发现,禁食(fasting)或禁食模拟饮食法(fasting mimicking diet, FMD)竟然可以提升癌症放/化疗效果,减轻副作用。 科学家说的“禁食&rdquo
现在医学研究新发现,禁食(fasting)或禁食模拟饮食法(fasting mimicking diet, FMD)竟然可以提升癌症放/化疗效果,减轻副作用。 科学家说的“禁食”疗法类似某些宗教奉行的“斋戒”习俗,信徒每天日出到日落期间禁止饮食,据说是为了净化身体。从生物医学角度来看,禁食本质就是卡路里限制或者限制特定食物成分配比,用大白话说就是短期内不吃或少吃。
意大利FITC分子癌症研究所的Irene Caffa和她同事做了这样一个实验,将几种不同的实体瘤细胞株,包括非小细胞肺癌细胞HCC827和H3122、乳腺癌细胞BT474和SKBR3、肠癌细胞HCT116“饥饿培养“24小时后, 加入相应的化疗药物,3天后检测细胞存活率。
短期禁食,可减轻放化疗不良反应-
在瓦尔特·隆哥教授的这项研究中,研究者在使用高剂量的化疗依托泊苷(80毫克/千克)之前让小鼠禁食48小时。23只老鼠中10只没有禁食的都死于化疗的毒性。没有禁食并且活下来的小鼠也表现出中毒症状,这些症状包括:行动不便,毛发竖起和驼背。与此相反,在禁食小鼠中,17只中只有一只死亡。并且这些禁食小鼠也没有表现焦虑或痛苦的迹象。
这项研究证实, 禁食能够减少化疗药物对实验鼠的副作用和死亡率,并能提升老年鼠的免疫力。
结果发现, 饥饿+化疗联合应用能将某些癌细胞杀伤率提高1~4倍! 在小鼠癌症模型中同样有效。
实验所用的药物特罗凯(erlotinib)、易瑞沙(gefitinib)、拉帕替尼(lapatinib)和格列卫(imatinib)等是靶向药,临床上广泛用于HER2或EGFR突变的癌症治疗。Changhan Lee和其同事在17种不同种类的癌细胞和7种小鼠的不同癌症模型亦证明禁食和化疗联用功效显著增加,其中15种肿瘤的化疗效果,明显高于单独使用化疗组,肿瘤体积缩小,体重增加。说明禁食后的癌细胞而不是正常细胞显然更容易被化疗所杀死。图1就概括说明了禁食+放/化疗的优势所在。
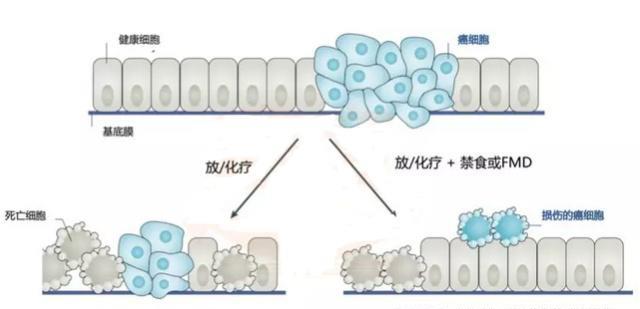
图1. 示意图说明禁食在放/化疗中的好处。正常细胞损伤程度减低,增加化疗对癌细胞的杀伤力
说到癌症治疗,临床医生基本采用化疗、放疗、手术和免疫治疗这几类手段或其组合,无论何种治疗策略,常见的头疼问题是疗效差强人意或/和伤及无辜细胞的毒副作用。
既然禁食对放化疗的增强作用已经在很多细胞或小鼠癌症模型中得到确认,那么,“禁食+ 放化疗“方案在临床癌症治疗中究竟效果如何呢?由于该癌症治疗策略新颖,到目前为止,只有4篇正式公开发表的结果,研究结论总结在如下表格1。
表1. “禁食 + 放化疗“方案在临床癌症治疗先导性研究结果


由此看来,禁食让癌细胞对放/化疗更敏感,提高正常细胞如造血干细胞,免疫细胞抵抗放/化疗毒副作用的能力,病人的生活质量改善明显。
另外有6个关于禁食和癌症的临床试验正在美国和欧洲的医院进行当中,招募的病人数扩大至300人,最快今年将报道部分结果(表2)

美国南加州大学的Longo VD教授是禁食与癌症治疗领域的先锋,2018年11月他受邀在Nature Reviews,Cancer子刊(影响因子43)上发表了综述文章,阐述了禁食增强放/化疗功效,提升患者生存质量的细胞分子生物学机理:
1)从整体上看,禁食或FMD导致血液中的葡萄糖、胰岛素样生长因子1(IGF1)、胰岛素、瘦素水平降低;脂联素adiponectin和酮体的水平升高;能量代谢通路IGF1R–AKT–mTOR–S6K 和cAMP–PKA被抑制;
2)饥饿诱导正常细胞和癌细胞压力抗性差别。饥饿刺激下,正常细胞下调细胞增殖速度迫使细胞进入“维持模式”从而更能“容忍”放/化疗的伤害;
3)癌细胞增殖无度,营养索求无度,氧化应激能力缺失,对放/化疗敏感性增加;
4)禁食刺激淋巴细胞前体细胞扩增,促进机体对抗癌细胞的免疫反应。
简而言之:禁食使疯狂扩张的癌细胞脆弱,放/化疗再临门致命一击,癌细胞崩溃。
禁食虽好,但要控制好时间-
禁食虽然有助于减轻放化疗的不良反应,但是,禁食必须控制好时间,切不可盲目进行。
关于禁食,目前研究最广泛的三种禁食方案是 隔日禁食、5:2间断性禁食(每周禁食2天)、限时进食。对于肿瘤患者而言,我们提倡间断性禁食。
间断性禁食,是指在正常饮食期间短时期的禁食、不禁水,禁食的时间通常为24~48小时,两次禁食的时间间隔目前无特殊要求, 可以每3~5 天禁食1次,也可以1周禁食1次。
美国南加州大学-诺里斯综合癌症中心针对禁食时间进行了相关测试, 在接受以铂(顺铂或卡铂)为基础的鸡尾酒化疗的患者身上,最多长达72小时的禁食(48小时前化疗输注+后24小时化疗输注)被认为是安全和可行的,而且不会对化疗疗效有明显的负面影响。
复旦大学附属肿瘤医院缪长虹、同济大学医学院张小平、复旦大学基础医学院马端等合作,在 Nature 子刊 Nature Communications 期刊发表了题为:Fasting inhibits aerobic glycolysis and proliferation in colorectal cancer via the Fdft1-mediated AKT/ mTOR/HIF1α pathway suppression 的研究论文。
该研究发现,FDFT1是禁食的关键下游靶标,禁食能够上调FDFT1的表达,抑制AKT/mTOR/HIF1α信号转导,从而抑制结直肠癌细胞的有氧糖酵解和增殖,该研究阐明了禁食能够抑制结直肠癌的详细分子机制,也表明了禁食和抑制mTOR通路是治疗结直肠癌的潜在方法。

之前的研究表明,禁食在包括结直肠癌在内的多种癌症中具有广泛的抗肿瘤作用。但是背后的具体机制尚不清楚。因此,研究团队进行的这项研究禁食对结直肠癌的具体影响。
首先,研究团队发现,FDFT1基因的表达下调与结直肠癌的的恶性进展和不良预后相关。FDFT1在结直肠癌中起着至关重要的肿瘤抑制作用。
接下来,研究团队发现禁食会上调FDFT1的表达,从而抑制结直肠癌细胞有氧糖酵解和增殖。从机制上讲,FDFT1通过负调节AKT/mTOR /HIF1α信号传导来执行其肿瘤抑制功能。此外,该研究还发现,mTOR抑制剂能够通过抑制结直肠癌细胞增殖,与禁食协同作用。这些结果表明,FDFT1是禁食的关键下游靶标,并可能参与结直肠癌细胞的葡萄糖代谢。
这项研究表明,胆固醇生成基因FDFT1与糖酵解之间有潜在的相互作用,对结直肠癌具有治疗意义,揭示了禁食通过FDFT1介导的AKT/mTOR/HIF1α通路抑制大肠癌细胞的有氧糖酵解和增殖,从而抑制结直肠癌,也表明了禁食和抑制mTOR通路是治疗结直肠癌的潜在方法。
禁食也有弊端,并不是每个人都适合-
虽然,禁食对于肿瘤的治疗有着积极意义,但也发现了一定的副作用,如可能出现头痛,头晕,恶心和虚弱。一些人起初可能还会感到饥饿,特别是对于习惯了吃早餐和宵夜的人。
参考文献
[1] J.E. Cropley, S.A. Eaton, A. Aiken, P.E. Young, E. Giannoulatou, J.W.K. Ho, M.E. Buckland, S.P. Keam, G. Hutvagner, D.T. Humphreys, K.G. Langley, D.C. Henstridge, D.I.K. Martin, M.A. Febbraio, and C.M. Suter, Male-lineage transmission of an acquired metabolic phenotype induced by grand-paternal obesity. Mol Metab 5 (2016) 699-708.
[2] J. Day, S. Savani, B.D. Krempley, M. Nguyen, and J.B. Kitlinska, Influence of paternal preconception exposures on their offspring: through epigenetics to phenotype. Am J Stem Cells 5 (2016) 11-8.
[3] S. Di Biase, C. Lee, S. Brandhorst, B. Manes, R. Buono, C.W. Cheng, M. Cacciottolo, A. Martin-Montalvo, R. de Cabo, M. Wei, T.E. Morgan, and V.D. Longo, Fasting-Mimicking Diet Reduces HO-1 to Promote T Cell-Mediated Tumor Cytotoxicity. Cancer Cell 30 (2016) 136-146.
[4] S.P. Bauersfeld, C.S. Kessler, M. Wischnewsky, A. Jaensch, N. Steckhan, R. Stange, B. Kunz, B. Bruckner, J. Sehouli, and A. Michalsen, The effects of short-term fasting on quality of life and tolerance to chemotherapy in patients with breast and ovarian cancer: a randomized cross-over pilot study. BMC Cancer 18 (2018) 476.
[5] I. Caffa, V.D. Longo, and A. Nencioni, Fasting plus tyrosine kinase inhibitors in cancer. Aging (Albany NY) 7 (2015) 1026-7.
[6] C. Lee, L. Raffaghello, S. Brandhorst, F.M. Safdie, G. Bianchi, A. Martin-Montalvo, V. Pistoia, M. Wei, S. Hwang, A. Merlino, L. Emionite, R. de Cabo, and V.D. Longo, Fasting cycles retard growth of tumors and sensitize a range of cancer cell types to chemotherapy. Sci Transl Med 4 (2012) 124ra27.
[7] A. Nencioni, I. Caffa, S. Cortellino, and V.D. Longo, Fasting and cancer: molecular mechanisms and clinical application. Nat Rev Cancer 18 (2018) 707-719.
[8] R.S. Sohal, and R. Weindruch, Oxidative stress, caloric restriction, and aging. Science 273 (1996) 59-63.
[9] L. Bordone, and L. Guarente, Calorie restriction, SIRT1 and metabolism: understanding longevity. Nat Rev Mol Cell Biol 6 (2005) 298-305.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#谣言#
45