【协和医学杂志】《脊柱关节炎靶向药物治疗专家共识》要点解读
2024-02-03 协和医学杂志 协和医学杂志 发表于陕西省
该共识围绕靶向药物治疗SpA的原则、适用人群、用药前筛查、用药时机、药物选择和转换、合并用药、不良反应监测、特殊人群用药注意事项等,共形成13条推荐意见。
脊柱关节炎(SpA)是一组以中轴骨和/或外周关节受累为主的慢性炎症性和致残性风湿免疫病,好发于青年男性,临床异质性强,除关节受累外还可合并银屑病、炎症性肠病、眼炎等,常伴发心脑血管疾病等合并症,严重影响患者的身体功能和生活质量,给患者和社会带来沉重负担。
一般而言,SpA可分为中轴型和外周型2个亚型,中轴型包括强直性脊柱炎(AS)和放射学阴性中轴型SpA(nr-axSpA),外周型包括银屑病关节炎(PsA)、炎症性肠病性关节炎、反应性关节炎、未分化SpA和幼年型SpA。我国SpA的患病率为0.93%,且呈逐年升高的趋势,据估计目前我国SpA患者超过70万人[1]。
早期诊断、早期规范治疗是延缓SpA疾病进展、改善预后的关键。在靶向药物出现前,SpA的治疗主要采用非甾体抗炎药(NSAIDs)和改善病情抗风湿病药(DMARDs)。随着对SpA发病机制研究的不断深入,研究人员发现一些炎症细胞因子或通路在SpA的发病中发挥重要作用。
靶向细胞因子或通路的药物具有快速改善症状、延缓疾病进展、提高生活质量、减少残疾的特点,目前国内外已获批用于治疗SpA的靶向药物包括生物靶向药物和合成小分子靶向药物。生物靶向药物包括肿瘤坏死因子(TNF)-α抑制剂(如依那西普、英夫利昔单抗、阿达木单抗、戈利木单抗、培塞利珠单抗)、白细胞介素(IL)-12/23抑制剂(如乌司奴单抗、古塞奇尤单抗)、IL-17A抑制剂(如司库奇尤单抗、依奇珠单抗)和选择性T细胞共刺激调节剂(如阿巴西普)。合成小分子靶向药物包括Janus激酶(JAK)抑制剂(如托法替布、乌帕替尼等)和磷酸二酯酶4抑制剂(如阿普米司特)。
由于不同靶向药物的作用机制不同,获批的适应证、禁忌证、不良反应等也不尽相同,对特定临床表现的研究证据及疗效也存在差异,因此如何选择靶向药物,做到合理、精准、规范使用具有重要临床意义。为规范我国临床医师靶向药物的使用,由国家皮肤与免疫疾病临床医学研究中心牵头组织,联合中国医师协会风湿免疫专科医师分会、中国康复医学会风湿免疫专业委员会和中国研究型医院学会风湿免疫专业委员会,遵循共识制定的国际规范,制定了我国首部《脊柱关节炎靶向药物治疗专家共识》(下文简称“共识”),并于2023年6月正式发布[2]。
该共识围绕靶向药物治疗SpA的原则、适用人群、用药前筛查、用药时机、药物选择和转换、合并用药、不良反应监测、特殊人群用药注意事项等,共形成13条推荐意见。本文将对共识主要推荐内容进行解读,以帮助临床医师更好地理解和掌握其核心内容。
1 靶向药物治疗的适用人群
SpA的标准初始治疗药物为NSAIDs,其可减轻患者临床症状[3-4],但NSAIDs需最大剂量且治疗2周以上才能获得最佳疗效[5]。与按需应用相比,最大剂量连续治疗可减轻脊柱融合[6]。此外,其他非药物治疗(如物理治疗等)亦应作为标准初始治疗的一部分。但部分患者对NSAIDs治疗反应差,病情无法得到有效控制。研究显示,TNF-α抑制剂、IL-17A抑制剂、JAK抑制剂均可改善NSAIDs治疗失败的中轴型SpA患者病情。
因此,共识建议先后经至少2种NSAIDs最大剂量治疗>4周效果仍不佳,或先后经过至少2种NSAIDs治疗2个月病情仍活动,或对NSAIDs不耐受,或经1种NSAIDs治疗但附着点炎和中轴症状仍活动的SpA患者,应考虑应用靶向药物治疗。对于外周关节病变突出、无或轻度中轴关节病变的患者,若NSAIDs治疗效果欠佳,DMARDs药物(如柳氮磺胺吡啶[7]、甲氨蝶呤[8]等)可改善症状。如疾病控制不佳,共识建议可考虑更换为靶向药物治疗。
PsA临床表现复杂,需根据病变部位和受累程度选择治疗方案[9]。若银屑病皮损范围广、病情重,特别是累及头面部、指(趾)甲及生殖器等特殊部位时,可在初始治疗时即使用靶向药物[10]。若PsA患者以外周关节受累为主、附着点炎或中轴症状突出,可在初始治疗时即使用靶向药物[9]。
2 靶向药物治疗前应进行疾病活动度评估
疾病活动度是决定SpA患者使用靶向药物治疗的重要依据[3]。中轴型SpA常用的疾病活动度评估工具包括强直性脊柱炎疾病活动评分(ASDAS)和Bath强直性脊柱炎病情活动指数( BASDAI)。
2017年SpA国际工作组推荐,中轴型SpA患者的ASDAS-C反应蛋白(CRP)<1.3或BASDAI<2为疾病缓解,ASDAS-CRP<2.1或BASDAI<4为低疾病活动度[11],ASDAS-CRP>2.1为高疾病活动度,ASDAS-CRP>3.5为极高疾病活动度。PsA异质性较强,常用的评估工具为PsA疾病活动指数(DAPSA)和最低疾病活动度(MDA)。高疾病活动度者应使用靶向药物治疗。
SpA病情进展将引起不可逆的结构损伤,附着点炎是其结构进展的基础,进而导致骨损伤[12],而髋关节受累、PsA常见的远端指间关节受累,可导致患者功能障碍或残疾。如SpA患者出现附着点炎及髋关节、远端指间关节受累,除高疾病活动度外,上述可造成功能障碍或残疾的特殊关节受累,均为应用靶向药物治疗的强指征,应尽早开始靶向药物治疗[13]。
3 靶向药物治疗前应进行感染筛查
由于靶向药物的应用可能升高感染风险并激活潜伏性感染[14],因此在应用靶向药物前应对感染进行评估,以尽可能减少不良事件的发生。
我国是乙型肝炎病毒(HBV)感染高负担国家[15],HBV感染的再激活可能引起肝炎复发、暴发性肝衰竭甚至死亡。HBV感染后TNF-α生成增多,提示TNF-α可抑制HBV病毒的复制。乙型肝炎表面抗原(HBsAg)阳性患者接受TNF-α抑制剂治疗后,HBV再激活的风险明显增加,可达27%~39%,既往HBV感染者亦有HBV再激活的风险[16-17]。JAK抑制剂可下调干扰素通路对病毒的抑制,亦有关于HBV再激活的文献报道[18]。
尽管IL-17A可能参与HBV的清除,但关于IL-17A抑制剂的相关临床研究和观察性报道均未证实其增加HBV再激活的风险[19]。慢性丙型肝炎病毒(HCV)感染者应用靶向药物治疗后,HCV再激活的风险相对较小。因此,共识推荐在开始靶向药物治疗前常规筛查HBsAg、HBV表面抗体、HBV核心抗体及HCV抗体,HBsAg和/或HBV核心抗体阳性者应进一步检测HBV-DNA。
我国亦是结核病高负担国家,SpA患者潜伏性结核感染率高达25.72%[20]。TNF-α在肉芽肿形成中发挥重要作用,应用TNF-α抑制剂可造成潜伏性结核感染激活。Meta分析显示,应用TNF-α抑制剂治疗的炎症性关节炎患者其结核再激活风险增高3倍,且在亚洲患者中更为突出[21]。经JAK抑制剂治疗后,结核感染再激活的风险亦有所升高[14,22]。目前,虽然在IL-17A抑制剂相关临床研究中未发现结核复发的证据[23],但仍需进一步观察。因此,共识推荐在开始靶向药物治疗前应常规进行活动性和潜伏性结核感染筛查。
4 初始靶向治疗药物种类选择
随机对照临床试验证实,TNF抑制剂和IL-17A抑制剂均可有效控制AS患者的炎症,改善临床症状,延缓影像学进展。国际SpA诊治指南推荐TNF抑制剂或IL-17A抑制剂作为AS的首选靶向治疗药物,二者无优先顺序[3]。
因此,本共识推荐将TNF抑制剂或IL-17A抑制剂作为中轴型SpA患者初始治疗的靶向药物。美国食品药品监督管理局(FDA)和欧盟药品管理局等均已批准TNF抑制剂和IL-17A抑制剂治疗nr-axSpA,但我国上市的TNF抑制剂和IL-17A抑制剂仅获批AS这一适应证,尚无药物获批用于治疗nr-axSpA。
PsA临床表现复杂,需根据患者受累情况选择治疗药物。TNF抑制剂[24-27]、IL-17A抑制剂[28]、JAK抑制剂[29-31]、IL-12/23抑制剂[32-33]、选择性T细胞共刺激调节剂[34]、PDE4抑制剂[35]均可有效改善PsA患者的外周关节炎及皮肤病变。
针对PsA患者开展的“头对头”临床研究表明,在银屑病皮肤病变治疗方面,IL-17A抑制剂疗效优于TNF抑制剂,在关节病变方面二者疗效相似[36-37]。因此,若PsA患者银屑病病变突出,应首选IL-17A抑制剂。TNF抑制剂和IL-17A抑制剂对指(趾)甲损害治疗有效[25-26,38-39],且均可有效治疗附着点炎[25-28,40-42]。TNF抑制剂、IL-17A抑制剂和IL-12/23抑制剂均可有效治疗指(趾)炎[25-28,41-43]。由此可见,可根据PsA患者不同临床表现选择有效的靶向药物。
JAK抑制剂托法替布[29]和乌帕替尼[30-31]均对PsA具有较好的疗效及安全性,二者与阿达木单抗相比,治疗PsA的疗效(皮损、关节炎等方面)无显著统计学差异。国外指南已推荐JAK抑制剂用于PsA的治疗[3,44],托法替布和乌帕替尼已在我国获批用于PsA的治疗。
阿巴西普对PsA的治疗亦有效,但优先级在TNF抑制剂、IL-17A抑制剂、IL-12/23抑制剂之后[34]。对于上述首选靶向药物治疗效果不佳、无法耐受或存在禁忌证者,包括既往存在严重感染史、反复感染、合并充血性心力衰竭或脱髓鞘疾病等[44],可选择阿巴西普。
除关节、皮肤损害外,阿普米司特治疗PsA的附着点炎和指(趾)炎亦有效,但单药治疗需较大剂量[35]。国外指南推荐,当阿普米司特治疗效果不佳时仍考虑更换为上述首选的靶向药物[44]。
5 SpA患者合并葡萄膜炎及炎症性肠病的治疗选择
SpA患者的关节外表现多种多样,且不同临床表现与不同细胞因子的通路激活相关,应根据临床表现选择合适的靶向药物[4]。在葡萄膜炎、炎症性肠病中,TNF-α通路发挥重要作用,而在皮肤病变中IL-23/IL-17通路发挥重要作用。因此,应选择对应通路的靶向药物[3,9]。
葡萄膜炎是SpA重要的关节外表现,可导致严重和不可逆的视力丧失,需积极治疗。SpA合并葡萄膜炎最常见于AS,可达23%[45]。15.9%的nr-axSpA患者、3%的PsA患者可合并葡萄膜炎。
在既往发生过葡萄膜炎的患者中,单克隆抗体类TNF抑制剂(如英夫利昔单抗、阿达木单抗、培塞利珠单抗、戈利木单抗)被证实可有效预防葡萄膜炎的复发,疗效优于依那西普[46-47]。而IL-17A抑制剂治疗葡萄膜炎的效果不确定。因此,对于合并复发性葡萄膜炎的SpA患者,建议优先使用单克隆抗体类TNF抑制剂,而非融合蛋白类TNF抑制剂及IL-17A抑制剂。
炎症性肠病也是SpA常见的关节外表现,6.4%的AS患者、4.1%的nr-axSpA患者、3%的PsA患者可合并炎症性肠病[45]。目前研究显示,单克隆抗体类TNF抑制剂对炎症性肠病的效果优于融合蛋白类[48-50]。IL-17A抑制剂具有诱发或加重炎症性肠病的风险,因此对于合并炎症性肠病的SpA患者,建议优先使用单克隆抗体类TNF抑制剂,慎用IL-17A抑制剂。
6 AS患者应用JAK抑制剂的时机
JAK抑制剂可抑制细胞内JAK通路的信号传导,是近年上市的具有全新作用机制的口服药物。托法替布及乌帕替尼在治疗SpA方面具有一定的疗效和安全性,可快速改善关节症状,对皮损、附着点炎、指(趾)炎均有效[29-31,51-53]。
2022年,国际脊柱关节炎协会/欧洲抗风湿病联盟推荐TNF抑制剂、IL-17A抑制剂及JAK抑制剂作为传统药物治疗效果欠佳时的选择,但由于JAK抑制剂的有效性等临床观察数据较前两者少,其长期安全性有待进一步评估,因此JAK抑制剂并未作为目前治疗SpA的常规首选[9]。
我国已批准托法替布用于治疗对1种或多种TNF抑制剂疗效不佳或不耐受的活动性AS成人患者,托法替布及乌帕替尼可用于治疗对1种或多种DMARD应答不佳或不耐受的活动性PsA成人患者。美国FDA和欧盟药品管理局已批准托法替布用于治疗活动性AS和PsA,乌帕替尼用于治疗活动性AS、nr-axSpA和PsA。
7 不推荐生物制剂联合甲氨蝶呤治疗中轴型SpA
甲氨蝶呤仅对外周关节炎、关节外表现有效,对中轴型SpA的中轴关节症状无效,可在患者存在其他首选药物禁忌证、无法耐受等情况下应用。研究表明,应用生物制剂联合甲氨蝶呤治疗中轴型SpA患者,其疗效并未增加,亦未延长药物使用时间[54-55]。药代动力学研究显示,英夫利昔单抗联合甲氨蝶呤治疗中轴型SpA患者,未提升英夫利昔单抗的血药浓度[54]。此外,联合治疗可能增加不良反应的发生率。因此,共识不推荐生物制剂联合甲氨蝶呤治疗中轴型SpA。
8 靶向药物治疗期间应定期评估和监测
SpA治疗的主要目标是控制症状和体征、消除炎症、预防结构损伤、正常化或保持功能,避免药物不良反应和尽量减少合并症,优化与健康相关的长期生活质量。AS患者的高疾病活动度与其结构损伤进展、功能损害加重相关。推荐根据预定治疗目标指导SpA治疗,可根据疾病个体化确定治疗目标。一般而言,治疗目标包括骨关节病变和关节外表现的临床缓解[9]。为实现这一治疗目标,需对患者病情作出评估,以及时调整治疗方案。
ASDAS和BASDAI可用于评估靶向治疗的疗效。ASDAS的评估内容包含炎症标志物,相对较为客观,而BASDAI仅包含主观项目的评估,其客观性较差;ASDAS与患者临床结局、骨赘形成、MRI评分具有良好的相关性,优于BASDAI[56];BASDAI联合炎症指标可提升其评估的客观性。对于临床表现较为复杂的PsA,可采用DAPSA和MDA等工具进行评估。本共识推荐,对于未达治疗目标的患者,建议每1~3个月评估1次治疗反应;对于达到治疗目标的患者,建议每3~6个月评估1次疾病活动度。
在SpA的治疗过程中应密切监测药物不良反应。TNF抑制剂治疗的常见不良反应为上呼吸道感染、血细胞减少、肝酶升高,罕见不良反应为充血性心力衰竭和脱髓鞘疾病。IL-17A抑制剂治疗的常见不良反应为上呼吸道感染、鼻咽炎、头痛等,少见不良反应为念珠菌感染、诱发或加重炎症性肠病。JAK抑制剂治疗的常见不良反应为上呼吸道感染,应用JAK抑制剂的患者带状疱疹病毒感染的发生率高于TNF抑制剂;对于存在心脑血管疾病危险因素的患者,其重大心血管不良事件、血栓事件的发生风险增加,应谨慎使用JAK抑制剂并加强监测。
9 靶向药物的减/停药策略
关于SpA患者减/停靶向药物的研究较少,且均为SpA患者处于缓解或低疾病活动度状态下开展。目前尚无大规模临床研究数据能够明确界定SpA治疗达标的具体目标及其获益,但已有研究证实治疗达标可改善部分指标[57]。
对于SpA患者,低疾病活动度与药物减量后的维持缓解相关。目前尚无临床研究数据提示最佳药物减量策略,减少用药剂量或延长用药间隔均可尝试。因此,共识推荐SpA患者治疗达标、缓解或低疾病活动度至少半年后方可考虑靶向药物减量,以避免或延缓病情加重。药物减量后,患者病情可能复发或加重,因此应严密监测,定期评估疾病活动度,如出现复发则应恢复原有用药剂量。
10 根据临床情况采取个体化分层管理策略
SpA患者的临床异质性强,应根据临床表型指导靶向药物治疗和时机选择。随着靶向药物的应用越来越广泛,合并疾病已成为治疗选择时需重点考虑的因素。当患者存在治疗禁忌证或可能导致不良事件的危险因素时,应采取个体化、分层管理策略,以最大程度保障患者安全。
|
1 |
接受TNF抑制剂治疗的SpA患者发生结核感染的风险增加3倍[21]。针对我国结核负担重的现状,专家组建议活动性结核感染患者应先行标准抗结核治疗后再确定后续治疗方案;潜伏性结核感染和陈旧性结核感染的患者应预防性抗结核治疗至少4周后方可开始TNF抑制剂治疗,用药后的第3个月、第6个月进行复查,此后每6个月复查一次,直至停药后3个月,警惕潜伏性结核感染活化或新发结核感染。IL-17A抑制剂治疗SpA患者的随访研究未发现结核复发相关证据[23-24]。因此,共识指出,对于有活动性结核感染的SpA患者,不推荐采用靶向药物治疗,建议先转诊至专科医院进行抗结核治疗。对于潜伏性和陈旧性结核感染的SpA患者,优先推荐IL-17A抑制剂,在启动靶向药物治疗前应预防性进行抗结核治疗。 |
|
2 |
合并HBV感染的SpA患者,应根据感染状态进行分层管理。既往感染HBV的患者,应用免疫抑制剂治疗后可能出现HBV再激活,因此用药前需进行相应的筛查,并根据感染状态进行分层管理。预防性抗病毒治疗可显著降低HBV再激活的发生。《慢性乙型肝炎防治指南(2022年版)》[58]建议:HBsAg和/或HBV-DNA阳性者应在靶向药物治疗前进行抗病毒治疗至少1周以上,急需治疗者可同时应用药物;如患者HBV-DNA阴性,应每1~3个月监测转氨酶、HBV-DNA和HBsAg,一旦HBV-DNA或HBsAg转为阳性应立即启动抗病毒治疗。共识推荐靶向药物治疗期间,应每1~3个月监测1次转氨酶、HBV-DNA和HBsAg。 |
|
3 |
合并充血性心力衰竭的SpA患者,共识推荐优先选择IL-17A抑制剂。研究显示,依那西普、英夫利昔单抗可加重充血性心力衰竭[59],目前尚未发现IL-17A抑制剂加重充血性心力衰竭的相关研究证据[23]。因此,共识推荐合并充血性心力衰竭的SpA患者优先选择IL-17A抑制剂。 |
|
4 |
合并严重活动性感染的SpA患者,不推荐应用靶向药物。靶向药物抑制免疫系统中的细胞因子或炎症通路,可能增加感染的发生风险[14]。靶向药物治疗的常见不良反应为各种类型的感染。一项Meta分析研究显示,中轴型SpA患者应用生物制剂治疗发生感染的风险显著升高[60]。因此,对于合并严重活动性感染的SpA患者,共识指出在靶向药物治疗前应充分评估患者有无活动性感染或潜伏性感染及再感染风险。在靶向药物治疗期间,如发生严重感染应尽快停药,待感染完全控制后再决定后续治疗。 |
|
5 |
存在恶性肿瘤史的SpA患者,需综合判断其肿瘤复发风险,谨慎使用靶向药物。TNF抑制剂、IL-17A抑制剂、JAK抑制剂等的临床研究显示,其应用过程中存在少数患者发生恶性肿瘤的情况。TNF-α因参与调控肿瘤生长的病理机制,对于有恶性肿瘤病史的SpA患者,需考虑TNF抑制剂应用后肿瘤复发的潜在风险。多项研究及Meta分析提示,类风湿关节炎患者应用TNF抑制剂治疗,发生实体肿瘤的风险未增加,但发生非黑色素瘤皮肤癌的风险增加[61]。目前研究未发现IL-17A抑制剂、IL-12/23抑制剂增加实体肿瘤的发生风险。目前,尚无明确证据证实靶向药物治疗可增加恶性肿瘤的发生风险[62]。因此,对于存在恶性肿瘤病史的SpA患者,共识建议对其肿瘤类型、分期、转移风险等进行全面评估,并根据患者的意愿和医生的判断,充分权衡获益与风险,决定靶向药物的治疗选择。 |
11 靶向药物治疗前或治疗期间可接种灭活疫苗
SpA患者受疾病本身及靶向药物治疗的影响,发生流行性感冒、肺炎等的风险高于普通人群。接受免疫抑制剂治疗的大多数风湿病患者可从接种疫苗中获益。临床研究证实,风湿病患者应用靶向药物(阿巴西普、利妥昔单抗除外)治疗期间,接种流行性感冒和灭活肺炎球菌疫苗是安全有效的。因此,共识推荐SpA患者在应用靶向药物治疗前或治疗期间接种流行性感冒和肺炎球菌疫苗。由于缺乏足够的安全性证据,共识不推荐SpA患者靶向药物治疗期间接种减毒活疫苗。
接受TNF抑制剂和JAK抑制剂治疗的患者,其带状疱疹病毒再激活的发生风险明显升高。因此,共识推荐SpA患者在开始TNF抑制剂和JAK抑制剂治疗前4周应接种带状疱疹疫苗,不推荐治疗期间接种。如治疗期间发生带状疱疹,应暂停治疗至病毒感染痊愈。如反复出现带状疱疹,可考虑预防性抗病毒治疗。
12 靶向药物治疗的SpA患者围术期管理
TNF-α在组织修复过程中发挥重要作用,应用TNF抑制剂除造成围术期感染风险升高外,还导致伤口愈合延迟或愈合不良,因此应于术前停用1个正常用药周期[63]。关于IL-17A抑制剂、IL-12/23抑制剂对感染及伤口愈合的影响,目前尚无相关研究数据,出于安全考虑,共识建议术前停用1个正常用药周期。
JAK抑制剂应在术前3 d停用,如既往存在应用托法替布造成假体关节感染史,建议围术期不再使用JAK抑制剂[63]。如术后伤口表现为愈合征象(通常在术后14 d左右)、已拆除所有缝线/皮钉,且手术伤口无明显水肿、红斑、渗出物,无非手术部位感染的临床证据时,可重新开始靶向药物治疗[63]。关于SpA患者围术期靶向药物应用的建议详见表1。
表1 脊柱关节炎患者围术期靶向药物应用建议
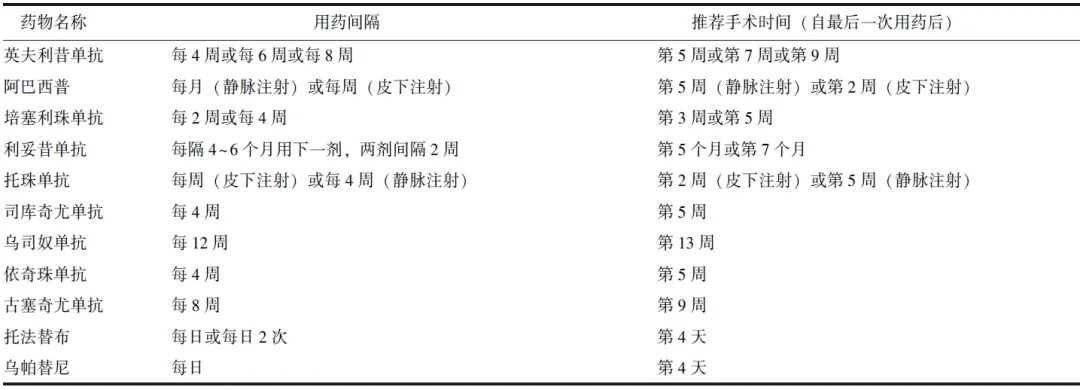
13 妊娠期和哺乳期靶向药物选择
SpA对患者的生育能力无显著影响,应重视患者的生育需求,及时调整药物种类和剂量以最大限度保证患者生育顺利、母胎健康。大多数生物制剂含Fc段,胎盘表达的Fc段受体可与药物结合,并将其转运至胎儿血液循环,对胎儿产生影响。经特殊设计后,不含Fc段的生物制剂(如培塞利珠单抗)不能转运至胎儿体内,目前临床研究显示其应用于妊娠全程是安全的[64]。
基于不同生物制剂独特的分子结构、半衰期、胎盘转运差异等因素考虑,共识推荐在妊娠20周前停用英夫利昔单抗和阿达木单抗,在妊娠30~32周停用依那西普。由于缺乏胎儿安全性相关数据支持,共识建议妊娠期停用戈利木单抗。
在类风湿关节炎患者中开展的小样本研究显示,接受TNF抑制剂治疗的患者,其乳汁内药物浓度极低或无法检测出,因此哺乳期可考虑继续使用TNF抑制剂。而对于其他靶向药物,目前尚需进一步积累相关安全性证据[65]。因此,共识不推荐妊娠期和哺乳期SpA患者应用除TNF抑制剂外的靶向药物。SpA患者妊娠期和哺乳期靶向药物应用建议详见表2[66]。
表2 脊柱关节炎患者不同妊娠阶段和哺乳期靶向药物应用建议
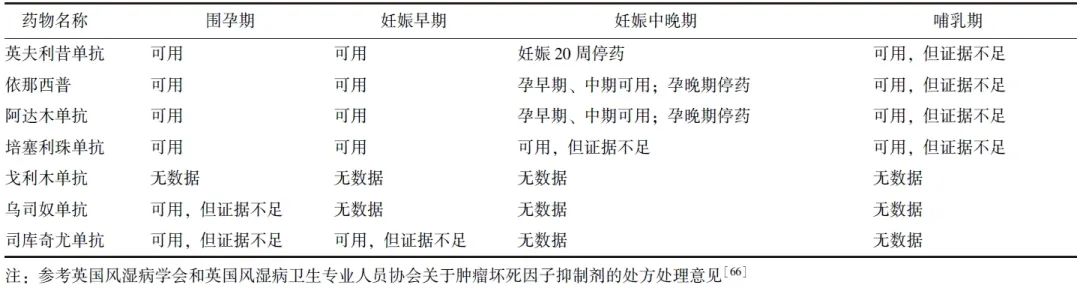
根据现有研究证据,男性SpA患者备孕期间可继续使用TNF抑制剂(包括依那西普、英夫利昔单抗、阿达木单抗和戈利木单抗),其他靶向药物的安全性证据尚需进一步积累,共识不推荐男性患者备孕期间应用除TNF抑制剂外的靶向药物。
14 小 结
《脊柱关节炎靶向药物治疗专家共识》对SpA患者靶向药物治疗相关事项均给出了详实的指导意见和推荐建议,涉及内容广泛,密切结合临床实际,可操作性强,适合我国国情,对于提升我国SpA规范化治疗、规范SpA患者靶向药物使用将发挥重要指导作用。
参考文献
[1]Ng S C, Liao Z T, Yu D T T, et al. Epidemiology of spondyloarthritis in the People's Republic of China: review of the literature and commentary[J]. Semin Arthritis Rheum, 2007, 37(1): 39-47.
[2]国家皮肤与免疫疾病临床医学研究中心(北京协和医院), 中国医师协会风湿免疫专科医师分会, 中国康复医学会风湿免疫专业委员会, 等. 脊柱关节炎靶向药物治疗专家共识[J]. 中华内科杂志, 2023, 62(6): 606-618.
[3]Ramiro S, Nikiphorou E, Sepriano A, et al. ASAS-EULAR recommendations for the management of axial spondyloarthritis: 2022 update[J]. Ann Rheum Dis, 2023, 82(1): 19-34.
[4]Ward M M, Deodhar A, Gensler L S, et al. 2019 Update of the American College of Rheumatology/Spondylitis Associa-tion of America/spondyloarthritis research and treatment network recommendations for the treatment of ankylosing spondylitis and nonradiographic axial spondyloarthritis[J]. Arthritis Rheumatol, 2019, 71(10): 1599-1613.
[5]Van Der Heijde D, Baraf H S B, Ramos-Remus C, et al. Evaluation of the efficacy of etoricoxib in ankylosing spondylitis: results of a fifty-two-week, randomized, controlled study[J]. Arthritis Rheum, 2005, 52(4): 1205-1215.
[6]Wanders A, Van Der Heijde D, Landewé R, et al. Nonsteroidal antiinflammatory drugs reduce radiographic progression in patients with ankylosing spondylitis: a randomized clinical trial[J]. Arthritis Rheum, 2005, 52(6): 1756-1765.
[7]Clegg D O, Reda D J, Weisman M H, et al. Comparison of sulfasalazine and placebo in the treatment of ankylosing spondylitis. A department of veterans affairs cooperative study[J]. Arthritis Rheum, 1996, 39(12): 2004-2012.
[8]Gonzalez-Lopez L, Garcia-Gonzalez A, Vazquez-Del-Mercado M, et al. Efficacy of methotrexate in ankylosing spondylitis: a randomized, double blind, placebo controlled trial[J]. J Rheumatol, 2004, 31(8): 1568-1574.
[9]Gossec L, Baraliakos X, Kerschbaumer A, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update[J]. Ann Rheum Dis, 2020, 79(6): 700-712.
[10]中华医学会皮肤性病学分会, 中国医师协会皮肤科医师分会, 中国中西医结合学会皮肤性病专业委员会. 中国银屑病生物制剂治疗指南(2021)[J]. 中华皮肤科杂志, 2021, 54(12): 1033-1047.
[11]Machado P, Landewé R, Lie E, et al. Ankylosing spondylitis disease activity score (ASDAS): defining cut-off values for disease activity states and improvement scores[J]. Ann Rheum Dis, 2011, 70(1): 47-53.
[12]Schett G, Lories R J, D'Agostino M A, et al. Enthesitis: from pathophysiology to treatment[J]. Nat Rev Rheumatol, 2017, 13(12): 731-741.
[13]Rocha F A C, Pinto A C M D, Lopes J R, et al. Tumor necrosis factor inhibitors prevent structural damage in hips in ankylosing spondylitis-time to reconsider treatment guidelines? A case series and review of literature[J]. Clin Rheumatol, 2021, 40(5): 1881-1887.
[14]Sepriano A, Kerschbaumer A, Bergstra S A, et al. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2022 update of the EULAR recommendations for the management of rheumatoid arthritis[J]. Ann Rheum Dis, 2023, 82(1): 107-118.
[15]Liu J, Zhang S K, Wang Q M, et al. Seroepidemiology of hepatitis B virus infection in 2 million men aged 21-49 years in rural China: a population-based, cross-pal study[J]. Lancet Infect Dis, 2016, 16(1): 80-86.
[16]Perrillo R P, Gish R, Falck-Ytter Y T. American Gastroenterological Association Institute technical review on prevention and treatment of hepatitis B virus reactivation during immunosuppressive drug therapy[J]. Gastroenterology, 2015, 148(1): 221-244.e3.
[17]Reddy K R, Beavers K L, Hammond S P, et al. American gastroenterological association institute guideline on the prevention and treatment of hepatitis B virus reactivation during immunosuppressive drug therapy[J]. Gastroenterology, 2015, 148(1): 215-219.
[18]Chen Y M, Huang W N, Wu Y D, et al. Reactivation of hepatitis B virus infection in patients with rheumatoid arthritis receiving tofacitinib: a real-world study[J]. Ann Rheum Dis, 2018, 77(5): 780-782.
[19]Akiyama S, Cotter T G, Sakuraba A. Risk of hepatitis B virus reactivation in patients with autoimmune diseases undergoing non-tumor necrosis factor-targeted biologics[J]. World J Gastroenterol, 2021, 27(19): 2312-2324.
[20]黄安芳, 罗妍, 赵毅, 等. 风湿病患者合并潜伏性结核感染的分析[J]. 中华内科杂志, 2016, 55(4): 307-310.
[21]Minozzi S, Bonovas S, Lytras T, et al. Risk of infections using anti-TNF agents in rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis: a systematic review and meta-analysis[J]. Expert Opin Drug Saf, 2016, 15(sup1): 11-34.
[22]Alves C, Penedones A, Mendes D, et al. The risk of infections associated with JAK inhibitors in rheumatoid arthritis: a systematic review and network meta-analysis[J]. J Clin Rheumatol, 2022, 28(2): e407-e414.
[23]Thatiparthi A, Martin A, Liu J, et al. Biologic treatment algorithms for moderate-to-severe psoriasis with comorbid conditions and special populations: a review[J]. Am J Clin Dermatol, 2021, 22(4): 425-442.
[24]Mease P J, Gladman D D, Ritchlin C T, et al. Adalimumab for the treatment of patients with moderately to severely active psoriatic arthritis: results of a double-blind, randomized, placebo-controlled trial[J]. Arthritis Rheum, 2005, 52(10): 3279-3289.
[25]Kavanaugh A, McInnes I B, Krueger G G, et al. Patient-reported outcomes and the association with clinical response in patients with active psoriatic arthritis treated with golimumab: findings through 2 years of a phase Ⅲ, multicenter, randomized, double-blind, placebo-controlled trial[J]. Arthritis Care Res (Hoboken), 2013, 65(10): 1666-1673.
[26]Mease P J, Fleischmann R, Deodhar A A, et al. Effect of certolizumab pegol on signs and symptoms in patients with psoriatic arthritis: 24-week results of a phase 3 double-blind randomised placebo-controlled study (RAPID-PsA)[J]. Ann Rheum Dis, 2014, 73(1): 48-55.
[27]Antoni C, Krueger G G, de Vlam K, et al. Infliximab improves signs and symptoms of psoriatic arthritis: results of the IMPACT 2 trial[J]. Ann Rheum Dis, 2005, 64(8): 1150-1157.
[28]McInnes I B, Mease P J, Kirkham B, et al. Secukinumab, a human anti-interleukin-17A monoclonal antibody, in patients with psoriatic arthritis (FUTURE 2): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2015, 386(9999): 1137-1146.
[29]Nash P, Coates L C, Kivitz A J, et al. Safety and efficacy of tofacitinib in patients with active psoriatic arthritis: interim analysis of OPAL balance, an open-label, long-term extension study[J]. Rheumatol Ther, 2020, 7(3): 553-580.
[30]McInnes I B, Kato K, Magrey M, et al. Upadacitinib in patients with psoriatic arthritis and an inadequate response to non-biological therapy: 56-week data from the phase 3 SELECT-PsA 1 study[J]. RMD Open, 2021, 7(3): e001838.
[31]Mease P J, Lertratanakul A, Papp K A, et al. Upadacitinib in patients with psoriatic arthritis and inadequate response to biologics: 56-week data from the randomized controlled phase 3 SELECT-PsA 2 study[J]. Rheumatol Ther, 2021, 8(2): 903-919.
[32]Kavanaugh A, Puig L, Gottlieb A B, et al. Maintenance of clinical efficacy and radiographic benefit through two years of ustekinumab therapy in patients with active psoriatic arthritis: results from a randomized, placebo-controlled phase Ⅲ trial[J]. Arthritis Care Res (Hoboken), 2015, 67(12): 1739-1749.
[33]Deodhar A, Helliwell P S, Boehncke W H, et al. Guselkumab in patients with active psoriatic arthritis who were biologic-naive or had previously received TNFα inhibitor treatment (DISCOVER-1): a double-blind, randomised, placebo-controlled phase 3 trial[J]. Lancet, 2020, 395(10230): 1115-1125.
[34]Mease P J, Gottlieb A B, Van Der Heijde D, et al. Efficacy and safety of abatacept, a T-cell modulator, in a randomised, double-blind, placebo-controlled, phase Ⅲ study in psoriatic arthritis[J]. Ann Rheum Dis, 2017, 76(9): 1550-1558.
[35]Edwards C J, Blanco F J, Crowley J, et al. Apremilast, an oral phosphodiesterase 4 inhibitor, in patients with psoriatic arthritis and current skin involvement: a phase Ⅲ, randomised, controlled trial (Palace 3)[J]. Ann Rheum Dis, 2016, 75(6): 1065-1073.
[36]McInnes I B, Behrens F, Mease P J, et al. Secukinumab versus adalimumab for treatment of active psoriatic arthritis (EXCEED): a double-blind, parallel-group, randomised, active-controlled, phase 3b trial[J]. Lancet, 2020, 395(10235): 1496-1505.
[37]Mease P J, Smolen J S, Behrens F, et al. A head-to-head comparison of the efficacy and safety of ixekizumab and adalimumab in biological-naïve patients with active psoriatic arthritis: 24-week results of a randomised, open-label, blinded-assessor trial[J]. Ann Rheum Dis, 2020, 79(1): 123-131.
[38]Nash P, Kirkham B, Okada M, et al. Ixekizumab for the treatment of patients with active psoriatic arthritis and an inadequate response to tumour necrosis factor inhibitors: results from the 24-week randomised, double-blind, placebo-controlled period of the SPIRIT-P2 phase 3 trial[J]. Lancet, 2017, 389(10086): 2317-2327.
[39]Reich K, Sullivan J, Arenberger P, et al. Secukinumab shows high and sustained efficacy in nail psoriasis: 2.5-year results from the randomized placebo-controlled TRANSFIGURE study[J]. Br J Dermatol, 2021, 184(3): 425-436.
[40]Coates L C, Wallman J K, McGonagle D, et al. Secukinu-mab efficacy on resolution of enthesitis in psoriatic arthritis: pooled analysis of two phase 3 studies[J]. Arthritis Res Ther, 2019, 21(1): 266.
[41]Vieira-Sousa E, Alves P, Rodrigues A M, et al. GO-DACT: a phase 3b randomised, double-blind, placebo-controlled trial of GOlimumab plus methotrexate (MTX) versus placebo plus MTX in improving DACTylitis in MTX-naive patients with psoriatic arthritis[J]. Ann Rheum Dis, 2020, 79(4): 490-498.
[42]Gladman D D, Orbai A M, Klitz U, et al. Ixekizumab and complete resolution of enthesitis and dactylitis: integrated analysis of two phase 3 randomized trials in psoriatic arthritis[J]. Arthritis Res Ther, 2019, 21(1): 38.
[43]McGonagle D, McInnes I B, Deodhar A, et al. Resolution of enthesitis by guselkumab and relationships to disease burden: 1-year results of two phase 3 psoriatic arthritis studies[J]. Rheumatology (Oxford), 2021, 60(11): 5337-5350.
[44]Singh J A, Guyatt G, Ogdie A, et al. Special article: 2018 American College of Rheumatology/National Psoriasis Foundation guideline for the treatment of psoriatic arthritis[J]. Arthritis Care Res (Hoboken), 2019, 71(1): 2-29.
[45]Robinson P C, Van Der Linden S, Khan M A, et al. Axial spondyloarthritis: concept, construct, classification and implications for therapy[J]. Nat Rev Rheumatol, 2021, 17(2): 109-118.
[46]Van Der Horst-Bruinsma I, Van Bentum R, Verbraak F D, et al. The impact of certolizumab pegol treatment on the incidence of anterior uveitis flares in patients with axial spondyloarthritis: 48-week interim results from C-VIEW[J]. RMD Open, 2020, 6(1): e001161.
[47]Van Bentum R E, Heslinga S C, Nurmohamed M T, et al. Reduced occurrence rate of acute anterior uveitis in ankylosing spondylitis treated with golimumab-the GO-EASY study[J]. J Rheumatol, 2019, 46(2): 153-159.
[48]Sandborn W J, Hanauer S B, Rutgeerts P, et al. Adalimumab for maintenance treatment of Crohn's disease: results of the CLASSIC Ⅱ trial[J]. Gut, 2007, 56(9): 1232-1239.
[49]Sandborn W J, Feagan B G, Stoinov S, et al. Certolizumab pegol for the treatment of Crohn's disease[J]. N Engl J Med, 2007, 357(3): 228-238.
[50]Adedokun O J, Xu Z H, Marano C W, et al. Pharmacokinetics and exposure-response relationship of golimumab in patients with moderately-to-severely active ulcerative colitis: results from phase 2/3 PURSUIT induction and maintenance studies[J]. J Crohns Colitis, 2017, 11(1): 35-46.
[51]Deodhar A, Sliwinska-Stanczyk P, Xu H J, et al. Tofacitinib for the treatment of ankylosing spondylitis: a phase Ⅲ, randomised, double-blind, placebo-controlled study[J]. Ann Rheum Dis, 2021, 80(8): 1004-1013.
[52]Van Der Heijde D, Song I H, Pangan A L, et al. Efficacy and safety of upadacitinib in patients with active ankylosing spondylitis (SELECT-AXIS 1): a multicentre, randomised, double-blind, placebo-controlled, phase 2/3 trial[J]. Lancet, 2019, 394(10214): 2108-2117.
[53]Deodhar A, Van Den Bosch F, Poddubnyy D, et al. Upadacitinib for the treatment of active non-radiographic axial spondyloarthritis (SELECT-AXIS 2): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2022, 400(10349): 369-379.
[54]Mulleman D, Lauféron F, Wendling D, et al. Infliximab in ankylosing spondylitis: alone or in combination with methotrexate? A pharmacokinetic comparative study[J]. Arthritis Res Ther, 2011, 13(3): R82.
[55]Nissen M J, Ciurea A, Bernhard J, et al. The effect of comedication with a conventional synthetic disease-modifying antirheumatic drug on drug retention and clinical effectiveness of anti-tumor necrosis factor therapy in patients with axial spondyloarthritis[J]. Arthritis Rheumatol, 2016, 68(9): 2141-2150.
[56]Ramiro S, Van Der Heijde D, Van Tubergen A, et al. Higher disease activity leads to more structural damage in the spine in ankylosing spondylitis: 12-year longitudinal data from the OASIS cohort[J]. Ann Rheum Dis, 2014, 73(8): 1455-1461.
[57]Molto A, López-Medina C, Van Den Bosch F E, et al. Efficacy of a tight-control and treat-to-target strategy in axial spondyloarthritis: results of the open-label, pragmatic, cluster-randomised TICOSPA trial[J]. Ann Rheum Dis, 2021, 80(11): 1436-1444.
[58]中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2022年版)[J]. 中华传染病杂志, 2023, 41(1): 3-28.
[59]Sinagra E, Perricone G, Romano C, et al. Heart failure and anti tumor necrosis factor-alpha in systemic chronic inflammatory diseases[J]. Eur J Intern Med, 2013, 24(5): 385-392.
[60]Sun W T, He Y H, Dong M M, et al. The comparative safety of biological treatment in patients with axial spondylarthritis: a meta-analysis of randomized controlled trials with placebo[J]. Eur Rev Med Pharmacol Sci, 2020, 24(19): 9824-9836.
[61]Xie W H, Xiao S Y, Huang Y R, et al. A meta-analysis of biologic therapies on risk of new or recurrent cancer in patients with rheumatoid arthritis and a prior malignancy[J]. Rheumatology (Oxford), 2021, 60(5): 2495.
[62]Winthrop K L, Cohen S B. Oral surveillance and JAK inhibitor safety: the theory of relativity[J]. Nat Rev Rheumatol, 2022, 18(5): 301-304.
[63]Goodman S M, Springer B D, Chen A F, et al. 2022 American College of Rheumatology/American Association of Hip and Knee Surgeons guideline for the perioperative management of antirheumatic medication in patients with rheumatic diseases undergoing elective total hip or total knee arthroplasty[J]. Arthritis Care Res (Hoboken), 2022, 74(9): 1399-1408.
[64]Clowse M E B, Scheuerle A E, Chambers C, et al. Pregnancy outcomes after exposure to certolizumab pegol: updated results from a pharmacovigilance safety database[J]. Arthritis Rheumatol, 2018, 70(9): 1399-1407.
[65]Gisbert J P, Chaparro M. Safety of new biologics (vedolizumab and ustekinumab) and small molecules (tofacitinib) during pregnancy: a review[J]. Drugs, 2020, 80(11): 1085-1100.
[66]Flint J, Panchal S, Hurrell A, et al. BSR and BHPR guideline on prescribing drugs in pregnancy and breastfeeding-Part I: standard and biologic disease modifying anti-rheumatic drugs and corticosteroids[J]. Rheumatology (Oxford), 2016, 55(9): 1693-1697.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#靶向药物# #脊柱关节炎#
26