Daratumumab皮下制剂治疗多发性骨髓瘤:CHMP持积极意见
Genmab制药公司今日宣布,欧洲药品管理局(EMA)人用药品委员会(CHMP)发表了积极意见,建议使用daratumumab皮下制剂治疗复发难治多发性骨髓瘤患者。
MedSci原创 - 多发性骨髓瘤,Daratumumab - 2020-05-01
欧盟授权阿斯利康的COVID-19疫苗AZD1222
本周五,欧盟委员会授予阿斯利康和牛津大学COVID-19疫苗AZD1222有条件销售许可,适用于18岁及18岁以上的人群。
MedSci原创 - COVID-19疫苗,AZD1222 - 2021-01-30
VAXNEUVANCE(肺炎球菌15价结合疫苗)或可在欧洲用于对18岁及以上人群
默克公司今天宣布,欧洲药品管理局人用药品委员会(CHMP)已建议批准VAXNEUVANCE™(肺炎球菌15价结合疫苗)用于主动免疫。
MedSci原创 - 肺炎球菌 - 2021-10-15
CHMP对RoActemra用于活动性幼年特发性关节炎(sJIA)持积极意见
罗氏制药近日宣布,欧洲人用药品委员会(CHMP)对RoActemra®(托珠单抗)皮下(SC)给药治疗1岁及以上患者的全身性幼年特发性关节炎(sJIA)持积极意见。
MedSci原创 - 幼年特发性关节炎,RoActemra,CHMP - 2018-09-27
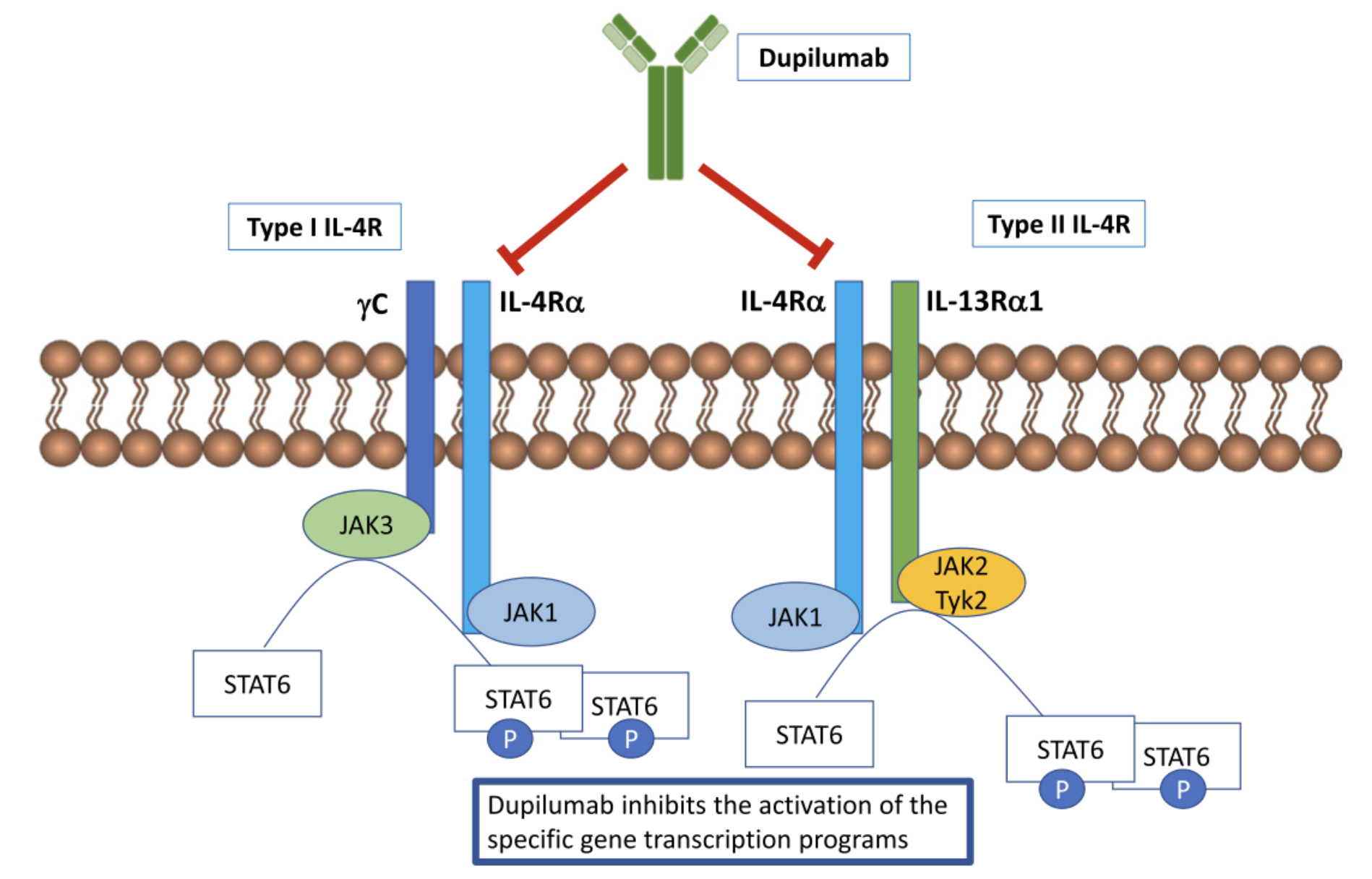
幼儿哮喘患者的福音,CHMP批准Dupixent用于患有哮喘的幼儿患者
Dupilumab是一种人IgG4抗体,能够抗IL-4受体 (IL-4R) α亚基,可阻断由IL-4和IL-13诱导的IL-4R信号传导,下调驱动2型炎症性疾病的分子途径。
MedSci原创 - 哮喘,Dupixent,IL-4/IL-13单抗Dupixent - 2022-02-01
CHMP支持Opdivo治疗食管、尿路上皮癌
百时美施贵宝本周五宣布,欧洲药品管理局人用药品委员会 (CHMP) 已就 Opdivo (nivolumab) 在两种一线食管鳞状细胞癌 (ESCC) 适应症和尿路上皮癌适应症中发表了积极意见。
MedSci原创 - CHMP,Opdivo,人用药品委员会(CHMP) - 2022-02-27
CHMP建议批准SOLIRIS(eculizumab)治疗神经脊髓炎光谱障碍
Alexion制药公司近日宣布,欧洲药品管理局(EMA)的人用药品委员会(CHMP)已发布积极意见,以扩大SOLIRIS®(eculizumab)目前的上市授权,包括治疗成人神经脊髓炎光谱障碍(NMOSD
MedSci原创 - Eculizumab,神经脊髓炎光谱障碍,CHMP - 2019-07-28
XENLETA(lefamulin)治疗社区获得性肺炎(CAP):欧盟CHMP持积极意见
社区获得性肺炎(community-acquired pneumonia, CAP)是全球发病和死亡的主要原因。
MedSci原创 - 社区获得性肺炎,Lefamulin - 2020-06-01
CHMP对Sarepta的DMD治疗持负面看法
Sarepta表示,在欧洲批准的杜氏肌营养不良疗法可能会有延迟,这表明这表明欧洲药品管理局人用药品委员会(CHMP)的投票结果是否定的。"根据与CHMP代表的讨论,我们了解到CHMP没有得出eteplirsen对于51号外显子患者无效的结论,而是Sarepta尚未达到有条件批准的监管门槛,部分原因是由于在研究中使用外部控制作为比较对象。"
MedSci原创 - CHMP,Sarepta的DMD治疗 - 2018-05-05
欧洲药品管理局开始审查芬戈莫德
2012年1月20日,欧洲药品管理局(EMA)发表声明称,其已开始审查治疗多发性硬化症的药物芬戈莫德(Gilenya)的疗效和风险。
MedSci原创 - 芬戈莫德,多发性硬化症,EMA - 2012-02-03
欧盟批准利伐沙班用于急性冠状动脉综合征的二级预防
5月24日,拜耳宣布欧洲委员会批准口服凝血因子Xa抑制剂利伐沙班(拜瑞妥,拜耳/杨森制药)用于生物标志物确诊的急性冠状动脉综合征(ACS)成人患者的二级预防。针对该适应症,利伐沙班每天服用两次,每次2.5 mg,并与标准抗血小板治疗药物合并用药。今年3月份,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)主要基于随机的、有15000多名患者参与的ATLAS ACS 2 TIMI 51临床
dxy - ACS,利伐沙班,急性冠状动脉综合征,抗凝血药 - 2013-05-27
CHMP建议批准GSK黑色素瘤药物Mekinist
葛兰素史克(GSK)4月25日宣布,黑色素瘤药物Mekinist(trametinib)获得了欧洲药品管理局(EMA)人用医药产品委员会(CHMP)的积极意见。CHMP建议批准Mekinist作为一种单药疗法,用于携带BRAF V600突变(V600E或V600K)的不可切除性或转移性黑色素瘤成人患者的治疗。
生物谷 - 新药,黑色素瘤 - 2014-05-12
Otezla可能被欧盟批准用于斑块型银屑病治疗
生物技术巨头新基(Celgene)重磅药物Otezla(apremilast)近日在欧盟监管方面收获好消息,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已建议批准Otezla,用于2种适应症。欧盟委员会(EC)通常都会采纳CHMP的意见,这意味着Otezla将在未来2-3个月在欧盟获批上市。 在美国,FDA分别于2014年3月和9月批准Otezla用于活动性银屑病关节炎(PsA)及中度
不详 - 银屑病,Otezla - 2014-11-28
强生HIV复方药Rezolsta获欧盟批准
强生(JNJ)旗下杨森(Jassen)近日宣布,欧盟委员会(EC)已批准HIV复方药Rezolsta(darunavir/cobicistat)联合其他抗逆转录病毒(ARV)药物,用于18岁及以上人类免疫缺陷病毒
生物谷 - 复方药,HIV - 2014-11-28
欧盟支持阿哌沙班治疗深静脉血栓形成和肺栓塞
欧洲药品管理局(EMA)人用药产品委员会(CHMP)支持阿哌沙班(apixaban)适应证的扩大,即用于深静脉血栓形成(DVT)和肺栓塞(PE)的治疗和预防。CHMP的意见是基于AMPLIFY 试验结果和其延伸试验AMPLIFY-EXT的。
医学论坛网 - 阿哌沙班,深静脉血栓形成,肺栓塞 - 2014-07-03
为您找到相关结果约500个