FDA批准首款遗传佝偻病药物burosumab
新闻事件今天FDA批准了Ultragenyx(RARE)/ Kyowa Kirin合作开发的FGF23抗体burosumab(商品名Crysvita?)用于治疗一岁以上X-连锁低磷性佝偻病(XLH)。
美中药源 - 佝偻病 - 2018-04-19
Epcoritamab 寻求 FDA/欧洲批准用于复发/难治性 LBCL/DLBCL
已向 FDA 提交生物制剂许可申请,寻求批准皮下 epcoritamab 用于治疗 2 线或更多线全身治疗后的复发/难治性大 B 细胞淋巴瘤或弥漫性大 B 细胞淋巴瘤患者。
MedSci原创 - epcoritamab - 2022-10-29
百济神州的BTK抑制剂zanubrutinib治疗淋巴瘤,获得了FDA的优先审查
百济神州BeiGene的BTK抑制剂zanubrutinib获得了FDA的优先审查,明年2月可能获得批准。这是BeiGene的一个重要里程碑,也是其候选药物首次在美国申请并接受FDA审查。
MedSci原创 - 百济神州,BTK抑制剂,zanubrutinib,淋巴瘤,FDA优先审查 - 2019-08-26
教育部批准14所“学院”更名为“大学”
日前,教育部在其官方网站发布文件,批准14所“学院”更名为“大学”:湖北师范学院更名为湖北师范大学;安庆师范学院更名为安庆师范大学;赣南师范学院更名为赣南师范大学;河南中医学院更名为河南中医药大学;广东药学院更名为广东药科大学
教育部 - 大学,教育部 - 2016-04-02
【热点解读分享】糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则》。
网络 - 糖尿病,视网膜病变 - 2024-03-18
基于细胞的流感疫苗已接近欧洲批准
Seqirus制药是流感预防的全球领导者,近日宣布其基于细胞的四价流感疫苗(QIVc)已收到欧洲药品管理局(EMA)人用医疗产品委员会(CHMP)的积极意见,用于9岁及以上的人群。Seqirus计划在2019/20流感季节在欧洲推出FLUCELVAX®TETRA疫苗。
MedSci原创 - 流感疫苗,CHMP,Seqirus制药 - 2018-10-21
纳米抗体药Cablivi获FDA批准 治疗罕见凝血障碍
近日,FDA批准 Cablivi(Caplacizumab-Yhdp),用于治疗成人获得性血栓性血小板减少性紫癜(aTTP)。
健康界 - 纳米抗体药 - 2019-02-20
FDA批准两款糖尿病新药组合
近日,美国FDA批准了两款2型糖尿病新药组合,这两款药物均为每天注射一次的长效胰岛素与胰高血糖素样肽-1(GLP-1)类似物组合,针对单独使用胰岛素或GLP-1类似物不能有效控制血糖的患者,它们分别来自法国药企赛诺菲
药明康德 - 糖尿病新药 - 2016-11-24
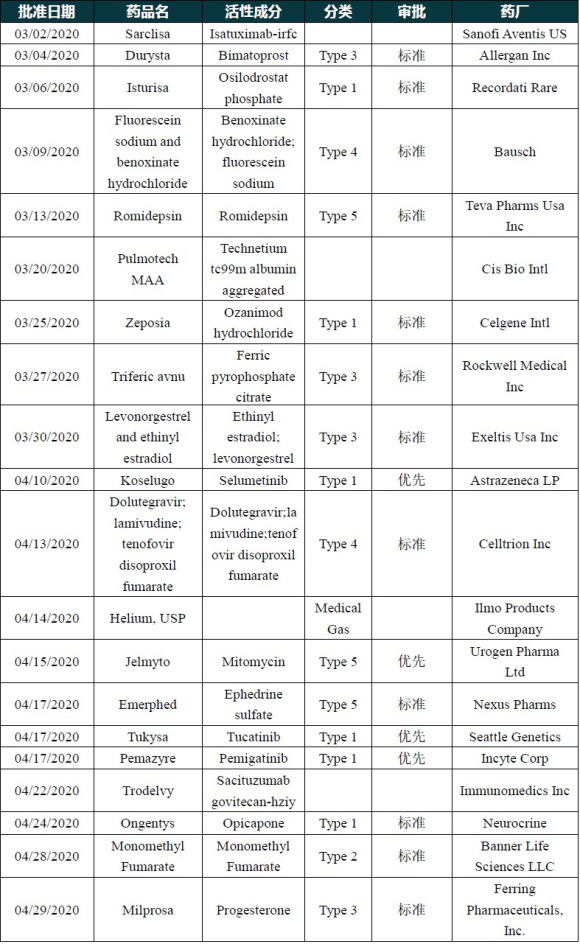
4月份,FDA和NMPA批准了哪些新药?
2020年1-4月批准了42个NDA/BLA申请新药,包括5个生物药,12个新分子实体(Type 1),7个新剂型(Type3),5个新组合(Type4),7个新配方或新制造商(Type5),2个已上
MedSci原创 - FDA,NMPA - 2020-05-07
FDA批准第五个生物类似物
近日FDA批准了罗氏明星产品Avastin的生物类似药物Mvasi治疗多种癌症,包括肠癌,肺癌,脑癌,肾癌以及子宫癌。本品也是美国首个获批的癌症生物仿制药。
HPC药闻药事 - 生物类似物,FDA - 2017-09-19
FDA 批准伊布替尼用于儿童慢性 GVHD 患者
根据 1/2 期 iMAGINE 试验的结果,FDA 已批准伊布替尼用于患有儿童慢性移植物抗宿主病的患者。
MedSci原创 - 伊布替尼 - 2022-08-25
Astellas宣布其FLT3抑制剂XOSPATA治疗白血病,正在NMPA接受监管审查
Gilteritinib属于第二代FLT3抑制剂,可抑制FLT3跨膜区内部串联重复(ITD)以及FLT3酪氨酸激酶结构域(TKD),这是2种常见的FLT3突变类型,约占所有AML病例的三分之一。
MedSci原创 - 急性髓性白血病,NMPA,FLT3抑制剂XOSPATA - 2020-04-11
NEJM:2013获FDA批准的新分子实体
FDA药物评价与研究中心每年都会批准多种不同的药物和诊断产品。这其中有些是新分子实体(NMEs),它们当中含有一种之前未批准过的活性成分。下面对2013年批准的27个NMEs进行了描述。
DXY - NEJM,FDA,新分子实体 - 2014-03-20
2012年有望获得FDA批准的26个热点药物
转载请注明生物谷 译文链接:http://blog.sina.com.cn/s/blog_4468f9470100zxmz.html 以下列出了26个2011年12月至2012年7月有可能获得FDA批准上市的药物生物技术的投资者知道,FDA的批准与否对该公司及其股价影响甚大。 在这
生物谷 - FDA,新药 - 2011-12-05
诺华治疗肢端肥大症长效药物获得FDA批准
美国FDA最近批准了诺华公司开发的用于治疗罕见疾病肢端肥大症的生长激素类药物Signifor登陆美国市场。这一药物也是继Sandostatin后,诺华公司在该领域开发的另一种主打产品。因此,诺华公司希望Signifor的批准能够填补公司在这一市场上的空白。 Signifor是一种肌肉注射用药物,这种药物能够结合患者体内的生长激素抑制素受体,进而下调患
生物谷 - 诺华,基因治疗 - 2014-12-18
为您找到相关结果约500个