AES 2020:抗癫痫药FYCOMPA的真实世界证据
Eisai制药公司在2020年美国癫痫病协会(AES)年会上展示了其抗癫痫药FYCOMPA®(perampanel)长期治疗癫痫发作的最新数据。
MedSci原创 - 癫痫症,FYCOMPA,Eisai制药公司 - 2020-12-08
梅斯医学张发宝博士:弥合裂痕——真实世界的临床证据
4月19日,由梅斯医学举办的"2016临床试验论坛"于国家会展中心(上海)召开,此次会议张发宝博士分享了主题为"真实世界的临床证据"的演讲。真实世界研究(RWS)将是未来研究的趋势,相对RCT而言,RWS的研究范围更广,更具有代表性,能够真实地反映研究的情况。是基于临床真实的情况采取的一种非随
梅斯医学 - 梅斯医学,张发宝,真实世界数据,临床试验 - 2016-04-22
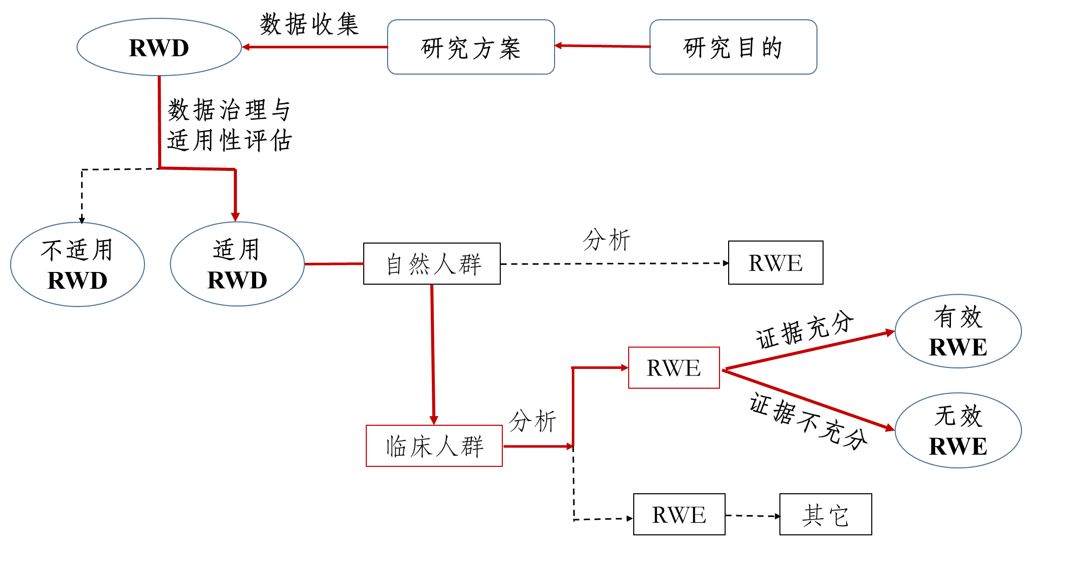
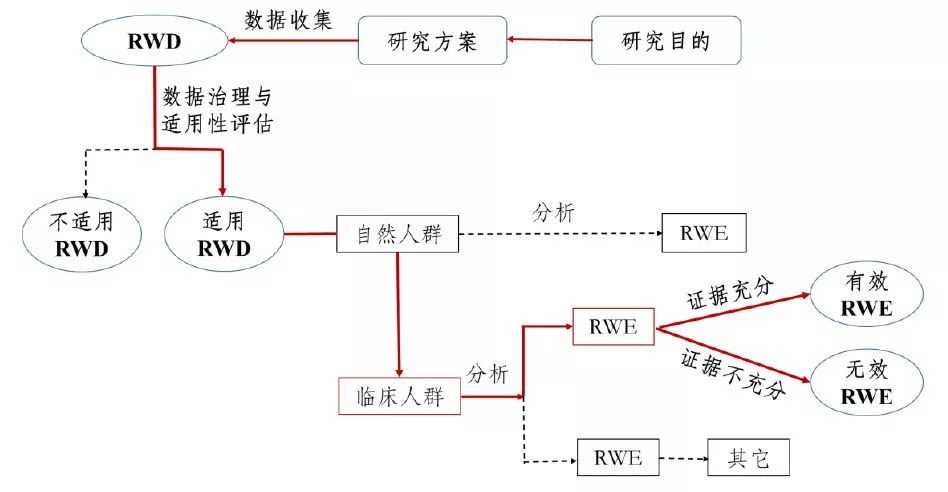
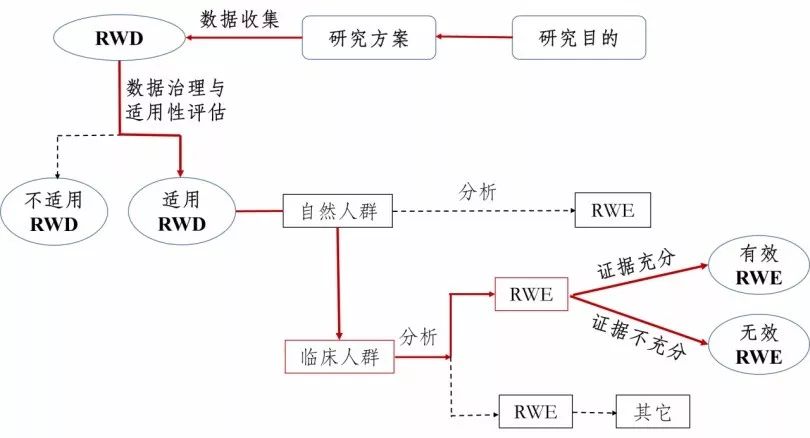
国家药监局药审中心关于发布《用于产生真实世界证据的真实世界数据指导原则(试行)》
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,药审中心组织制定了《用于产生真实世界证据的真实世界数据指导原则(试行)》(见附件)。
国家药品监督管理局药品审评中心 - 2021-04-15
真实世界证据支持药物研发与审评的指导原则(试行)
为进一步指导和规范真实世界证据用于支持药物研发和审评的有关工作,保障药物研发工作质量和效率,国家药品监督管理局组织制定了《真实世界证据支持药物研发与审评的指导原则(试行)》,现予发布。
CDE - 真实世界,证据 - 2020-01-11
支付方该如何看待真实世界证据用于罕见病?
药品的最终消费者,是患者;患者使用药品,离不开支付方(payer),当罕见病、支付方、真实世界证据(real world evidence, RWE)这几个热点聚焦在一起时,孤儿药研发中,有什么成功的RWE
药明康德 - 罕见病 - 2019-12-05
CDE发布《真实世界证据支持药物研发的基本考虑》意见稿
5月29日,动脉新医药获悉,国家药品监督管理局药品审评中心组织起草发布了《真实世界证据支持药物研发的基本考虑(征求意见稿)》。为鼓励研究和创制新药的要求,考虑到药物临床研发过程中,存在临床试验不可行或难以实施等情形,利用真实世界证据用以评价药物的有效性和安全性成为可能的一种策略和路径。
动脉网 - CDE,药物研发,罕见病 - 2019-05-30
真实世界证据支持药物研发的基本考虑(征求意见稿)
真实世界证据支持药物研发的基本考虑(征求意见稿)国家药品监督管理局药品审评中心2019年5月 一、 引言1.
CDE - 真实世界,药物研发 - 2019-05-29
真实世界证据支持药物研发审评,这四点思考值得关注!
1月7日,国家药监局把2020年的一号文件,留给了此前就备受行业关注的真实世界证据支持药物研发与审评。 在其官网上,药监局同时公布了《真实世界证据支持药物研发与审评指导原则(试行)》,以及该文件的起草说明。作为国内发布的首个真实世界证据支持药物研发与审评的指导文件,这被视为新药研发审评道路上的里程碑事件,并迅速引起了行业的密切关注。事实上,如何利用真实世界证据评价药物的有效性和安全性
E药经理人 - 真实世界,证据 - 2020-01-11
【证据驱动的营销策略】真实世界研究主题沙龙 邀请函
伴随着互联网的发展、大数据的应用、真实世界研究的证据等级提升,企业的营销转型有方法,有工具,快速开展产品证据的挖掘和医学信息的多渠道推广等合规高效的营销模式,从而助力学术推广的完美破局。
MedSci原创 - 真实世界研究,药企 - 2017-08-16
真实世界证据支持药物注册申请的沟通交流指导原则(试行)
为促进真实世界证据在药品注册申请中的应用实践,提高研发效率,针对申请人与审评机构开展真实世界证据支持注册申请的沟通交流给出具体要求和指导性建议,药审中心组织制定了《真实世界证据支持药物注册申请的沟通交
国家药品监督管理局药品审评中心 - 真实世界证据,真实世界证据支持药物 - 2023-02-23
CDE公开征求意见:儿童用药研究如何使用真实世界证据
5月18日,国家药监局药品审评中心发布通知,就《真实世界证据支持儿童药物研发与审评的技术指导原则(征求意见稿)》(以下简称指导原则)公开征求意见。征求意见时间为期一个月。
CDE - 儿童用药,真实世界证据 - 2020-05-19
FDA:CVM GFI #266 使用真实世界数据和真实世界证据来支持新动物药物的有效性
本指南描述了 CVM 打算如何评估提交给 CVM 的真实世界数据和真实世界证据,以证明新动物药物申请的有效性的实质性证据或新动物药物有条件批准申请的有效性的合理预期。 它还提供有关申办者如何在提交申请
FDA - 真实世界数据 - 2021-10-24
CDE:《真实世界证据支持药物研发的基本考虑》意见稿
以及中共中央办公厅、国务院办公厅印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)鼓励研究和创制新药的要求,考虑到药物临床研发过程中,存在临床试验不可行或难以实施等情形,利用真实世界证据用以评价药物的有效性和安全性成为可能的一种策略和路径
网络 - 真实世界证据,药物研发 - 2019-05-29
FDA行业指南:使用真实世界数据和真实世界证据向 FDA 提交文件以获取药物和生物制品审批
本指南旨在鼓励使用真实世界数据 (RWD) 的申办者和申请人生成真实世界证据 (RWE),作为向 FDA 提交监管文件的一部分,以简单、统一的格式提供有关其使用 RWE 的信息 . FDA 将仅将这些
FDA - 真实世界,真实世界数据 - 2021-10-24
为您找到相关结果约500个