肺癌丨阿替利珠单抗(T药)系列研究汇总
阿特珠单抗(Atezolizumab,Tecentriq)是一种人源化单克隆抗PD-L1抗体,它能够抑制PD-L1—PD-1和PD-L1—B7-1信号传导,并恢复肿瘤特异性T细胞免疫。
e药安全 - 阿替利珠单抗(T药) - 2022-11-18
药明生物未来的又一增长极:ADC和广泛的偶联药物全球领先CRDMO平台药明合联(WuXi XDC)将分拆上市
ADC行业正以势不可挡的速度快速发展。 根据弗若斯特沙利文的数据,全球已经批准了15个ADC药物,其中11个都是过去5年获批。
药明生物 - 2023-07-09
武田抗体偶联药物Adcetris获日本批准
武田(Takeda)宣布,抗体偶联药物Adcetris(brentuximab vedotin)获日本卫生劳动福利部(MHLW)批准,用于2种适应症:(1)复发性或难治性CD30阳性霍奇金淋巴瘤(HL)此前,日本MHLW已授予Adcetris治疗HL和sALCL的孤儿药地位,并授予Adcetris优先审查资格
生物谷 - 新药,FDA - 2014-01-20
抗体偶联药物(ADC)的挑战与前景
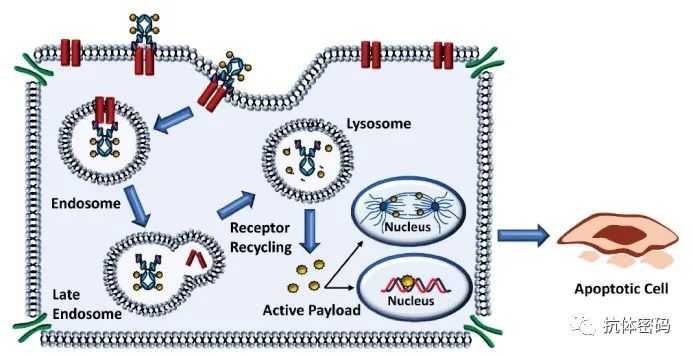
抗体偶联药物(ADCs)目前正在快速发展,其利用抗体选择性地将细胞毒性药物送到肿瘤部位。截至2021年5月,美国食品和药物管理局(FDA)已经批准了10种ADC。即Adcetris®、Kadc
抗体密码 - 抗体偶联药物 - 2021-09-12
帕博丽珠单抗单药治疗部分胃癌患者数据公布
近日,第55届美国临床肿瘤学会(ASCO)召开, 公布了多项重磅研究数据,包括近年来备受关注的肿瘤免疫治疗的最新进展。
医谷 - 默沙东,ASCO,帕博丽珠单抗,胃癌 - 2019-06-04
国家药监局药审中心关于发布《抗体偶联药物非临床研究技术指导原则》的通告(2023年第46号)
为进一步规范和指导抗体偶联药物的非临床研究与评价,提高企业研发效率,药审中心组织起草了《抗体偶联药物非临床研究技术指导原则》。
国家药品监督管理局药品审评中心 - 抗体偶联药物 - 2023-09-28
国内首个贝伐珠单抗生物类似药获批上市
近日,国家药品监督管理局批准齐鲁制药有限公司研制的贝伐珠单抗注射液(商品名:安可达)上市注册申请。该药是国内获批的首个贝伐珠单抗生物类似药,主要用于晚期、转移性或复发性非小细胞肺癌、转移性结直肠癌患者的治疗。 贝伐珠单抗是利用重组DNA技术制备的一种人源化单克隆抗体IgG1,通过与人血管内皮生长因子(VEGF)结合,抑制VEGF与其受体结合,阻断血管生成的信号传导途径,抑制肿瘤细胞生长。
国家药监局网站 - 贝伐珠单,生物类似药,上市 - 2019-12-09
首个国产生物类似药利妥昔单抗获批上市
2月22日,国家药品监督管理局批准上海复宏汉霖生物制药有限公司研制的利妥昔单抗注射液(商品名:汉利康)上市注册申请。该药是国内获批的首个生物类似药,主要用于非霍奇金淋巴瘤的治疗。生物类似药是指在质量、安全性和有效性方面与已获准注册的参照药具有相似性的治疗用生物制品。生物类似药上市有助于提高生物药的可及性和降低价格,可以更好地满足公众对生物治疗产品的需求。
国家药品监督管理局 - 利妥昔,单抗,肿瘤药物 - 2019-02-25
首个国产生物类似药利妥昔单抗获批上市!
2月22日,上海复宏汉霖生物制药有限公司研制的利妥昔单抗注射液(商品名:汉利康;产品代号:HLX01)获得国家药品监督管理局批准,成为了国内获批的首个生物类似药。该药获批了原研利妥昔单抗在中国的所有适应证[1],包括:1)复发或耐药的滤泡性中央型淋巴瘤;2)先前未经治疗的CD20阳性III-IV期滤泡性非霍奇金淋巴瘤;3)CD20阳性弥漫大B细胞淋巴瘤(DLBCL
医学界肿瘤频道 - 利妥昔单抗 - 2019-02-26
JCC:英夫利西单抗静脉给药与皮下给药治疗炎症性肠病的比较
将接受IV英夫利西单抗治疗的患者转变为SC制剂与较高的持续临床缓解率和较低的不良事件发生率相关。
MedSci原创 - 炎症性肠病,英夫利昔单抗 - 2024-04-27
Blood:派姆单抗单药治疗RRcHL可获得持久的缓解
研究人员开展了一个为期2年的2期临床试验,研究派姆单抗用于HL患者的疗效和安全性。共有210位患者,分成了3个队列。
MedSci原创 - 派姆单抗,RRcHL,程序性死亡蛋白1抑制剂 - 2019-08-14
EMA批准抗体偶联药物Adcetris上市
Adcetris是近30多年来首个获批用于复发性或难治性CD30阳性霍奇金淋巴瘤的靶向性治疗药物,对于CD30阳性复发性或难治性霍奇金淋巴瘤患者来说,欧盟委员会对于Adcetris的有条件上市许可批准,标志着该患者群体临床治疗的重大进步。
医学论坛网 - 抗体偶联药物,Adcetris,霍奇金淋巴瘤 - 2012-12-04
托珠单抗注射液生物类似药临床试验指导原则
为鼓励生物类似药研发,进一步规范和指导托珠单抗生物类似药的临床试验设计和终点选择,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《托珠单抗注射液生物类似药临床试验指导原则》(见
国家药品监督管理局药品审评中心 - 托珠单抗,指导原则 - 2021-05-13
国家药监局药审中心关于发布 《抗体偶联药物药学研究与评价技术指导原则》的通告(2024年第14号)
为规范和指导抗体偶联药物(Antibody-Drug Conjugate,ADC)产品的研发与申报,在国家药品监督管理局的部署下,药审中心组织制定了《抗体偶联药物药学研究与评价技术指导原则》(见附件)
国家药品监督管理局药品审评中心 - 2024-02-15
为您找到相关结果约500个