【每日一例】无菌性股骨头坏死
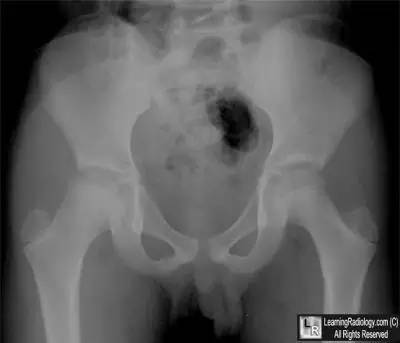
Legg-Calve-Perthes病:双髋前后位及蛙式侧位示右侧股骨头骨骺(黑箭)较左侧小(白箭),为该病一早期征象。
放射沙龙 learningradiology - 无菌性股骨头坏死,特发性股骨头缺血性坏死 - 2022-10-08
Gastroenterology:无菌粪便滤液同样能治疗艰难梭菌感染吗?
研究目的是,调查无菌粪便滤液(含细菌碎片、蛋白质、抗菌化合物、代谢产物和寡核苷酸/ DNA)而不是完整的微生物,对CDI的治疗是否有效。
MedSci原创 - 艰难梭菌感染,无菌粪便滤液,粪便菌群移植 - 2016-11-20
一次性使用无菌闭合夹注册技术审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《一次性使用无菌闭合夹注册技术审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 无菌闭合夹 - 2024-04-26
一次性使用无菌尿液引流袋注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《一次性使用无菌尿液引流袋注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 引流袋 - 2024-03-18
JAMA surg:术前无菌尿的筛查不影响手术预后
对于术前尿液有菌是否影响患者手术后的康复目前还没有定论,但是大多数专家认为术前进行无症状菌尿(ASB)的筛查是没有必要的,因此,本项研究就此问题进行了一项回顾性研究,探讨术前ASB检测与治疗及术后预后的关系。
MedSci原创 - Preoperative,asymptomatic,Bacteriuria,postoperative,outcome - 2018-12-15
一次性使用无菌三棱针产品注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《一次性使用无菌三棱针产品注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 无菌三棱针 - 2024-03-05
一次性使用无菌阴道扩张器注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《一次性使用无菌阴道扩张器注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 阴道扩张器 - 2024-03-06
非无菌产品微生物控制中水分活度应用指导原则研究
国家药典委员会于2017年设立了“水分活度在非无菌产品微生物控制中的应用指导原则”研究课题。本文从指导原则的制定背景、研究思路、主要内容、相关说明和应用展望等5个方面综合介绍。
《中国药品标准》 - 非无菌产品 - 2023-11-20
单次外周神经阻滞的无菌操作,是做全套还是偷偷简化?
发展早期的传统神经阻滞是根据解剖标志以及操作者所谓各种筋膜『突破感』进行盲穿,这种穿刺会面临很多问题:准确性差,并发症多,操作训练时间长,效果不确切。
梧桐医学 - 感染,无菌,外周神经阻滞 - 2024-01-13
Pediatrics:新型算法可有效区分细菌性和无菌性脑膜炎
新的生物标志物,如降钙素和C-反应蛋白,可能有助于识别细菌性脑膜炎低风险或高风险。近日,西班牙的一项研究旨在开发和验证一个评分(MSE),以区分在急诊科进行初步评估胸膜炎儿童时的细菌性脑膜
MedSci原创 - C-反应蛋白,细菌性脑膜炎 - 2020-12-11
Sci Rep:管周细胞中的ATP调控事件能够导致无菌睾丸炎症
管周类肌细胞能够在睾丸中形成曲细精管的壁组织,然而它的功能却仍旧未知。虽然它们能够转运精子和创造精原干细胞小生境,但它们在睾丸免疫监控和雄性不育方面越来越多的作用仍旧没有相关研究。之前,有研究人员在培养的管周细胞中,阐释了细胞因子的产生和Toll样受体(TLRs)的激活。最近,有研究人员展示了人管周细胞能够表达嘌呤受体P2RX4和P2RX7,这2个受体与TLRs具有功能性的联系,并且P2RX4是普
MedSci原创 - 睾丸炎,管周细胞,ATP - 2018-02-04
FDA:代替无菌测试作为无菌产品稳定性协议的一个组成部分的容器和封闭系统完整性测试
FDA:代替无菌测试作为无菌产品稳定性协议的一个组成部分的容器和封闭系统完整性测试
FDA - 无菌 - 2021-10-24
杜邦等无菌医疗包装行业巨头9月将齐聚上海Medtec中国展
美通社 - 2017-06-29
CFDA:1月1日起无新GMP认证无菌药企须停产
据国家食品药品监督管理总局网站消息,国家食品药品监督管理总局日前就无菌药品实施《药品生产质量管理规范(2010年修订)》有关事宜发布公告。公告指出,自2014年1月1日起,未通过新修订药品GMP认证的血液制品、疫苗、注射剂等无菌药品生产企业或生产车间一律停止生产。根据《药品生产质量管理规范(2010年修订)》(以下简称新修订药品GMP)实施规划,血液制品、疫苗、注射剂等无菌药品的生产必须在20
米内网 - 无新GMP,无菌药企须停产 - 2014-01-02
化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)(2020年)
为促进化学药品注射剂的研究和评价工作,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原
NMPA - 化学药品 - 2021-02-09
为您找到相关结果约500个