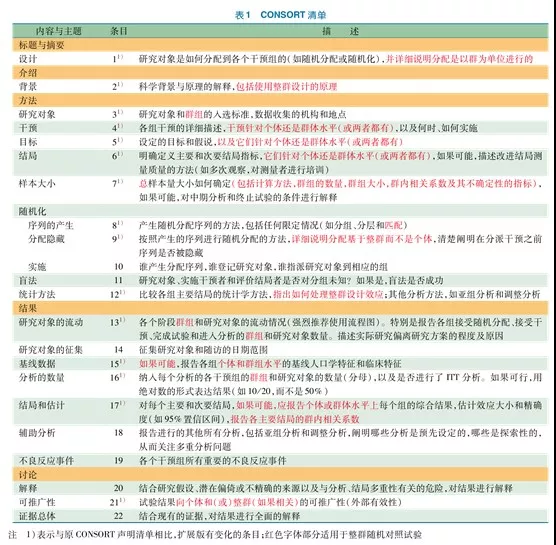
【讲堂】临床试验报告的统一标准(CONSORT)
一随机对照试验及其报告现状随机对照试验(RCT)通常是评估干预效果的最佳研究设计,但低质量的临床试验可能会错误地估计疗效。自2000年以来,每年都有25000篇随机或对照试验的文章被发表,但庞大的数量并不意味着决策者很容易找到可信的证据进行临床和保健决策,中国发表的随机对照试验文章质量亦令人堪忧。解决这些问题,一方面需从源头抓起,注重顶层设计和实施过程的质量控制;另一方面,完整、准确地报告研究论文
复旦循证护理中心 - 临床试验报告 - 2018-12-13
非随机对照试验报告规范——TREND规范简介
TREND规范简介以上就是非随机对照研究写作规范TREND Checklist的内容,需要注意的是,TREND规范只适用于采用非随机设计的关于干预效果评价的研究,并不适用于所有的非随机试验研究。希望大家通过本节的介绍,了解并严格按照TREND规范内容进行非随机对照研究报告的撰写。
MedSci原创 - 科研基金 - 2018-04-11
中药复方临床随机对照试验报告规范2017: CONSORT声明的扩展、说明与详述(附全文下载)
中医方剂随机对照试验报告国际标准当日通过美国《内科学年鉴》正式向全球发布,以简体中文、繁体中文、英文三种文字同期发表,并配发编者社论。该标准历时十年余,由中国、加拿大、英国学者组成的国际核心团队共同完成,包括香港浸会大学协理副校长、中医药学院临床部主任、我分会副会长卞兆祥教授,四川大学华西医院、我分会顾问李幼平教授、吴泰相副教授,北京中医药大学东直门医院
MedSci原创 - 中药,复方临床,随机对照试验,报告规范 - 2017-07-07
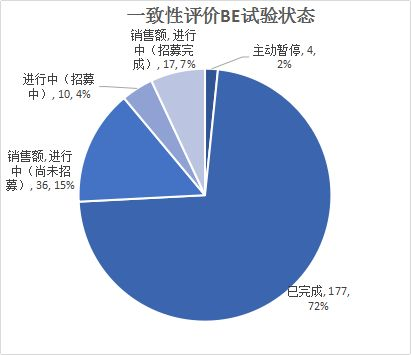
2019年国内临床试验年中报告,一致性评价BE试验占19%
随着仿制药质量和疗效一致性评价等政策的出台,临床试验的关注度不断提高。1.药物类别2019年上半年,CDE药物临床试验登记平台总共公示961个临床试验。2.国内试验和国际多中心试验目前药物临床试验平台中的临床试验多以国内试验为主,2019年上半年总计47个国际多中心试验,大多都是3期试验,主要研究安全性和有效性。从药品来看,基本均为新
药智网 - 一致性评价 - 2019-07-17
最新临床试验专场试验揭晓
侯静波获CIT青年医师一等奖 刘健获CIT最具教育意义病例奖 昨日(3月16日)下午,第十届中国介入心脏病学大会(CIT)最新临床试验专场的四项研究在众人期待中揭晓,本报记者刘敏第一时间为您传递TRACK-D 与任何商业利益无关的TRACK-D研究通过大样本的前瞻性多中心随机对照试验纳入患者2998例。结果显示,瑞舒伐他汀可降低伴有慢性肾病2~3期的糖尿病患者对比
MedSci原创 - 临床试验 - 2012-03-23
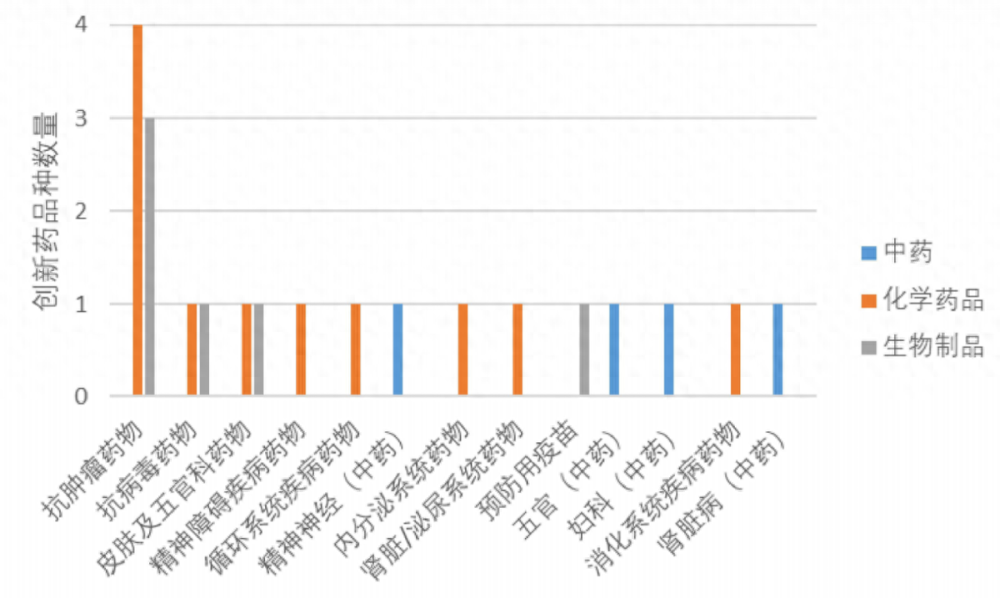
CDE发布中国新药注册临床试验进展年度报告(2022年)
9月7日,CDE官方公告显示,国家药监局药审中心发布《中国新药注册临床试验进展年度报告(2022年)》。
药研网 - 临床试验,CDE - 2023-09-10
CDE发布药物临床试验期间安全性数据快速报告常见问答
昨日(4月11日),国家药审中心发布《关于药物临床试验期间安全性数据快速报告常见问答(1.0版)》的通知》。
国家药品审评中心 - 药物临床试验,安全性数据 - 2019-04-13
实施临床试验报告规范,提高临床试验透明度
临床试验是指以人为对象的前瞻性研究,预先将受试者或受试人群分配至接受一种或多种医疗干预,以评价医疗干预对健康结局的影响。1、临床试验信息透明化的必要性 临床试验是获得防病治病知识的必要途径,主要目的是不断改进预防、诊断和治疗方法,提
MedSci原创 - 临床试验,规范,透明度 - 2014-04-24
CIT 2014预告:临床试验报告日程
最新临床试验 2014年3月21日星期五2:00 PM-3:00 PM 上海跨国采购会展中心二层201会议室 主持人:Patrick W.
医学论坛网 - CIT2014,最新临床试验,预告 - 2014-03-17
CTRC-AACR:多项贝伐单抗临床试验报告公布
在今年即将召开的圣安东尼奥乳癌研讨会(CTRC-AACR)上,将会报告两项新的临床试验研究(BEATRICE研究和LEA研究)。
MedSci原创 - CTRC-AACR,贝伐单抗,乳腺癌 - 2012-12-01
从中药复方临床随机对照试验报告规范谈我国临床试验的变革
中国循证医学杂志主编李幼平教授发表述评“从中药复方临床随机对照试验报告规范的正式发表谈我国临床试验的变革”。
中国循证医学杂志 - 临床试验,随机对照,中药复方 - 2017-09-21
Lancet:临床研究试验报告在医疗公关下扭曲
When doctors are deciding which drug to prescribe a patient, the idea behind evidence-based medicine is that they inform their thinking by consulting scientific literature. To a great extent, th
MedSci原创 - 临床研究,试验报告 - 2013-12-21
汤森路透:临床试验结果报告中的种种趋势
从Clinicaltrials.gov随机选择600项试验分析,显示其中仅50%的结果发表在文献中[3] 。但近日一项研究报告称Clinicaltrials.gov注册的大型临床试验中30%左右都未发表[2] 筛查“Cortellis临床试验情报”,我们发现2000年-2010年完成的临床试验平均40%有结果按试验完成年份的实际比例见图1。 为进一步评估临
汤森路透 - 临床试验 - 2014-10-22
BMJ: 期刊文章和临床试验注册中心报告漏报主要危害数据
为了测定临床试验方案、临床研究报告和主要的公开资源(期刊文章和试验注册)之间的数据在疗效和重大危害方面是否有矛盾的地方,以及临床研究报告本身是否矛盾,采用度洛西汀治疗重度抑郁症的研究作为研究对象。9个随机的度洛西汀安慰剂对照试验(共2878个病人)用于重度抑郁症提交给欧盟药品管理局(EMA)审批。研究者于2011年5月从EMA获得包含
MedSci原创 - 度洛西汀,数据来源 - 2014-11-03
患者报告结局:ePRO评估在临床试验的过去、现在和未来
患者报告结局(PROs)是用来评估新的医疗产品的治疗效果一种非常重要的方式。通常认为PRO评估应用于评估一些概念,这些概念要么患者非常清楚,要么从患者角度可以被很好的测量。此外,技术的进步已经显著的增加了临床试验中电子化PRO(ePRO)数据收集的功能和选项。从纸质数据到电子化PRO数据的转变已经增强了临床试验数据的完整性和精确性,且监管机构也
BioMed数据坊 - 患者,评估 - 2017-03-12
为您找到相关结果约500个